Clear Sky Science · nl
De consensus moleculaire subtypes van plaveiselcelcarcinoom van de slokdarm
Waarom dit onderzoek van belang is voor patiënten
Plaveiselcelcarcinoom van de slokdarm is een dodelijke keelkanker met weinig op maat gemaakte behandelopties en over het algemeen slechte overleving. Artsen weten dat niet alle tumoren zich hetzelfde gedragen, maar tot nu toe was er geen duidelijke, eenduidige manier om deze kankers in biologisch betekenisvolle groepen te verdelen. Deze studie brengt veel onderdelen van genetische en beeldvormingsgegevens samen om vier hoofdtypen van deze kanker te definiëren en toont aan dat een eenvoudige microscoopplaat vaak kan onthullen welk type een patiënt heeft. Dat opent de deur naar nauwkeurigere, minder op proef-en-fout gebaseerde behandelingen.
Orde scheppen in een verwarrend kankerlanschap
In het afgelopen decennium stelden verschillende onderzoeksteams minstens zeven manieren voor om deze kanker te verdelen op basis van DNA-mutaties, kopie‑aantalveranderingen, genactiviteit of andere moleculaire metingen. Elk systeem gebruikte verschillende gegevens en methoden, wat leidde tot overlappende maar niet identieke subtypes en het moeilijk maakte om ze in de dagelijkse praktijk te gebruiken. De auteurs heranalyseerden eerst een goed gekarakteriseerde groep van 152 Chinese patiënten waarvoor meerdere datalagen beschikbaar waren, waaronder gehele-genoomsequencing, genexpressie, DNA-methylering en microRNA-profielen. Met een methode genaamd similarity network fusion combineerden ze al deze gegevens tot één beeld en identificeerden vier multi-omics-subtypen. Vervolgens bouwden ze een statistisch “netwerk van subtypen” dat hun nieuwe groepen koppelde aan 21 eerder gepubliceerde, waardoor sterke verbanden tussen studies zichtbaar werden.
Vier belangrijke biologische persoonlijkheden van de tumor
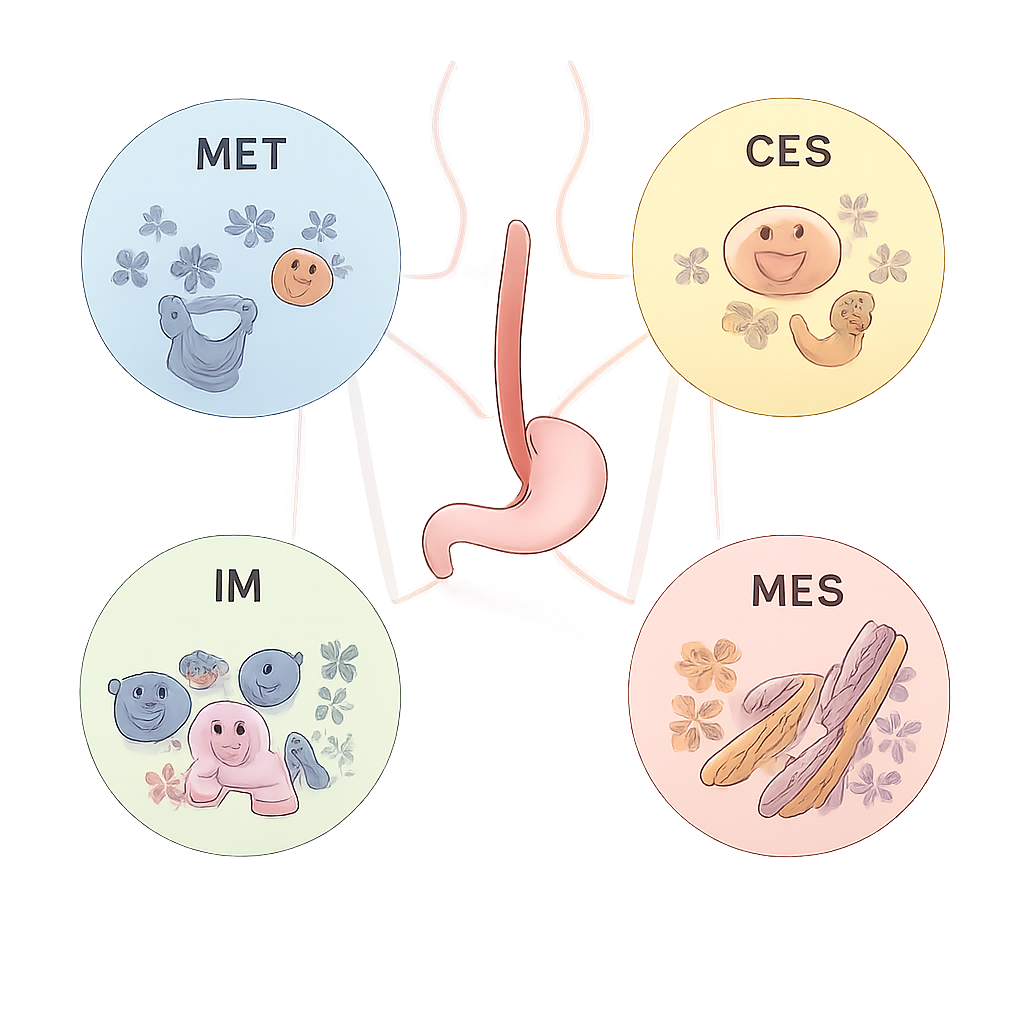
Uit dit netwerk destilleerde het team vier consensus moleculaire subtypes, ECMS1 tot en met ECMS4, elk met een verschillend gedrag. ECMS1, het metabolische type (MET), vertoont hoge activiteit in routes die geneesmiddelen en voedingsstoffen verwerken en frequente activatie van het NFE2L2-gen, wat resistentie tegen chemotherapie en radiotherapie kan stimuleren. ECMS2, het klassieke type (CLS), wordt gedomineerd door sterke celcyclus- en groeisignaalactiviteit en draagt vaak extra kopieën van het ERBB2 (HER2)-gen. ECMS3, het immuun type (IM), heeft een lagere totale mutatielast maar sterke immuunactivatie, inclusief hoge niveaus van het PD-1 checkpointpad. ECMS4, het mesenchymale type (MES), toont tekenen van weefselremodellering, angiogenese en cellen die mobieler en invasiever worden, kenmerken die gekoppeld zijn aan slechtere uitkomsten.
Subtypen koppelen aan prognose en behandelkeuzes
Toen de onderzoekers deze vier groepen vergeleken met klinische gegevens van patiënten, kwamen duidelijke patronen naar voren. Patiënten met mesenchymale ECMS4-tumoren hadden het hoogste risico op recidief en de slechtste totale en ziektevrije overleving. De immuun ECMS3-groep, ondanks een actief immuunmilieu, reageerde slecht op standaard chemoradiotherapie maar liet een hogere kans op voordeel zien bij een anti-PD-1-immunotherapie. De klassieke ECMS2-tumoren leken gevoeliger voor gangbare cytostatica zoals cisplatina en taxanen, en hun frequente HER2-amplificatie suggereert dat ze baat kunnen hebben bij HER2-gerichte middelen. De metabolische ECMS1-tumoren, verrijkt voor NFE2L2-activiteit en bepaalde groeifactorreceptoren, kunnen beter reageren op middelen die die metabole en signaalroutes targeten. Kort gezegd suggereren de vier subtypen verschillende zwakke punten en verschillende waarschijnlijke therapieresponsen.
Een computer leren moleculaire aanwijzingen te zien in routinekleuringen
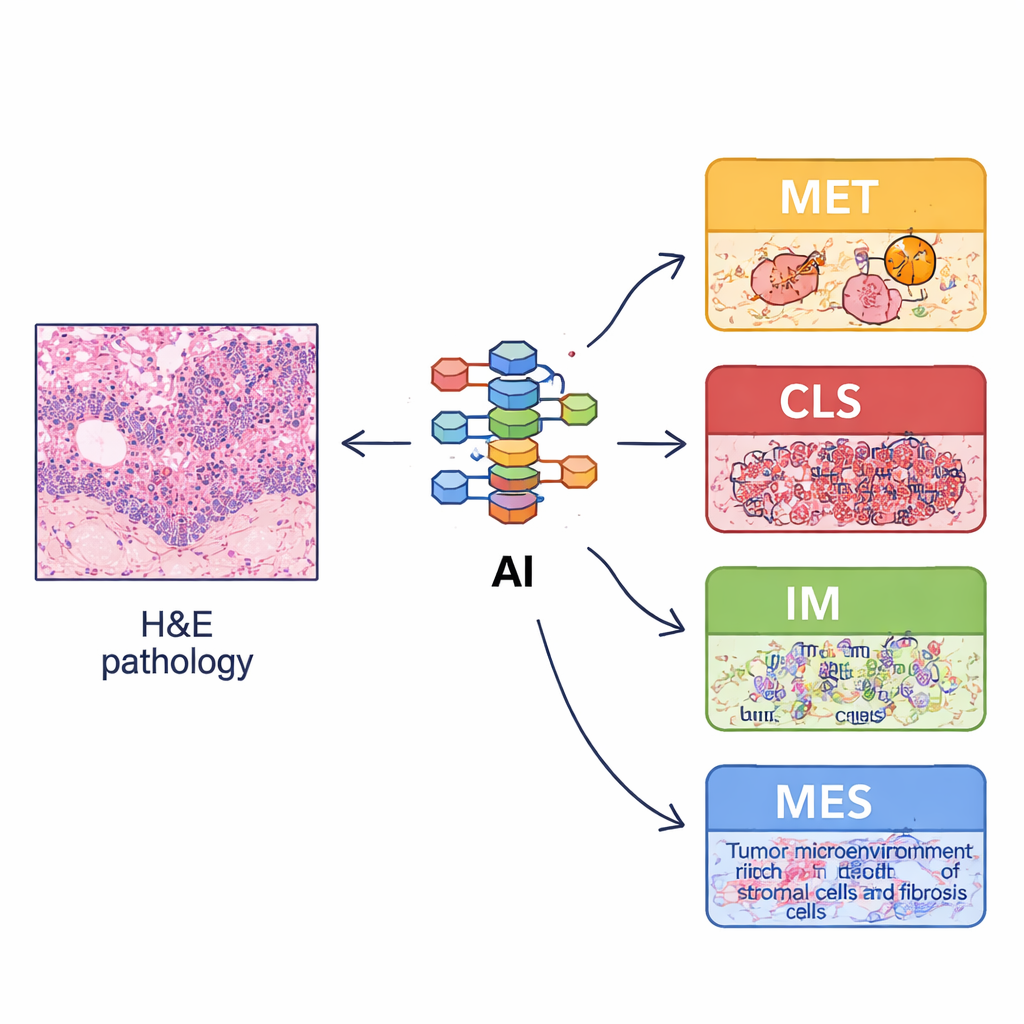
Aangezien volledige moleculaire profilering duur is en in veel ziekenhuizen niet beschikbaar, vroegen de onderzoekers zich af of gewone hematoxyline‑en‑eosine (H&E) pathologieplaatjes als proxy konden dienen. Ze trainden een deep‑learning‑systeem op tienduizenden geannoteerde afbeeldingssnippetjes om basale weefselelementen te herkennen zoals tumorcellen, stroma, lymfocyten, klieren en spierweefsel. Uit hele-slide afbeeldingen berekenden ze vervolgens “ruimtelijke organisatiekenmerken” – hoeveel van elk weefseltype aanwezig is, hoe ze gerangschikt zijn en hoe gemengd of gescheiden ze zijn. Deze beeldafgeleide patronen weerspiegelden de biologie van de vier subtypen: zo toonde het immuun ECMS3-type meer lymfocyten en normale structuren, terwijl het mesenchymale ECMS4-type meer ondersteunend stroma liet zien. Met deze kenmerken bouwden ze een op beelden gebaseerde classifier, imECMS genaamd, die in staat was om platen toe te wijzen aan MET, CLS, IM of MES met goede nauwkeurigheid in meerdere onafhankelijke patiëntgroepen.
Wat dit betekent voor toekomstige zorg
Voor niet‑specialisten is de conclusie dat deze studie een ogenschijnlijk uniforme kanker transformeert in vier biologisch onderscheiden ziekten, elk met een eigen waarschijnlijke beloop en beste behandelingsstrategie. Nog belangrijker is dat veel van deze informatie automatisch kan worden afgeleid uit standaard microscoopbeelden die elke patiënt al heeft, zonder dure sequencing. Met verdere validatie in grotere en diversere populaties zouden de ECMS- en imECMS-systemen artsen kunnen helpen patiënten met plaveiselcelcarcinoom van de slokdarm te matchen met de therapieën waarvan ze het meest waarschijnlijk zullen profiteren, terwijl ze worden bespaard van behandelingen die waarschijnlijk niet werken.
Bronvermelding: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Trefwoorden: slokdarmkanker, tumorsubtypen, precisie-oncologie, diepgaande leerpathologie, immunotherapie