Clear Sky Science · nl
Hyperglutaminolyse drijft veroudering en senescentie aan via activering van de arginine–mTORC1-as
Waarom dit onderzoek belangrijk is voor gezond ouder worden
Ouder worden gaat niet alleen over rimpels en grijs haar — het gaat erom dat cellen in het hele lichaam geleidelijk hun vermogen verliezen om zich te herstellen en te vernieuwen. Deze studie stelt een deceptief eenvoudige vraag met grote implicaties: helpt de manier waarop onze cellen het aminozuur glutamine verbranden hen daadwerkelijk richting ouderdom te duwen? De auteurs onthullen een eerder verborgen metabole keten die koppelt hoe cellen glutamine verwerken aan een krachtige groeischakelaar genaamd mTORC1, en tonen aan dat overmatige activatie van dit pad cellulaire veroudering actief kan versnellen in vliegen en muizen.
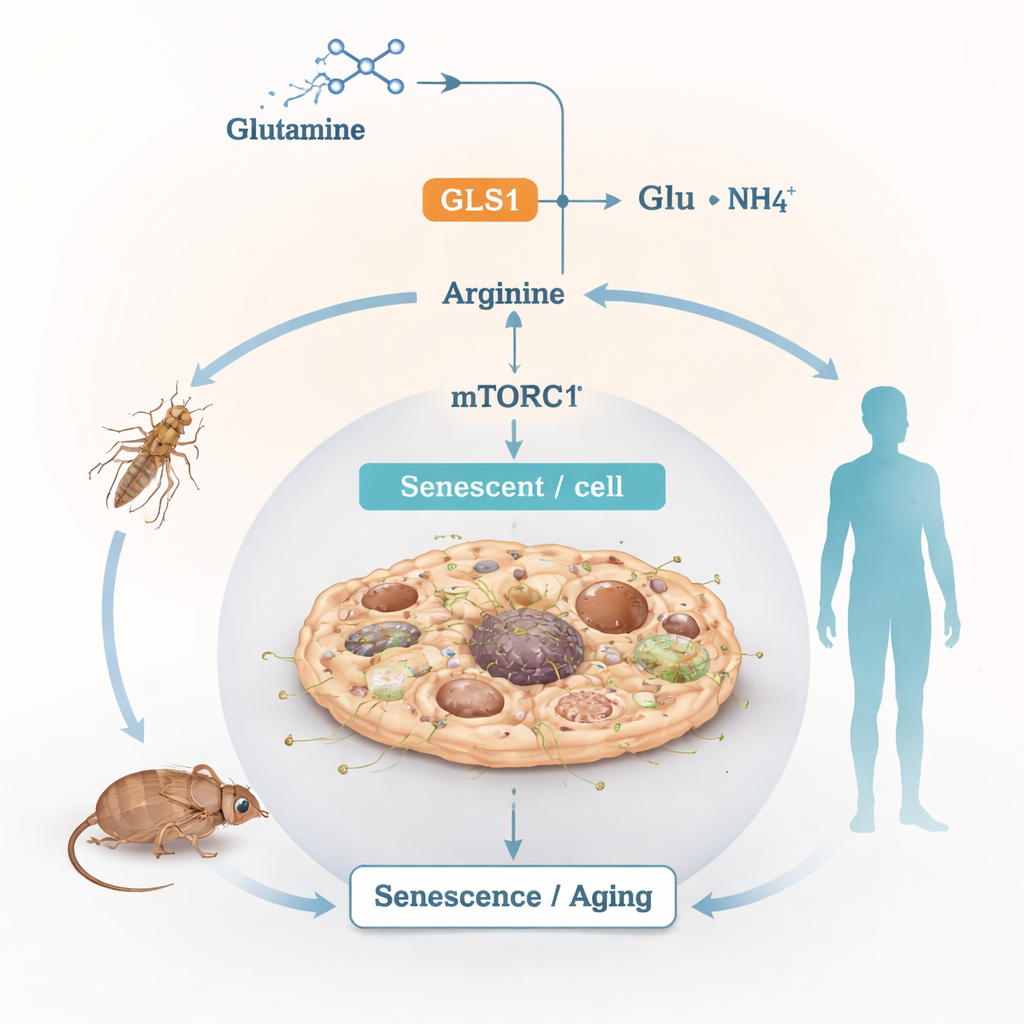
Een brandstofleiding die te heet loopt
Glutamine is het meest voorkomende vrije aminozuur in ons bloed en weefsels. Cellen gebruiken het als veelzijdige brandstof en bouwsteen, en breken het af via een proces dat glutaminolyse heet. De eerste stap wordt uitgevoerd door een enzym genaamd GLS1, dat glutamine omzet in glutamaat en ammonium; vanaf daar voeden de producten energielevering, antioxidantafweer en de aanmaak van andere aminozuren. Hoewel deze afbraak cruciaal is voor normaal functioneren, vroegen de auteurs zich af wat er gebeurt als die chronisch overactief wordt in de context van veroudering en stress.
De ontdekking van “hyperglutaminolyse” in oude cellen en dieren
Met behulp van geavanceerde metabolietprofilering vergeleek het team jonge, delende cellen met senescente cellen — oudere cellen die zijn gestopt met delen en inflammatoire factoren uitscheiden. Ze ontdekten dat veel aminozuren waren verhoogd, met glutamine in het centrum van het herschikte netwerk. Senescente cellen verbruikten meer glutamine, hadden hogere GLS1-niveaus en -activiteit, en stapelden meer glutamaat en ammonium op. Vergelijkbare veranderingen verschenen in hele organismen: oudere fruitvliegen en oude muizen toonden verhoogde GLS-activiteit in meerdere weefsels. De auteurs noemden deze gedeelde staat van versterkte glutamineafbraak “hyperglutaminolyse” en suggereerden dat het een geconserveerd kenmerk van veroudering is, eerder dan een klein bijverschijnsel.
Het terugschakelen van glutamineafbraak vertraagt tekenen van veroudering
Als hyperglutaminolyse samengaat met veroudering, draagt het er dan daadwerkelijk aan bij? Om dit te testen blokkeerden de onderzoekers glutaminolyse op verschillende manieren: door glutamine in het kweekmedium te verlagen, GLS te remmen met geneesmiddelen, of GLS1 genetisch te verminderen. In gestresste of replicatief verouderde cellen verminderden deze ingrepen klassieke senescentiemarkers zoals SA-β-gal-kleuring, de celdelingsremmer p16 en inflammatoire “SASP”-signalen. Bij fruitvliegen gaf ofwel genetische knockdown van GLS of lage doses GLS-remmende middelen een verlenging van de levensduur, verbeterde klautervaardigheid (een maat voor vitaliteit) en verminderde leeftijdsgebonden darmlekkage. Belangrijk is dat wanneer glutaminolyse vanaf het begin van stress werd beperkt, het effect niet vooral kwam door het doden van oude cellen, maar door te voorkomen dat ze ten eerste senescent werden.
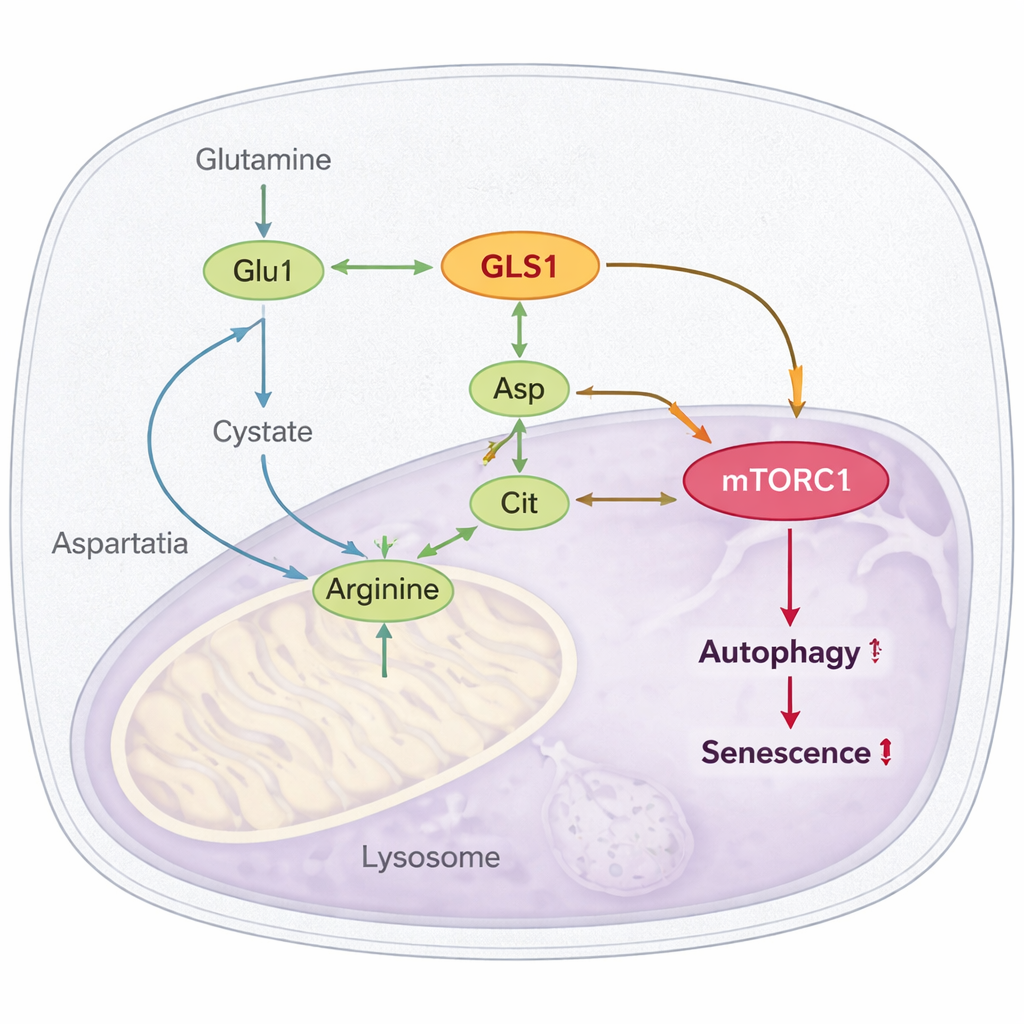
Een verborgen circuit: van glutamine naar arginine naar mTORC1
De meest opvallende bevinding is hoe dit overactieve pad wordt gekoppeld aan mTORC1, een meesterregelaar die, wanneer persistent geactiveerd, bekendstaat om veroudering te bevorderen en cellulaire recycling (autofagie) te blokkeren. De auteurs tonen aan dat hyperglutaminolyse de productie van arginine versterkt, een ander aminozuur dat mTORC1 direct activeert. Glutamaat en ammonium, gegenereerd uit glutamine, voeden de aanmaak van aspartaat en citrulline, die vervolgens worden gecombineerd tot arginine. In verouderde cellen en vliegen stijgen de niveaus van arginine en zijn voorlopers; het blokkeren van GLS of het knockdownen van een sleutelenzym in argininesynthese (ASL) verlaagt arginine en dempt mTORC1-activiteit. Ze tonen verder aan dat het arginine-sensorproteïne CASTOR1 vereist is voor dit effect: wanneer CASTOR1 wordt uitgeschakeld, dempt het blokkeren van glutaminolyse mTORC1 niet langer of verbetert autofagie niet, en gaat de verlichting van senescentie verloren.
Wanneer te veel van het goede veroudering versnelt
Om te zien of het simpelweg harder duwen op dit pad cellen sneller kan doen verouderen, overstroomde het team anders gezonde cellen wekenlang met glutamine, arginine of combinaties van de tussenliggende metabolieten. Het resultaat was een duidelijke stijging van senescentiemarkers en inflammatoire genen. Bij vliegen verkortte langdurige supplementatie met extra glutamine of arginine zowel de mediane als de maximale levensduur. Samengevat schetst het werk een volledige cascade: overmatige glutamineafbraak (hyperglutaminolyse) versterkt arginineproductie, wat door CASTOR1 wordt waargenomen, mTORC1 abnormaal actief houdt, cellulair opruimen onderdrukt en senescentie en organismale veroudering bevordert.
Wat dit betekent voor toekomstige anti-verouderingsstrategieën
Voor niet-specialisten herprofileert deze studie glutaminemetabolisme als een tweesnijdend zwaard: noodzakelijk voor gezondheid, maar potentieel schadelijk wanneer het chronisch overgedreven is in midden- tot latere levensfasen. Door een concreet pad van glutaminekatabolisme naar mTORC1-overactivatie in kaart te brengen, wijzen de auteurs nieuwe interventiepunten aan — zoals de enzymen GLS1 en ASL of de arginine-werkingsstap — die mogelijk kunnen worden bijgestuurd om leeftijdsgebonden achteruitgang te vertragen zonder vitale stofwisseling volledig uit te schakelen. Hoewel het veel te vroeg is om deze bevindingen te vertalen naar dieetadviezen of behandelingen, voegt het werk een belangrijk stuk toe aan de puzzel van hoe alledaagse nutriëntenverwerking onze cellen richting veerkracht of versnelde veroudering kan sturen.
Bronvermelding: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
Trefwoorden: glutaminemetabolisme, cellulaire senescentie, mTORC1-signaaloverdracht, argininesynthese, verouderingsinterventies