Clear Sky Science · nl
Ringvingereiwit 213 reguleert B-celreceptor‑signalering, metabolisme en ontwikkeling in B-lymfocyten
Hoe een weinig bekend eiwit antilichamen op koers houdt
Ons immuunsysteem is afhankelijk van B-cellen, de antilichaamproducerende fabrieken die ons helpen infecties te bestrijden en zich eerdere ziekteverwekkers te herinneren. Deze studie onthult hoe een reusachtig, interferon‑responsief eiwit genaamd RNF213 stilletjes B-cellen stuurt terwijl ze rijpen, gevaar waarnemen, hun eigen activiteit van energie voorzien en uiteindelijk effectieve antilichamen produceren. Inzicht in dit controlesysteem kan verklaren waarom sommige mensen kwetsbaarder zijn voor infecties of immuunonevenwicht, en kan zelfs een verband leggen tussen immuunproblemen en een zeldzame vaatziekte die met RNF213 wordt geassocieerd.
Een verkeersregelaar voor B-cellen
B-cellen doen veel meer dan enkel antilichamen uitscheiden: ze moeten zich door verschillende ontwikkelingsstadia bewegen, signalen van binnendringende microben lezen en hun metabolisme aanpassen aan energievraag. De onderzoekers ontdekten dat RNF213 fungeert als een cruciale verkeersregelaar tijdens deze processen in de milt, waar veel B-cellen zich bevinden. Muizen zonder RNF213 vertoonden een verstoorde balans tussen twee hoofdtypen B-cellen: follikel-B-cellen, die langdurige antilichaamreacties ondersteunen, en marginale zone-B-cellen, die snelle verdediging bieden tegen bepaalde in het bloed aanwezige microben. Hoewel het totale aantal B-cellen grotendeels ongewijzigd bleef, was de structuur van de B-celcompartimenten duidelijk verstoord, wat RNF213 aanwijst als een interne organisator van B-celpopulaties.
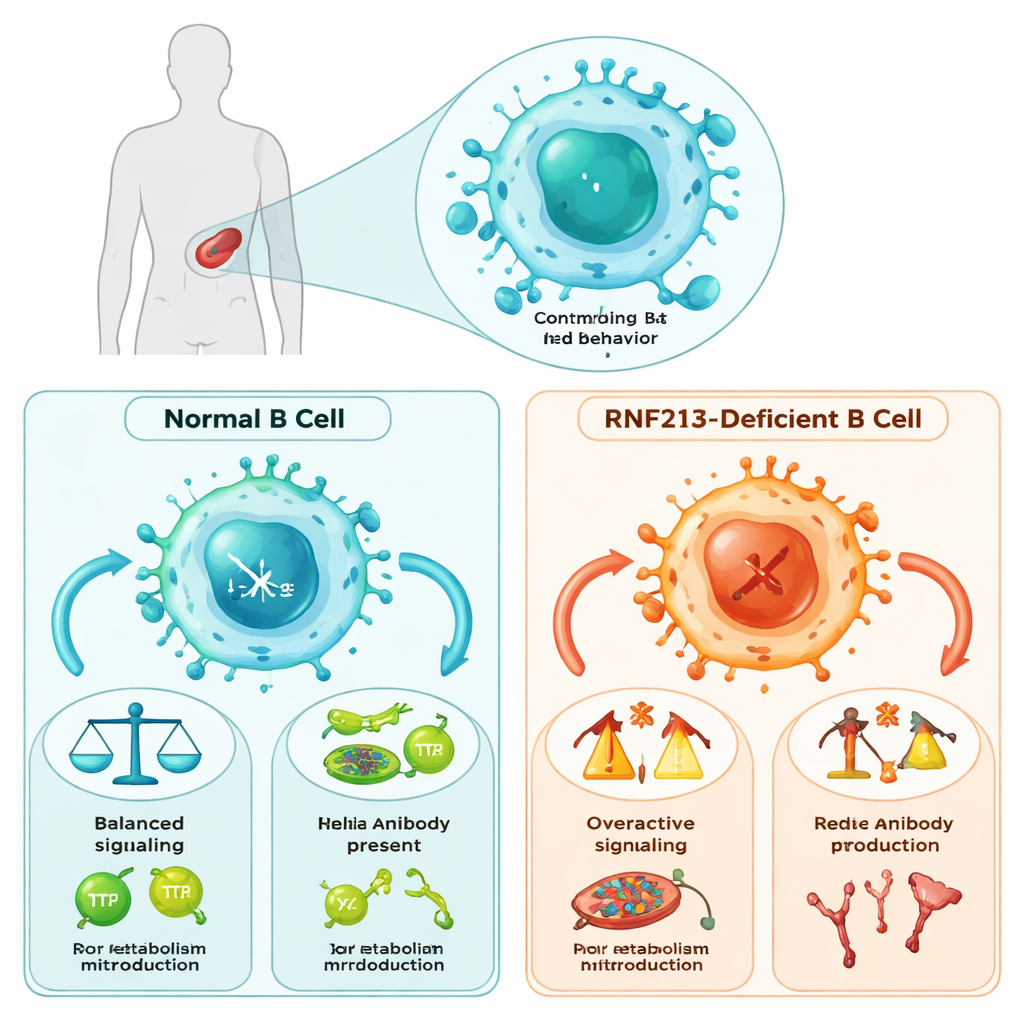
Wanneer B-cellen het alarm niet horen
Om hun taak te vervullen vertrouwen B-cellen op een moleculaire “antenne” genaamd de B-celreceptor (BCR), die vreemde moleculen detecteert en signaleringsk cascades binnen de cel activeert. In muizen zonder RNF213 functioneerde dit alarmsysteem slecht: BCR’s clusteren slecht aan het celoppervlak en belangrijke signaalmoleculen werden minder efficiënt geactiveerd. Verderop in de keten werden grote routes die genactiviteit en overleving regelen—zoals NFκB, STAT en MAPK—verzwakt. Het belangrijkst was dat de PI3K–AKT–mTOR-route, die binnenkomende signalen koppelt aan energiegebruik en groei, sterk verzwakte. Deze defecten werden gezien in meerdere B-celsubsets, wat aangeeft dat RNF213 een breed signaalraamwerk ondersteunt in plaats van één smalle route.
Stroomvoorzieningsproblemen binnen immuuncellen
Signaalverlies ging gepaard met een energietekort. Met metabolische testen toonden de auteurs aan dat RNF213‑deficiënte B-cellen verminderde mitochondriale functie hadden en minder reactieve zuurstofsoorten produceerden, die normaal gesproken fungeren als zorgvuldig gecontroleerde “vonken” voor immuunactivatie. Zowel glycolyse—de afbraak van suiker voor snelle energie—als oxidatieve fosforylering—de tragere mitochondriale energievoorziening—waren verminderd. Genexpressie‑analyses onthulden wijdverspreide dalingen in metabole programma’s, inclusief vetzuur- en cholesterolhandhaving. Samen pleiten deze bevindingen ervoor dat RNF213 niet alleen een signaalassistent is; het is ook essentieel om het metabolisme van B-cellen te herbedraden zodat cellen snel kunnen opschakelen bij blootstelling aan een antigeen.
Een moleaire kettingreactie: van genregelaar naar brandstofuitval
Dieper graven liet zien dat RNF213 een transcriptiefactor genaamd SPIB onder controle houdt. RNF213 labelt SPIB met een moleculair “afbraaklabel” en stuurt het naar het eiwitrecycling‑systeem van de cel. Zonder RNF213 hoopt SPIB zich op en activeert het extra kopieën van een gen genaamd Pik3c3, dat het enzym PIK3C3 codeert. Dit enzym produceert een lipidesignaal, PI3P, op vroege endosomen—kleine interne membraanzakjes. Overtollig PI3P trekt meer van het enzym PTEN naar deze membranen, waar PTEN een ander lipidesignaal, PIP3, afbreekt, dat cruciaal is voor het inschakelen van AKT en mTOR. Kortom: teveel SPIB en PIK3C3 leidt tot teveel PI3P, wat PTEN aantrekt om PIP3 te vernietigen, waardoor de AKT–mTOR‑stroomlijn doorgesneden wordt en het metabolisme en de groei van B-cellen verlamd raken.
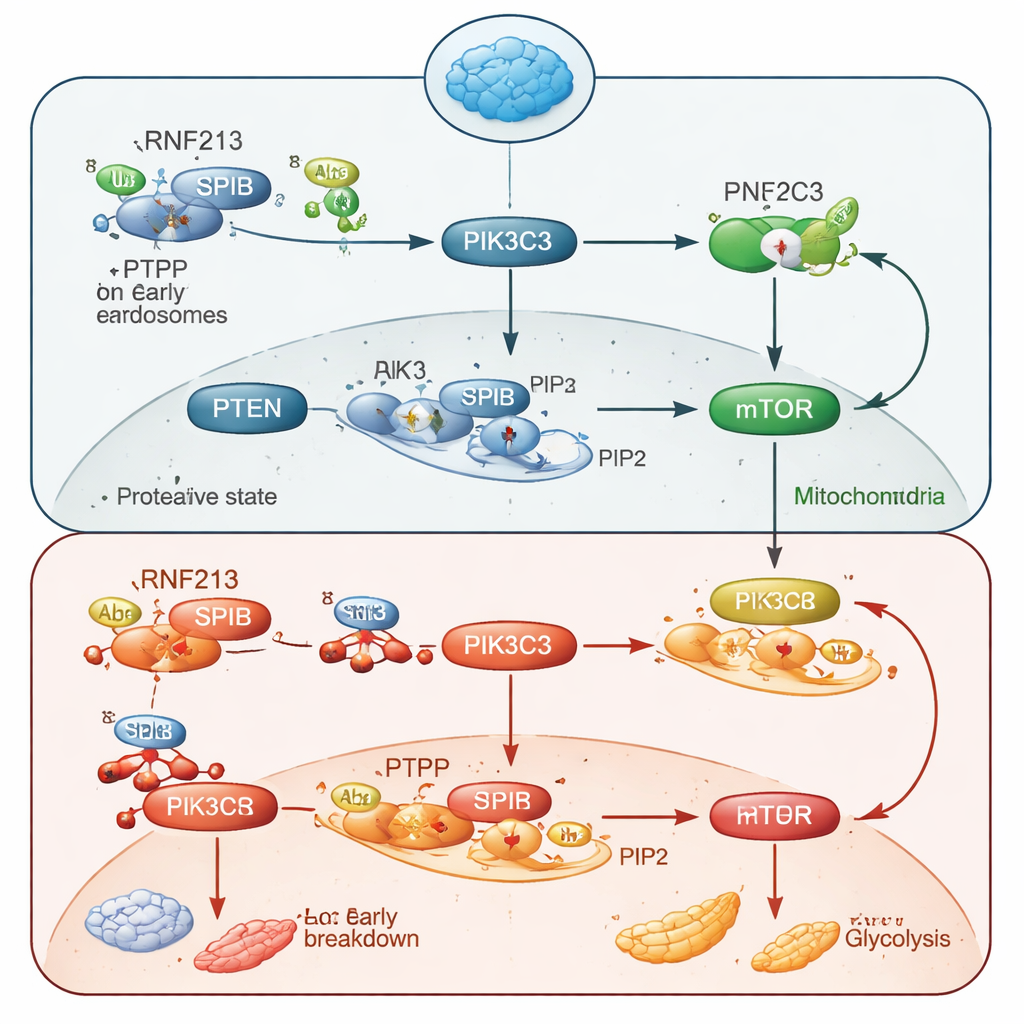
Het circuit herstellen en antilichaamreacties terugbrengen
De onderzoekers vroegen zich vervolgens af of het corrigeren van deze kettingreactie de B-celfunctie kon herstellen. Toen ze SPIB genetisch verwijderden in muizen zonder RNF213, of PIK3C3 blokkeerden met een middel genaamd SAR405, herwonnen B-cellen sterkere AKT–mTOR‑signalering, gezondere mitochondriën en een meer normaal metabolisch profiel. Deze ingrepen repareerden ook veel van de ontwikkelingsdefecten in milt-B-celsubsets. Functioneel gaven RNF213‑deficiënte muizen zwakkere antilichaamreacties tegen zowel T‑onafhankelijke antigenen (die grotendeels leunen op snelle marginale zone-B-celactie) als T‑afhankelijke antigenen (die kiemcentra en geheugen-B-cellen vereisen). De hoeveelheid en kwaliteit van antilichamen—vooral hoog‑affiniteits IgG1—waren aangetast, wat het belang van RNF213 voor effectieve humorale immuniteit benadrukt.
Waarom dit belangrijk is voor gezondheid en ziekte
Voor niet‑specialisten toont dit werk aan hoe één interferon‑induceerbaar eiwit, RNF213, vroege immuunalarmsignalen kan koppelen aan de diepe interne werking van B-cellen: hun genprogramma’s, brandstoftoevoer en vermogen om beschermende antilichamen te maken. Door de degradatie van SPIB te regelen en de PIK3C3–PI3P–PTEN‑rem op AKT–mTOR‑signalering te temperen, helpt RNF213 B-cellen zich correct te ontwikkelen en krachtig op infecties te reageren. Omdat RNF213 ook een belangrijke genetische risicofactor is voor moyamoya‑ziekte, suggereren deze bevindingen dat verstoringen in hetzelfde pad vaatafwijkingen zouden kunnen verbinden met subtiele immuun- en metabole onbalansen.
Bronvermelding: Zhang, Z., Xiang, N., Liu, Q. et al. Ring finger protein 213 regulates B-cell receptor signaling, metabolism, and development in B lymphocytes. Sig Transduct Target Ther 11, 59 (2026). https://doi.org/10.1038/s41392-026-02575-x
Trefwoorden: B-cellen, RNF213, antilichaamreacties, immuunmetabolisme, AKT-mTOR‑signalering