Clear Sky Science · nl
Exogene Epstein–Barr-virus nucleair antigeen 1 veroorzaakt door ADAR1 aangedreven tumorresistentie tegen immunotherapie
Waarom een veelvoorkomend virus ertoe doet voor kankerbehandeling
Veel vormen van kanker worden tegenwoordig behandeld met immunotherapieën die het eigen immuunsysteem van het lichaam ontketenen. Toch profiteert het merendeel van de patiënten nog steeds niet, omdat hun tumoren leren zich te verbergen voor immuunaanvallen. Deze studie onthult hoe een zeer veelvoorkomend virus, het Epstein–Barr-virus (EBV), tumoren helpt immuunafweer uit te schakelen en resistent te worden tegen deze sterke medicijnen — en hoe een nieuw type ontworpen molecuul die afweer mogelijk weer kan inschakelen.
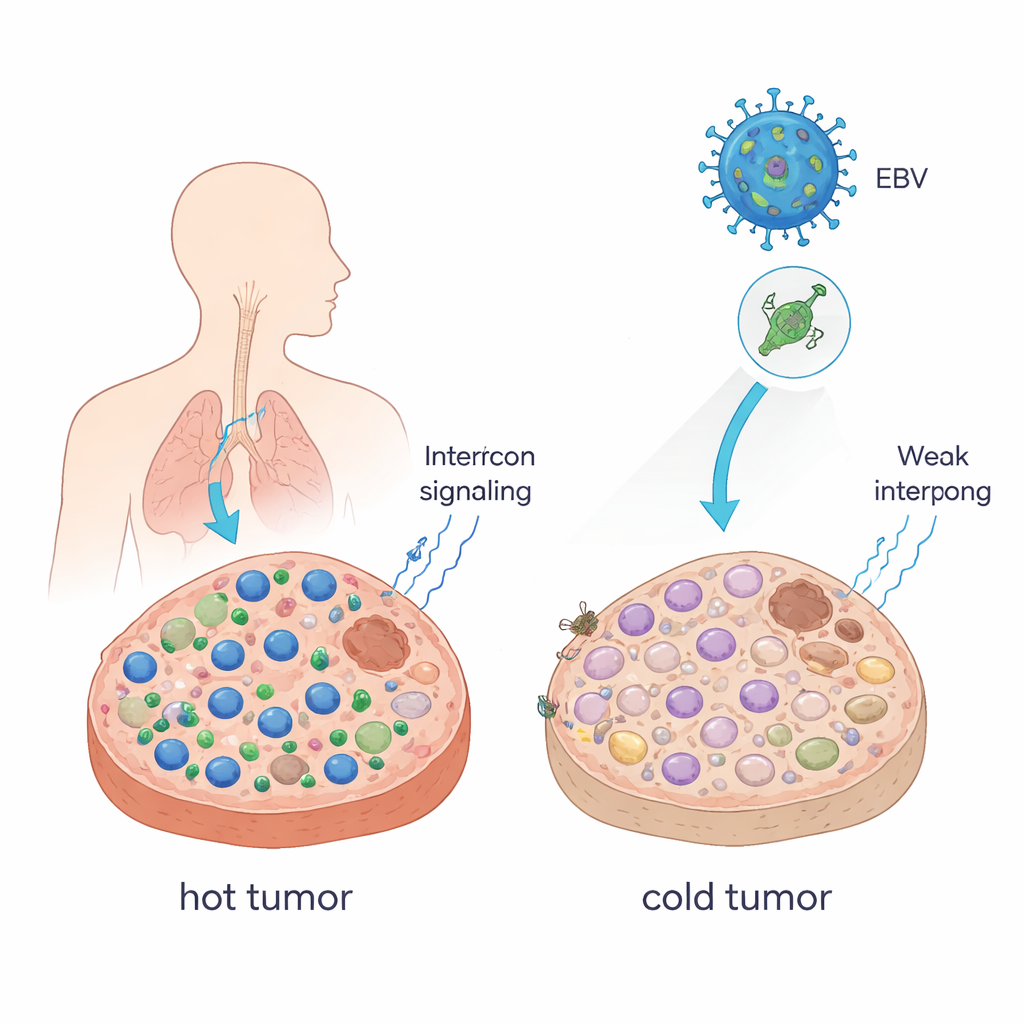
Van warme tumoren naar koude tumoren
Artsen beschrijven tumoren vaak als “warm” wanneer ze vol zitten met kankerdodende T-cellen, en als “koud” wanneer die cellen schaars zijn. Warme tumoren reageren meestal goed op remmers van immuuncheckpoints (ICB) zoals anti–PD-1-antistoffen; koude tumoren vaak niet. De auteurs tonen aan dat een enkel EBV-eiwit, EBNA1, tumoren in de richting van deze koudere, meer ontwijkende staat kan duwen. Wanneer zij muizentumorcellen dwongen EBNA1 te produceren en die in muizen met een intact immuunsysteem lieten groeien, werden de tumoren groter, bevatten ze minder CD8+ T-cellen en natural killer-cellen, en hadden ze meer immuunsuppressieve macrofagen. Signalen genaamd interferonen — belangrijke boodschappers die immuuncellen bijeenroepen — waren ook sterk verminderd. In patiëntmonsters van nasofaryngeaal carcinoom, een kanker die sterk met EBV is geassocieerd, lieten tumoren die EBNA1 uitdrukten eveneens minder CD8+ T-cellen zien dan normaal weefsel.
Een viraal kortere weg naar het RNA-regelmechanisme van de cel
Om te begrijpen hoe EBNA1 de tumoromgeving herstructureert, zochten de onderzoekers naar menselijke eiwitten die fysiek met het virus-eiwit interacteren. Ze concentreerden zich op een eiwit genaamd IGF2BP3, dat kleine chemische tekens (m6A) op boodschapper-RNA leest en de stabiliteit daarvan of de vertaling naar eiwit kan versterken. EBNA1 bond sterk aan IGF2BP3 in meerdere celtypen, inclusief EBV-positieve kankercellen. Gegevens uit patiëntentumoren toonden dat hoge IGF2BP3-niveaus samen gingen met zwakke interferon-gerelateerde genactiviteit en lagere infiltratie van CD8+ T-cellen, wat suggereert dat deze virus–gastheeralliantie de anti-tumorimmuniteit kan dempen.
Het versterken van een RNA-editor die waarschuwingssignalen stillegt
Diepergaande analyse benadrukte één belangrijk doelwit van deze interactie: ADAR1, een enzym dat dubbelstrengs RNA bewerkt door bepaalde “A”-letters in “I” te veranderen. Deze bewerking kan viraalachtig RNA in cellen minder gevaarlijk laten lijken voor interne sensoren, waardoor interferonreacties afnemen. De auteurs vonden dat EBNA1, IGF2BP3 en een translatiefactor genaamd EIF4G1 een drieledig complex vormen op ADAR1-mRNA. Dit complex verhoogt m6A-markering, rekruteert het translatiemechanisme en verhoogt selectief de ADAR1-eiwitproductie zonder de RNA-niveaus te verhogen. Daardoor voeren tumorcellen meer RNA-bewerking uit in herhaalde genetische elementen nabij interferon-gerelateerde genen. Deze bewerkingen verkleinen de voorraad ongelokaliseerd dubbelstrengs RNA die normaal gesproken sensoren zoals MDA5 en PKR zou alarmeren, waardoor interferonproductie wordt onderdrukt en tumoren zich beter kunnen verbergen voor immuunaanvallen.
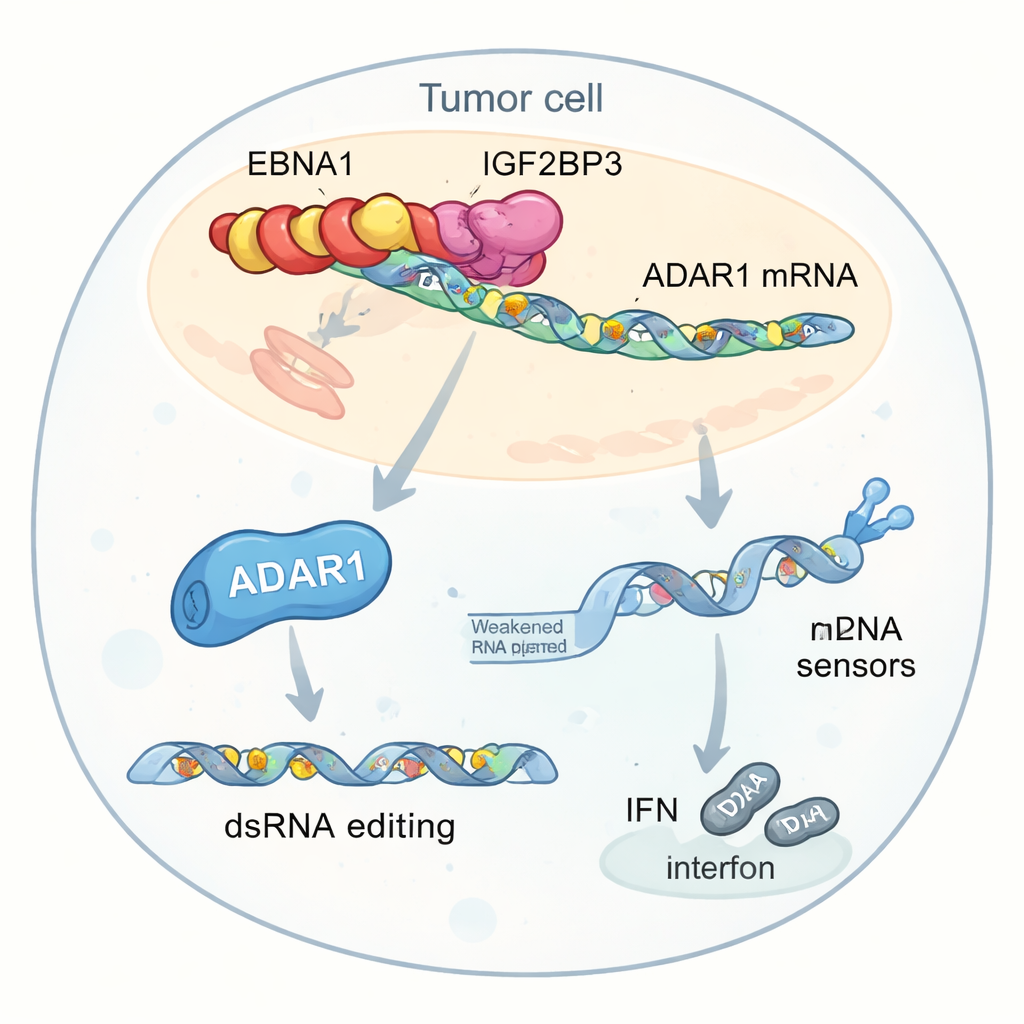
Minder interferon, zwakkere immunotherapie
Wanneer tumorcellen die EBNA1 uitdrukken in het laboratorium werden blootgesteld aan T-cellen en anti–PD-1-antistoffen, waren ze moeilijker te doden dan controlecellen en gaven ze minder interferon af. Zelfs wanneer ze direct met interferon werden behandeld, waren EBNA1-bevattende cellen minder gevoelig en waren hun interne RNA-sensoren minder sterk geactiveerd. Het verlagen van ADAR1-niveaus keerde deze effecten gedeeltelijk om, herstelde sensoractiviteit en interferonsignalering. Genetische en sequencing-experimenten bevestigden dat EBNA1-uitdrukkende cellen meer A-naar-I-bewerkingsgebeurtenissen vertoonden in specifieke RNA-regio’s, vooral na interferonstimulatie, wat het idee ondersteunt dat het virale versterken van ADAR1 helpt waarschuwingssignalen te neutraliseren die anders sterke immuunreacties zouden opwekken.
Een ontworpen degrader die de immuunaanval heractiveert
Het team vroeg zich vervolgens af of het verwijderen van EBNA1 uit tumoren hun kwetsbaarheid voor immunotherapie zou kunnen herstellen. Ze ontwierpen een PROTAC-molecuul, EP-1215, dat EBNA1 tagt voor afbraak door het eigen opruimsysteem van de cel. Bij lage doses degradeerde EP-1215 EBNA1 efficiënt en verlaagde het ADAR1-eiwitniveaus. In muisexperimenten had EP-1215 alleen een beperkt effect op EBNA1-positieve tumoren, en anti–PD-1 alleen was eveneens zwak. Maar in combinatie krompen de twee behandelingen de tumoren scherp, nam de infiltratie van CD8+ T-cellen toe en steeg het aantal interferon-producerende T-cellen. In gehumaniseerde muismodellen met menselijke immuuncellen en EBV-gerelateerde tumoren presteerde de combinatie opnieuw beter dan afzonderlijke behandelingen, zonder duidelijke lever- of niertoxische effecten.
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat een veelvoorkomend virus stilletjes kankercellen kan herbedraden om interne alarmsystemen te dempen, waardoor chemische signalen worden uitgeschakeld die anders immuuncellen zouden aantrekken en activeren. EBNA1 doet dit door een gastheer-RNA-lezer (IGF2BP3) en een translatiefactor (EIF4G1) te kapen om de RNA-editor ADAR1 te overproduceren, die de RNA-structuren wegbewerkt waar immuunsensoren juist op zijn gebouwd. Door EBNA1 te degraderen met een op maat gemaakte PROTAC zoals EP-1215, konden de auteurs deze waarschuwingssignalen herstellen en resistent geworden tumoren opnieuw gevoelig maken voor bestaande checkpointmiddelen. Als vergelijkbare strategieën veilig en effectief blijken bij mensen, zou het richten op virale helpers zoals EBNA1 een nieuwe manier kunnen bieden om koude, EBV-gekoppelde tumoren om te zetten in warme doelwitten waarop moderne immunotherapieën eindelijk effect hebben.
Bronvermelding: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Trefwoorden: Epstein-Barr-virus, resistentie tegen immunotherapie, ADAR1, RNA-bewerking, nasofaryngeaal carcinoom