Clear Sky Science · nl
Moleculair mechanisme van cholesterolafhankelijke membraanfusie bij SARS-CoV-2-infectie
Waarom cholesterol belangrijk is voor een luchtweginfectie
Het virus dat COVID-19 veroorzaakt, SARS-CoV-2, dringt onze cellen binnen door zijn buitenmantel te laten versmelten met onze celmembranen. Dit artikel stelt een schijnbaar eenvoudige vraag met grote gevolgen: in hoeverre bepaalt cholesterol — een vetachtige stof die bekender is uit hart- en vaatziekten — die fusiefase? De auteurs laten zien dat cholesterol in het virale membraan niet alleen de efficiëntie van infectie lichtweg beïnvloedt; het helpt daadwerkelijk de spike-eiwitten van het virus te organiseren in krachtige aanmeerplatforms die binnendringing gemakkelijker en betrouwbaarder maken.
Een minimaal model van virale binnendringing opbouwen
Om dit proces te ontleden, bouwden de onderzoekers de ontmoeting tussen virus en cel na in een reageerbuis met behulp van kleine vetbelletjes genaamd liposomen. De ene set liposomen droeg het SARS-CoV-2-spike-eiwit en fungeerde als het virale membraan; de andere droeg de ACE2-receptor en bootste het gastheercelmembraan na. Wanneer ze werden gemengd en geactiveerd door specifieke enzymen die de spike “doorsnijden” naar zijn fusieklare vorm, fuseerden deze kunstmatige membranen zodat een fluorescerende kleurstof van het ene belletje naar het andere kon overgaan. Dit teruggebrachte systeem stelde het team in staat de lipidesamenstelling — inclusief cholesterolsamenstelling — aan elke kant nauwkeurig aan te passen en stap voor stap te volgen hoe fusie verliep. 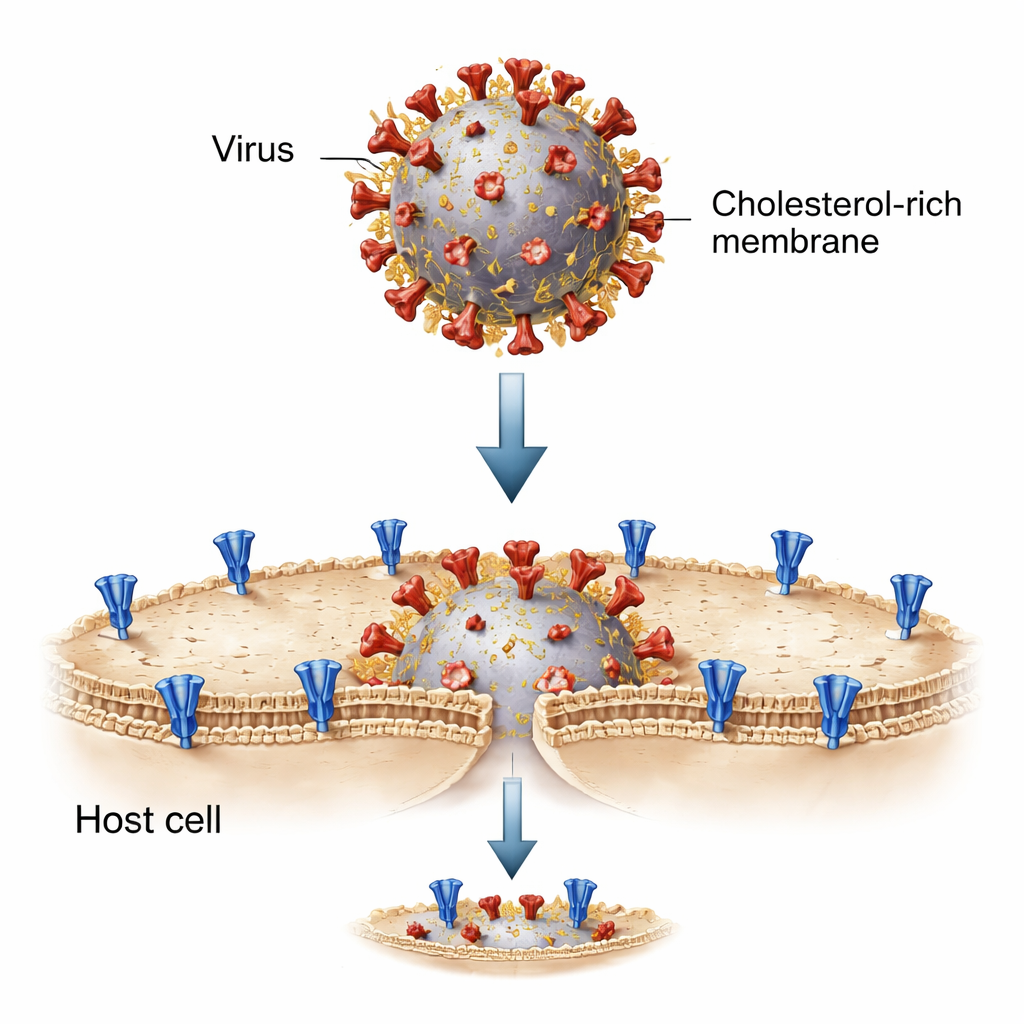
Cholesterol stimuleert aanmeeren meer dan fusie zelf
Door cholesterol op en neer te draaien, ontdekten de onderzoekers dat toevoeging van cholesterol aan het spike-bevattende membraan fusie vaker liet voorkomen, maar niet op de manier die je misschien zou verwachten. Hoge cholesterol veranderde niet ingrijpend de kans dat twee reeds aangehechte membranen daadwerkelijk zouden samensmelten. In plaats daarvan verhoogde het sterk hoe vaak vesikels met spike eerst aan vesikels met ACE2 aanmeerden. Enkel-deeltje beeldvorming toonde veel meer succesvolle aanmeer-evenementen wanneer spike in cholesterolrijke membranen zat, terwijl de waarschijnlijkheid dat een aangemeerd paar volledig zou fuseren ongeveer constant bleef. Interessant genoeg leverde het laden van cholesterol aan de ACE2-kant weinig voordeel en bij zeer hoge niveaus zelfs een remming van fusie, wat wijst op viraal — en niet gastheer — cholesterol als de belangrijkste drijvende kracht.
Van modelmembraan naar levende cellen
Vervolgens vroegen de onderzoekers of hetzelfde patroon in levende cellen gold. Ze manipuleerden menselijke cellen zodat ze óf spike óf ACE2 uitdrukten en zagen dat deze grote gefuseerde structuren, of syncytia, vormden wanneer ze werden gemengd. Verwijderen van cholesterol uit spike-exprimerende cellen maakte bijna een einde aan de vorming van syncytia, terwijl het herstel van cholesterol de fusie herstelde. In parallelle experimenten met SARS-CoV-2 “pseudovirussen” (ongevaarlijke deeltjes die de coronavirus-spike gebruiken om cellen binnen te dringen) verminderde het strippen van cholesterol uit het virale membraan de infectie sterk, en het terugplaatsen ervan versterkte de infectie op een dosisafhankelijke manier. Daarentegen gaf het wijzigen van cholesterol alleen aan ACE2-exprimerende cellen weinig verandering. Over alle tests was de boodschap consistent: cholesterol in het spike-bevattende membraan is essentieel voor efficiënte binnendringing.
Spike-clusters: cholesterols geheime wapen
Waarom zou cholesterol aan de virale zijde zoveel uitmaken? Hoge-resolutie beeldvorming van celmembranen liet zien dat spike-eiwitten de neiging hebben dichte clusters te vormen wanneer cholesterol overvloedig aanwezig is, maar meer verspreid blijven wanneer het ontbreekt. Single-molecule metingen gingen verder en toonden aan dat deze clusters meer kopieën van spike bevatten onder cholesterolrijke omstandigheden. De auteurs herleidden dit effect naar een cysteïnerijk gebied (CRR) aan het staartuiteinde van spike, binnenin het virale membraan. Dit segment wordt gemodificeerd door palmitoylering — een type vetachtige “anker” dat de voorkeur geeft aan cholesterolrijke microdomeinen. Wanneer het team de staart van spike inkortte of alle tien cysteïnen muteerde om palmitoylering te blokkeren, clusterde spike niet langer met cholesterol en verdween de cholesterolgestuurde versterking van aanmeeren en fusie. 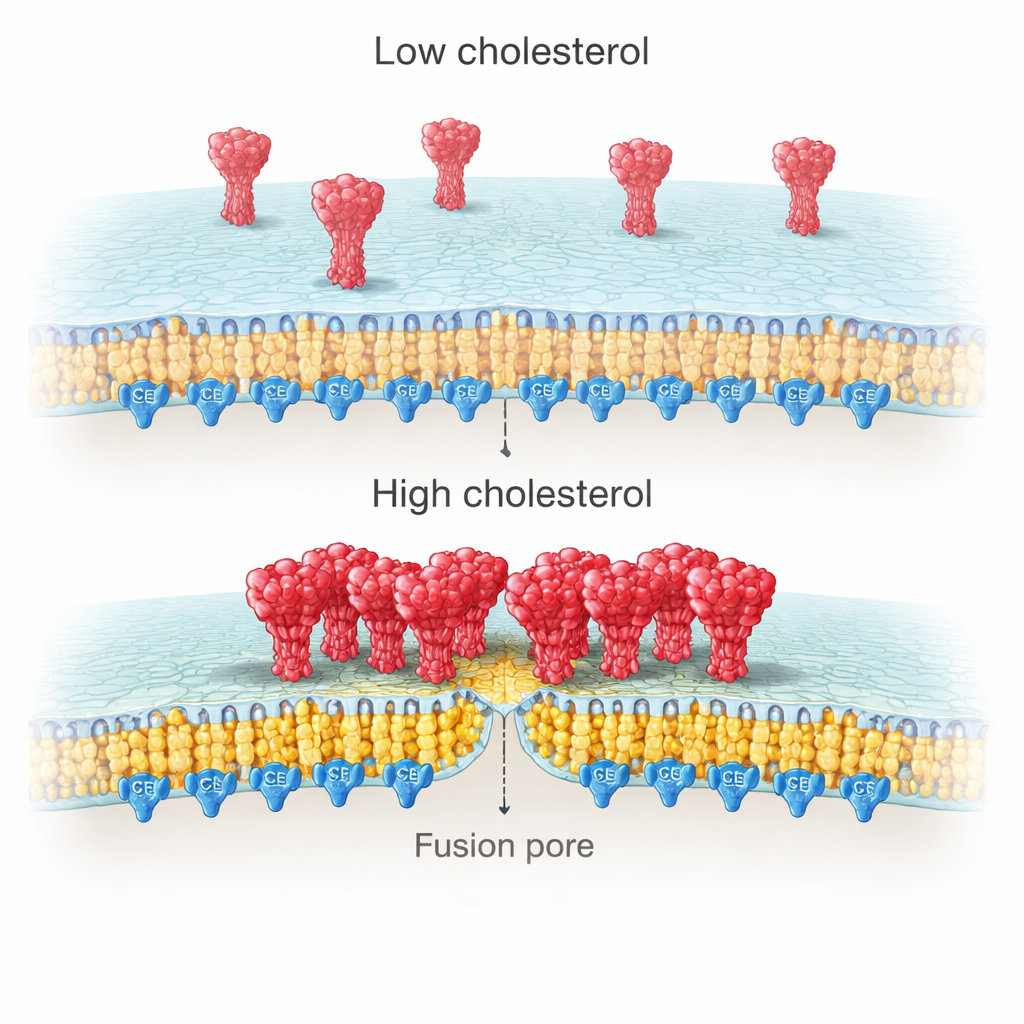
Hoe dit toekomstige behandelingen kan helpen
In eenvoudige bewoordingen concludeert de studie dat cholesterol het virale membraan omzet in een fusieplatform door veel spike-eiwitten via hun gepalmitoylleerde staartregio in strakke clusters te verzamelen. Deze clusters ameren efficiënter aan ACE2 op gastheercellen, waardoor de kans toeneemt dat een gegeven ontmoeting leidt tot succesvolle fusie en infectie. Voor niet-specialisten is de belangrijkste les dat cholesterol niet slechts een passief bestanddeel van de virale mantel is; het is een actieve organisator van het spike-machinery. Dit maakt de cysteïnerijke, cholesterolgevoelige staart van spike — en de enzymen die deze palmitoyleren — veelbelovende doelen voor brede antivirale strategieën die werkzaam zouden kunnen zijn tegen verschillende coronavariants.
Bronvermelding: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Trefwoorden: cholesterol, SARS-CoV-2 spike, membraanfusie, virale binnendringing, palmitoylering