Clear Sky Science · nl
PKC-eta bevordert uitzaaiing van borstkanker door regulatie van de Hippo–YAP-signaleringsroute
Waarom dit onderzoek ertoe doet
Triple-negatieve borstkanker (TNBC) is een van de gevaarlijkste vormen van borstkanker omdat ze vroeg uitzaait en weinig gerichte behandelingen heeft. Deze studie onthult hoe een specifiek enzym binnen kankercellen, PKC-eta (PKCη), fungeert als een soort hoofdschakelaar die tumoren helpt los te komen, door het lichaam te reizen en nieuwe tumoren te vormen. Door deze schakelaar te begrijpen, identificeren de onderzoekers ook een klein natuurlijk peptide dat hem kan uitzetten, wat wijst op een potentiële nieuwe behandelaanpak voor deze agressieve ziekte. 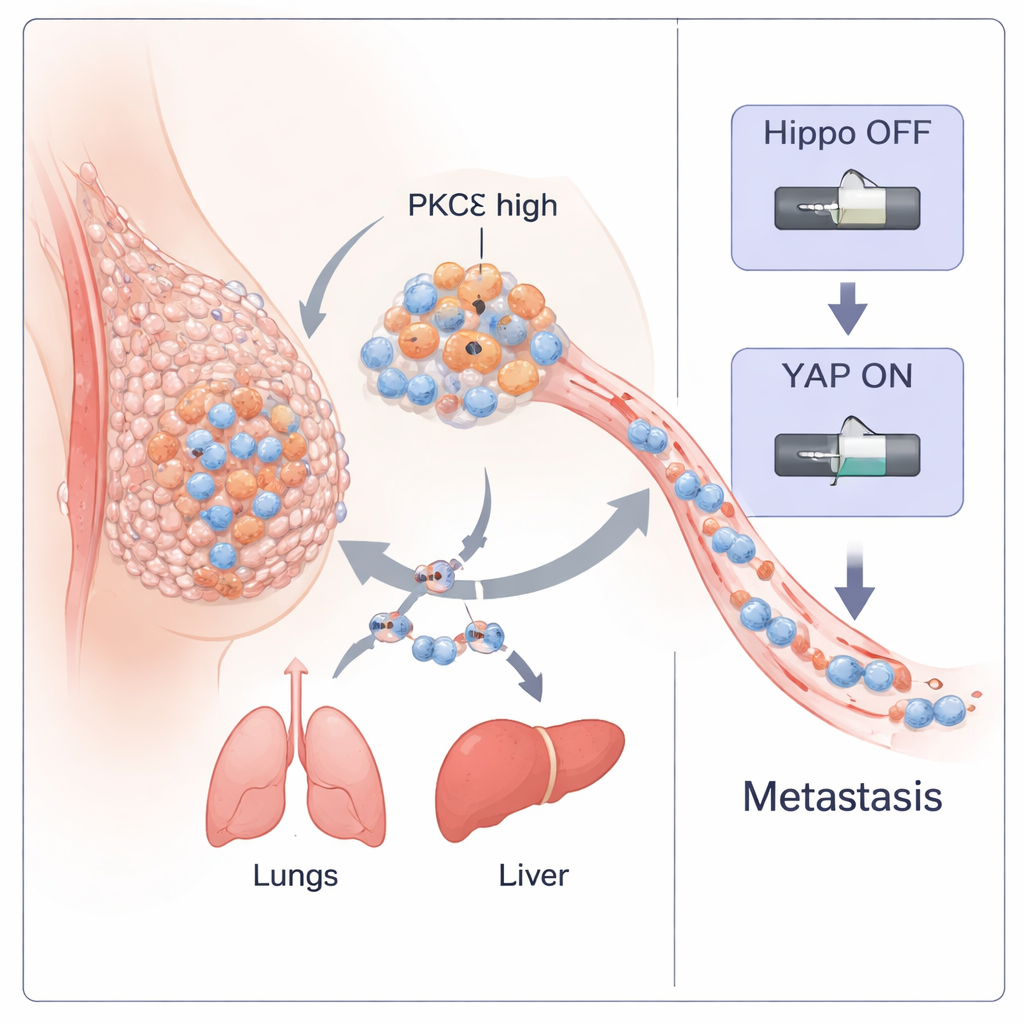
Een verborgen aandrijver in agressieve borsttumoren
Het team begon met het analyseren van grote verzamelingen gegevens van borstkankerpatiënten. Ze ontdekten dat het gen dat PKCη codeert (PRKCH) bijzonder sterk tot expressie komt in een subtype tumoren dat bekendstaat als “claudin-low”, dat sterk overlapt met TNBC en rijk is aan stamcelachtige, zeer mobiele cellen. In meerdere patiëntengroepen vertoonden tumoren met hoge PRKCH-signaturen duidelijke kenmerken van epitheliale–mesenchymale transitie (EMT)—een proces waarbij ooit geordende cellen hun hechting verzwakken, van vorm veranderen en invasiever worden. PRKCH-niveaus waren ook hoger in metastatische monsters dan in de oorspronkelijke primaire tumoren, en eiwitkleuring van menselijke TNBC-weefsels toonde meer actieve, perinucleaire PKCη in hogergradige, gevorderde kankers. Gezamenlijk wezen deze bevindingen erop dat PKCη nauw verbonden is met tumoragressiviteit en verspreiding.
Van petrischaal naar muis: aantonen dat PKCη de verspreiding aanwakkert
Om oorzaak en gevolg te testen, gebruikten de onderzoekers CRISPR-genbewerking om PKCη te verwijderen uit twee sterk metastatische TNBC-cellijnen, één muis (4T1) en één menselijk (MDA-MB-231). Zonder PKCη verschoof het cellulaire fenotype naar een meer “epitheliale” staat: ze verhoogden hechtingseiwitten zoals E-cadherine en EpCAM en verminderden klassieke mesenchymale markers waaronder vimentine en N-cadherine. Deze PKCη-deficiënte cellen vormden minder en kleinere kolonies, migreerden en invadeerden minder efficiënt, waren gevoeliger voor celdood bij loslating en vertoonden een sterke afname van kanker-stamcelkenmerken, waaronder minder CD44high/CD24low en ALDH-positieve cellen en een verminderde bolvormende capaciteit. Wanneer deze cellen in muizen werden geïnjecteerd, gaven cellen zonder PKCη kleinere primaire tumoren en veel minder metastasen naar longen, lever, hersenen en andere organen; de muizen leefden ook langer. Het herstellen van PKCη keerde deze veranderingen om, wat bevestigt dat het enzym actief de progressie en verspreiding van TNBC bevordert.
Hoe PKCη een groeireguleringsroute kapert
De studie zoomde vervolgens in op hoe PKCη deze prometastatische werking uitoefent. Patiëntgegevens toonden aan dat PKCη-niveaus parallel lopen met YAP, een krachtig genregulerend eiwit dat wordt gecontroleerd door de Hippo-route—een cellulaire “veiligheidsrem” die normaal groei afremt. Hoge niveaus van PRKCH of YAP1 voorspelden slechtere patiëntuitkomsten, en hoge niveaus van beide samen waren gekoppeld aan bijzonder slechte overleving zonder verre metastasen. In TNBC-cellen verlaagde het verwijderen van PKCη de totale YAP-niveaus en verschoof YAP van de kern naar het cytoplasma, waar het inactief is. Biochemische experimenten lieten zien dat PKCη fysiek aan YAP bindt en specifiek een fosfaatgroep toevoegt op de Ser128-plek. Deze wijziging stabiliseert YAP en helpt het de kern binnen te komen om genen aan te zetten die EMT, stamcelkenmerken en metastase stimuleren. Wanneer PKCη afwezig is, wordt YAP in plaats daarvan gefosforyleerd op andere plaatsen (Ser127 en Ser397) die ervoor zorgen dat het bindt aan 14-3-3-eiwitten, gevangen blijft in het cytoplasma en uiteindelijk wordt afgebroken. PKCη versterkt ook PTEN—een natuurlijke rem op het AKT-enzym—waardoor AKT-activiteit laag blijft en de upstream Hippo-kinasen die anders YAP zouden inactiveren, worden onderdrukt. Op deze manier activeert PKCη YAP zowel direct als indirect door de Hippo-“rem” uit te schakelen. 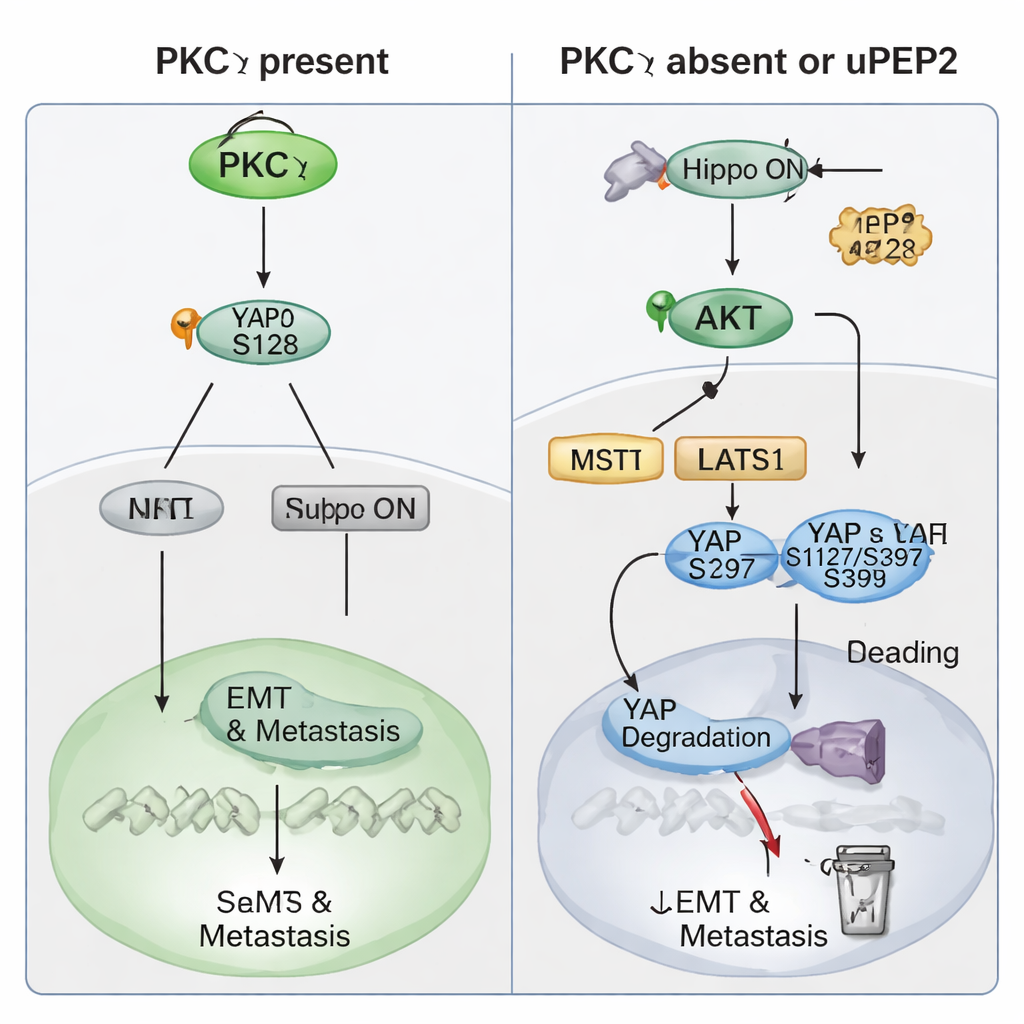
Een klein peptide dat de kankerschakelaar ontwapent
Interessant genoeg bevat het PKCη-gen een korte upstream open reading frame (uORF) dat een micropeptide codeert, genaamd uPEP2. Eerder werk toonde aan dat uPEP2 kan binden aan en PKCη en verwante enzymen kan remmen. Hier bootste behandeling van TNBC-cellen met synthetisch uPEP2 de effecten van PKCη-knockout na: migratie, invasie en stamcelachtig gedrag namen allemaal af, EMT-markers verschoof naar een minder agressief profiel, en YAP-niveaus daalden terwijl diens “off”-fosforylatie tekens toenamen. In muistumoren verminderde uPEP2 PKCη en YAP in primaire tumoren, verhoogde het YAP-inactivatie en ging dit gepaard met minder micrometastasen in lever en longen. Mechanistisch bevordert uPEP2 de afbraak van PKCη, schakelt de Hippo-route weer in en duwt YAP richting cytoplasmatische retentie en afbraak.
Wat dit betekent voor toekomstige behandelingen
Voor de niet-specialistische lezer is de kernboodschap dat de onderzoekers PKCη hebben geïdentificeerd als een spil die de meest agressieve vormen van borstkanker helpt los te komen, bewegen en koloniseren van verre organen door een natuurlijk groeicontrolesysteem uit te schakelen en de YAP-“gaspedaal” te activeren. Door PKCη uit te schakelen of het kleine natuurlijke peptide uPEP2 te gebruiken om het af te breken, konden zij de Hippo-veiligheidsrem herstellen, YAP tot rust brengen en de metastasering in preklinische modellen sterk verminderen. Hoewel dit werk nog experimenteel is en is uitgevoerd in cellijnen en immuundeficiënte muizen, benadrukt het PKCη en zijn interactie met YAP als veelbelovende doelwitten voor nieuwe TNBC-therapieën en suggereert het dat uPEP2-achtige geneesmiddelen ooit kunnen helpen de verspreiding van deze moeilijk te behandelen kanker te voorkomen of te beperken.
Bronvermelding: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Trefwoorden: triple-negatieve borstkanker, PKC-eta, Hippo-YAP-route, epitheliale-mesenchymale transitie, kankeruitzaaiing