Clear Sky Science · nl
Ontdekking en ontwikkeling van antivirale middelen: uitdagingen en toekomstige richtingen
Waarom we nog steeds betere virusbestrijdende geneesmiddelen nodig hebben
De COVID-19-pandemie toonde hoe snel een nieuw virus het dagelijks leven kan ontwrichten — en hoezeer we nog steeds afhankelijk zijn van goede medicijnen wanneer vaccins niet voldoende zijn. Dit overzichtsartikel blikt terug op 60 jaar antivirale medicijnontwikkeling en vraagt: hoe kunnen we snellere, slimere en bredere verdedigingslinies opbouwen tegen toekomstige virale bedreigingen? Het legt op toegankelijke wijze uit hoe onderzoekers antivirale middelen ontdekken, ontwerpen en afleveren, wat ze van COVID-19 hebben geleerd en hoe technieken zoals kunstmatige intelligentie en nanotechnologie het speelveld kunnen veranderen.
Van de eerste antivirale middelen tot het huidige arsenaal
Antivirale geneeskunde is een relatief jong vakgebied. Het eerste goedgekeurde middel, idoxuridine in de jaren 1960, liet zien dat het aanpassen van de bouwstenen van DNA virale replicatie kon vertragen, maar het beschadigde ook gezonde cellen en kon daarom alleen op het oog worden gebruikt. Later kwam aciclovir, een baanbrekend middel tegen herpes dat voornamelijk in geïnfecteerde cellen wordt geactiveerd, waardoor het zowel krachtig als veilig is. In de jaren 1980 werd zidovudine het eerste behandelingsmiddel tegen hiv, wat de deur opende naar moderne combinatietherapieën die hiv nu tot een beheersbare chronische aandoening maken. In de loop van de decennia hebben betere chemie en computerondersteund ontwerp meer precieze middelen opgeleverd tegen influenza, hepatitis B en C, hiv en recentelijk SARS‑CoV‑2. Het overzicht schetst deze tijdlijn en laat zien hoe elk doorbraak een nieuwe manier introduceerde om virussen te slim af te zijn.
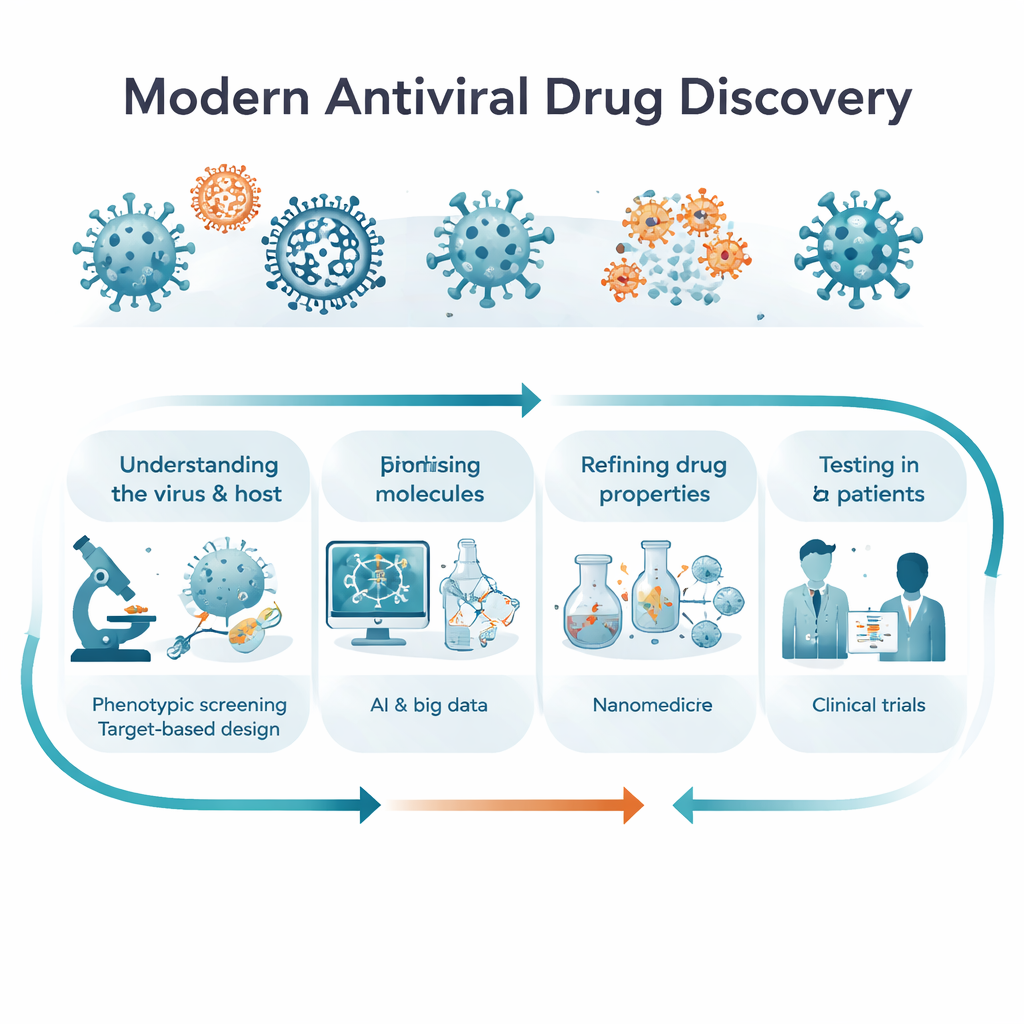
Twee manieren om een goed middel te vinden: cellen observeren versus op targets mikken
Onderzoekers volgen over het algemeen twee aanvullende paden naar nieuwe antivirale middelen. Bij “fenotypische” ontdekking beginnen ze niet met een specifiek eiwit; in plaats daarvan brengen ze geïnfecteerde cellen of modelorganismen in contact met duizenden moleculen en vragen simpelweg: welke houden het virus onder controle en houden de cellen in leven? Dit kan verrassende, first‑in‑class middelen blootleggen, inclusief middelen die op meer dan één pad werken. Bij “target-gebaseerde” ontdekking identificeren wetenschappers eerst een viraal of humaan eiwit dat cruciaal is voor infectie — zoals een polymerase, protease of immuunsignaal — en ontwerpen ze vervolgens moleculen om dat target te blokkeren of te moduleren. Het artikel legt uit hoe deze strategieën verschillen, waarom ze elk belangrijk zijn in verschillende stadia van onderzoek, en hoe toekomstige projecten ze waarschijnlijk zullen combineren, soepel bewegend van brede observatie naar precieze moleculaire inzichten.
De virus en zijn ondersteuningssysteem daar raken waar het pijn doet
Moderne antivirale middelen doen veel meer dan slechts één viraal enzym blokkeren. Het overzicht doorloopt de virale levenscyclus, van binnendringen in de cel tot kopiëren van het genoom en vrijlating, en licht de soorten middelen toe die bij elk stapje ingrijpen. Sommige verbindingen binden direct aan virale enzymen of structurele eiwitten. Andere werken door gastheerfactoren te richten waarop virussen afhankelijk zijn — zoals celoppervlaktereceptoren, belangrijke metabolische enzymen of aangeboren immuunroutes zoals interferonen en toll‑like receptoren. Door te handelen op gastheer‑“hulp”-eiwitten kunnen deze middelen de kans verkleinen dat een snel muterend virus ontsnapt. De auteurs beschrijven ook opkomende ideeën zoals kleine moleculen die membraneloze “druppels” in cellen verstoren waar virussen assembleren, of die viraal eiwit en RNA selectief afbreken in plaats van ze alleen te blokkeren.
Betere moleculen ontwerpen: vorm, eigenschappen en afleveringswijze
Een initiële “hit” omzetten in een bruikbaar medicijn betekent meer dan alleen potentie maximaliseren. Chemici passen de vorm en lading van moleculen aan zodat ze als sleutels in sloten in hun targets passen, vaak gestuurd door hoogresolutie-eiwitstructuren en simulaties. Ze verfijnen ook wateroplosbaarheid, stabiliteit en metabolisme zodat het middel het juiste weefsel bereikt, lang genoeg actief blijft en onnodige toxiciteit vermijdt. Het artikel geeft voorbeelden van hoe kleine veranderingen — zoals het toevoegen van een zijketen of het vormen van een zout — de werkzaamheid tegen resistent hiv of coronavirus kunnen verhogen en tegelijk de veiligheid kunnen verbeteren. Het bespreekt ook prodrugs, die onactieve of minder actieve vormen zijn die in het lichaam worden omgezet, en gerichte afgiftesystemen zoals leverzoekende suikertags en lipidenanodeeltjes die kwetsbaar mRNA of nucleïnezuurmiddelen veilig in cellen afleveren.
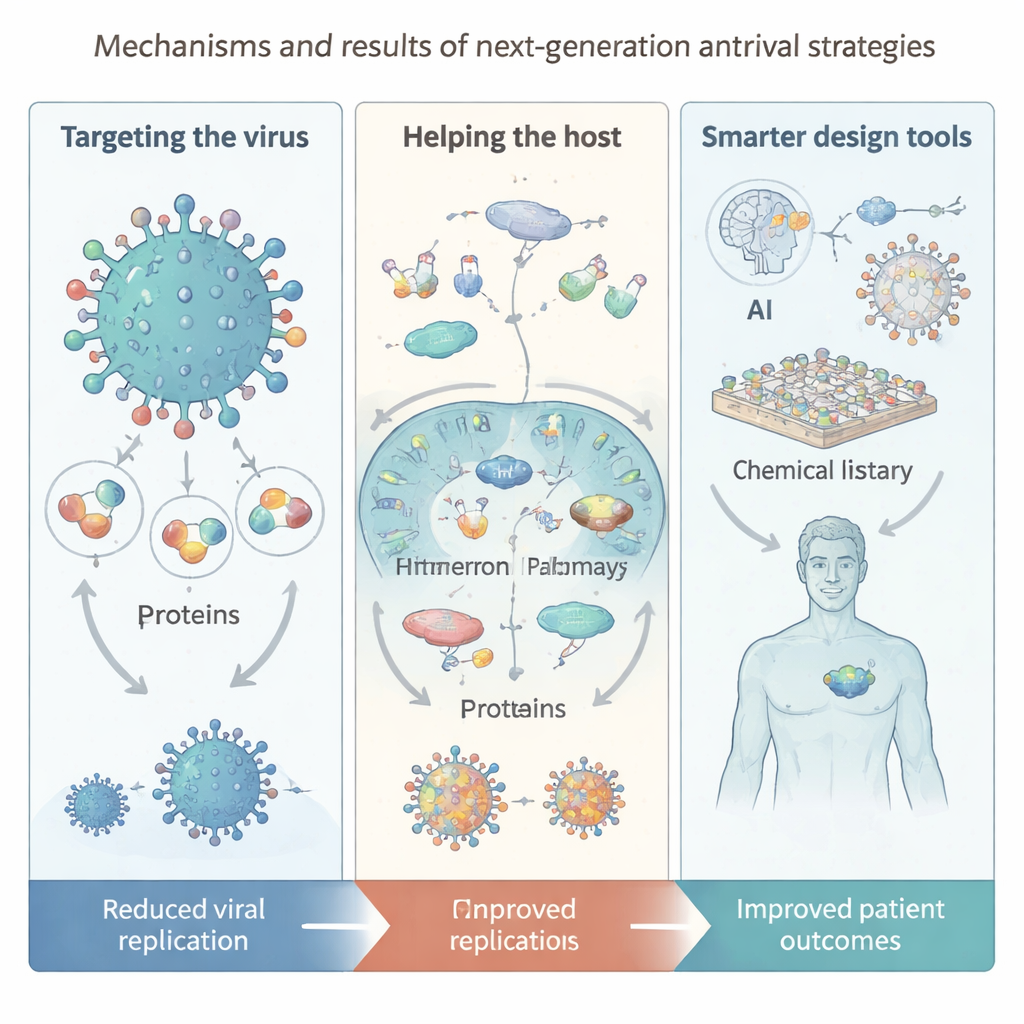
Nieuwe hulpmiddelen: kunstmatige intelligentie, enorme bibliotheken en nanotechnologie
Een belangrijk thema van het overzicht is hoe technologie de antivirale ontdekking hervormt. Kunstmatige intelligentie helpt nu eiwitstructuren te voorspellen, enorme “virtuele” bibliotheken met miljarden mogelijke moleculen te doorzoeken en nieuwe verbindingen of medicijncombinaties voor te stellen. DNA‑gecodeerde bibliotheken en macrocyclische peptideplatforms maken ultrarapide screening van enorme chemische ruimtes mogelijk, terwijl geautomatiseerde synthese‑ en zuiveringssystemen de bouw‑en‑testcyclus versnellen. Aan de afleveringskant biedt nanotechnologie virusachtige deeltjes, slimme polymeren en “nanozymen” die viraalkappen direct kunnen beschadigen of immuunreacties kunnen aanscherpen. Toch waarschuwen de auteurs dat AI‑modellen nog steeds afhankelijk zijn van hoogwaardige data, dat veel gegenereerde moleculen moeilijk te maken of te testen zijn, en dat kwesties rond veiligheid, eerlijkheid en privacy moeten worden aangepakt naarmate deze hulpmiddelen centraler worden.
Waarheen de ontdekkingsreis van antivirale middelen gaat
Voor de algemene lezer is de kernboodschap van het artikel zowel somber als hoopvol. Virussen muteren snel, en geen enkele pil zal voor altijd of tegen elke dreiging werken. Maar door te leren van COVID‑19, ons begrip van virus–gastheerinteracties te verdiepen en slimme chemie, geavanceerde biologie, AI en nanotechnologie te combineren, bouwen wetenschappers aan een wendbaarder antiviraal gereedschapkist. Toekomstige behandelingen zullen waarschijnlijk breder van toepassing zijn, beter verdragen worden en zijn afgestemd om niet alleen het virus te raken maar ook de kwetsbare “zwakke plekken” in het infectieproces. Voortdurende samenwerking tussen disciplines, industrieën en landen zal essentieel zijn om deze wetenschappelijke vooruitgang om te zetten in betaalbare, praktische geneesmiddelen vóór de volgende pandemie toeslaat.
Bronvermelding: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
Trefwoorden: ontdekking van antivirale middelen, COVID-19 therapeutica, gastheer-gerichte antivirale middelen, kunstmatige intelligentie in geneesmiddeldesign, nanotechnologie in de geneeskunde