Clear Sky Science · nl
Cytotoxische CD4+ T-cellen: oorsprong, biologische functies, ziekten en therapeutische doelen
Wanneer helpercellen moordenaars worden
Het immuunsysteem wordt vaak in eenvoudige rollen beschreven: sommige cellen signaleren problemen, andere voeren de daadwerkelijke strijd. Dit artikel richt zich op een verrassende groep die die grens vervaagt — cytotoxische CD4 T-cellen. Lange tijd bekend vooral als “helper”-cellen die de verdediging coördineren, kunnen bepaalde CD4 T-cellen zelf gewapende moordenaars worden. Begrijpen hoe deze vormveranderende cellen ontstaan, wat ze doen en hoe ze bijdragen aan ziekten zoals kanker, virusinfecties, auto-immuunstoornissen en hartziekten, kan nieuwe manieren openen om zowel de immuniteit te versterken als schadelijke ontsteking te temperen. 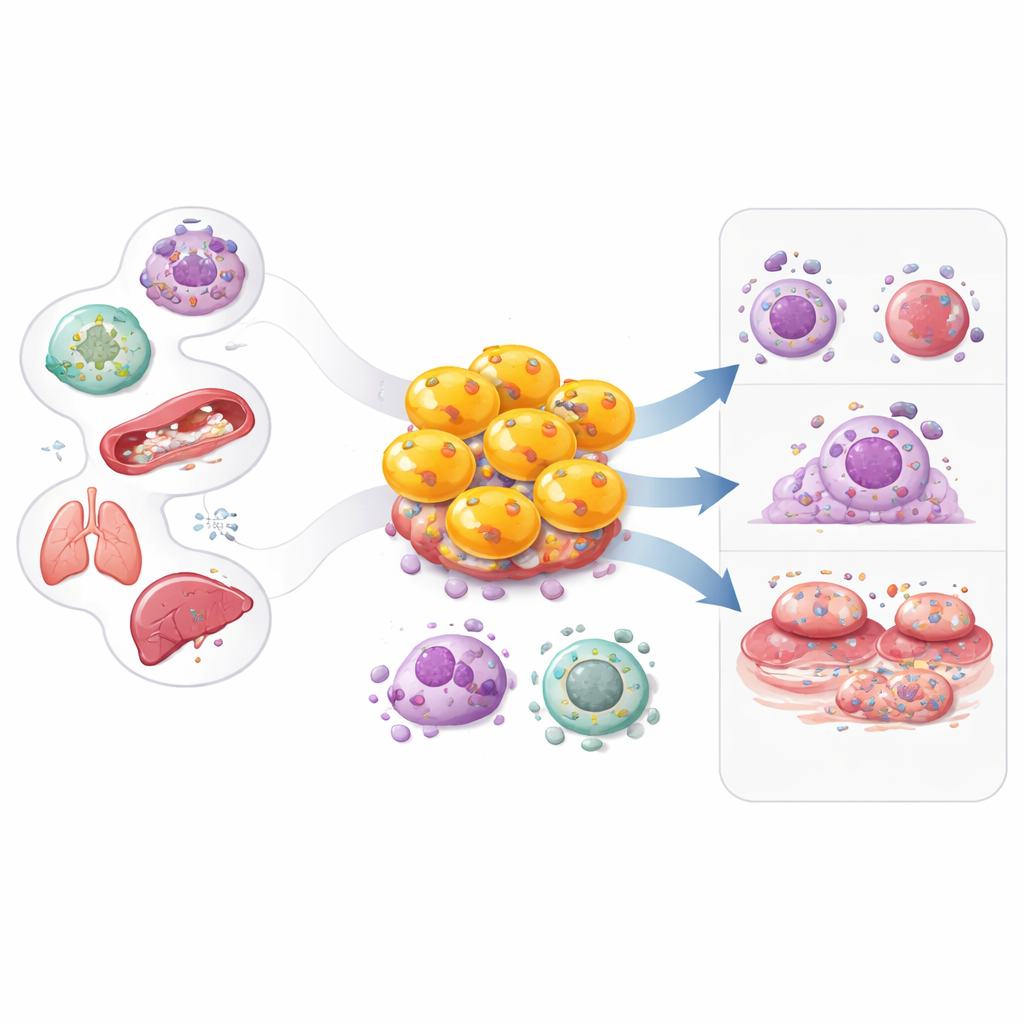
Hoe een flexibele verdediger ontstond
Vroeg werk eind jaren zeventig en in de jaren tachtig toonde aan dat een fractie van CD4 T-cellen direct andere cellen kon doden die de juiste immuursignalen vertoonden, veelal overeenkomstig met klassieke CD8 “killer”-cellen. Aanvankelijk verwierpen veel wetenschappers deze bevindingen als kweekartefacten. In de daaropvolgende decennia bevestigden diermodellen van influenza en studies bij mensen met reumatoïde artritis, hartziekten, chronische virusinfecties en kanker dat cytotoxische CD4 T-cellen echt en klinisch relevant zijn. Moderne technieken zoals flowcytometrie en single-cell RNA-sequencing hebben sindsdien hun diversiteit in kaart gebracht en laten zien dat deze cellen zich uitbreiden bij chronische infecties, tumoren, veroudering en verschillende inflammatoire aandoeningen, waar ze langdurig kunnen aanhouden.
Waar deze dodelijke helpers vandaan komen
De review legt uit dat cytotoxische CD4 T-cellen waarschijnlijk op twee hoofdmanieren ontstaan. Een idee is dat ze deels lijken op natural killer-cellen omdat ze veel van dezelfde oppervlakte-receptoren en cytotoxische moleculen delen, wat wijst op een verwant ontwikkelingspad. Opeenstapeling van bewijs ondersteunt echter een ander beeld: de meeste van deze cellen beginnen als gewone helper-CD4 T-cellen — vooral Th1-achtige cellen — die, onder chronische antigenblootstelling en sterke ontstekingssignalen, “omscholen” naar een terminal gedifferentieerde, cytotoxische staat. Deze verschuiving wordt gestuurd door een netwerk van externe cues (zoals interleukinen 2, 7 en 15) en interne schakelaars (waaronder Runx3, T-bet, Eomes, Blimp-1 en Hobit) die samen genen voor perforine, granzymen en doodsinducerende liganden aanzetten.
Hoe ze doden en ontsteking vormen
Functioneel opereren cytotoxische CD4 T-cellen via twee hoofdaanvalswegen. In de granulaire route vormen ze een nauwe verbinding met een doelcel en geven ze pakketjes vrij die perforine en granzymen bevatten, waarmee gaten worden geslagen en geprogrammeerde celdood van binnenuit wordt geïnduceerd. In de doods-ligandroute tonen ze moleculen zoals Fas-ligand en TRAIL op hun oppervlak, die bij bijpassende receptoren op doelcellen binden om een intern zelfmoordprogramma te starten. Naast directe doding scheiden deze cellen inflammatoire boodschappers uit zoals interferon-gamma, tumornecrosefactor en groeifactoren die andere immuuncellen rekruteren en activeren, bloedvaten hervormen en het lokale weefselgedrag veranderen. In tegenstelling tot klassieke helpers zijn ze vaak resistent tegen normale “remmen” zoals regulerende T-cellen en zijn ze minder vatbaar voor apoptose, waardoor ze zich in chronische aandoeningen kunnen ophopen. 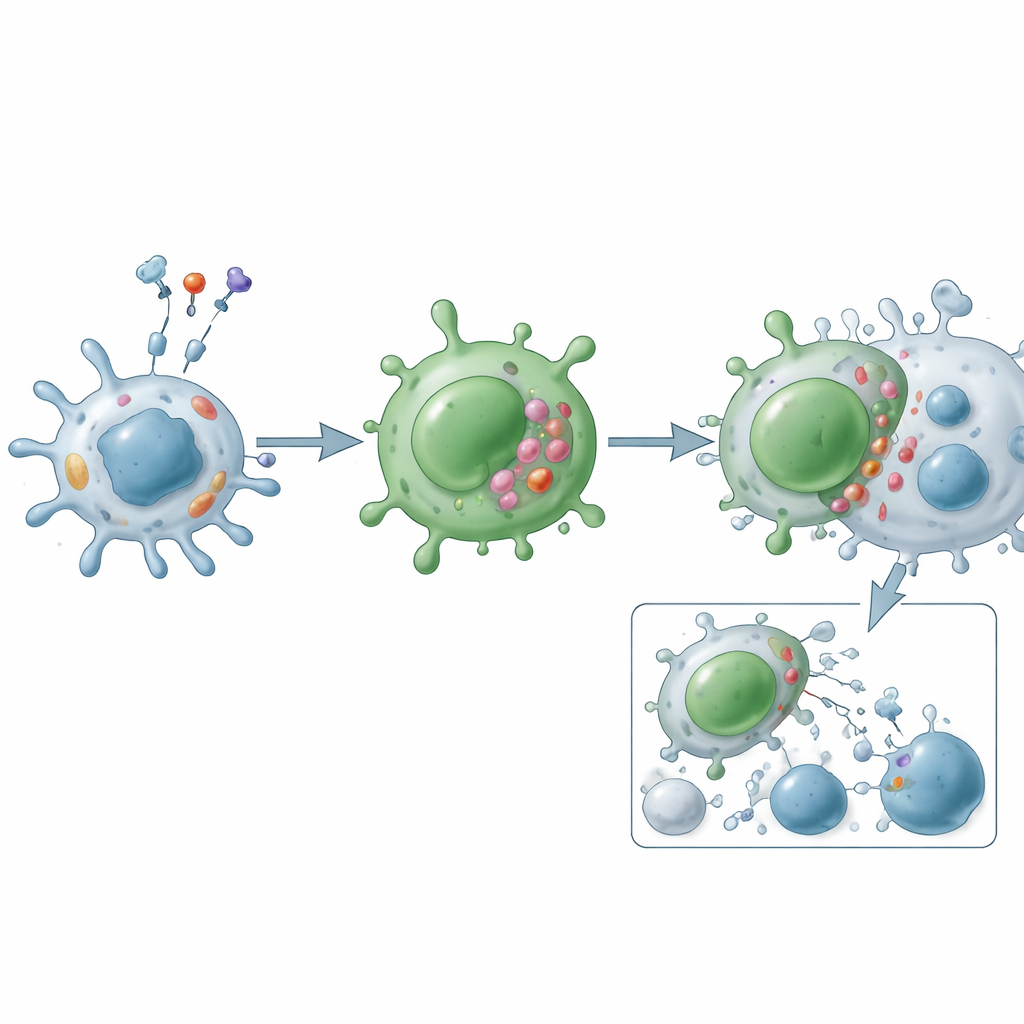
Vrienden bij infectie en kanker, vijanden bij auto-immuniteit en hartziekte
Dit tweeledige gedrag komt in veel aandoeningen naar voren. Bij chronische hepatitis B, HIV en COVID-19 helpen cytotoxische CD4 T-cellen virussen onder controle te houden wanneer CD8-killers uitgeput zijn, en hun aanwezigheid kan correleren met betere controle of herstel. In solide tumoren en bloedkankers kunnen ze tumorcellen die de juiste immuursignalen of stresssignalen tonen direct herkennen en mogelijk de respons op immunotherapieën zoals checkpointremmers en CAR-T-celbehandelingen verbeteren. Tegelijkertijd kunnen dezelfde mechanismen schade veroorzaken: bij lupus, reumatoïde artritis, inflammatoire darmaandoeningen, coronaire hartziekte, boezemfibrilleren, reuzenceltakarteritis en orgaantransplantaatafstoting infiltreren uitgebreide populaties cytotoxische CD4 T-cellen weefsels, beschadigen bloedvaten of organen en versterken langdurige ontsteking, wat vaak samenhangt met een slechtere prognose.
Een riskant instrument omzetten in therapie
Aangezien cytotoxische CD4 T-cellen zowel beschermend als destructief kunnen zijn, belicht het artikel opkomende therapeutische strategieën die erop gericht zijn deze populatie fijner af te stemmen in plaats van simpelweg uit te schakelen. Een benadering is het dempen van hun schadelijke activiteit met selectieve remmers die costimulerende receptoren (zoals OX40 of 4-1BB), inflammatoire cytokinen, ionkanalen of overlevingsroutes targeten. Een andere is het benutten van hun dodelijke kracht in adoptieve celtherapieën, inclusief genetisch bewerkte T-cellen en CAR-T-cellen, waarbij cytotoxische CD4-cellen vaak betere persistentie tonen dan uitsluitend CD8-producten. Een derde strategie stelt voor langlevende, virus-specifieke CD4-killers naar tumoren te heroriënteren met vaccins of pathogeen-afgeleide peptiden die door kankercellen worden gepresenteerd. Samen positioneren deze onderzoeksrichtingen cytotoxische CD4 T-cellen niet slechts als een biologische curiositeit, maar als een centraal hefboompunt voor toekomstige behandelingen die de verdediging tegen infecties en kanker preciezer kunnen versterken en tegelijkertijd weefselvernietigende ontsteking verminderen.
Een nieuwe hefboom voor toekomstige immuuntherapieën
Voor niet-specialisten is de kernboodschap dat “helper”-CD4 T-cellen veel veelzijdiger zijn dan lange tijd werd aangenomen: sommige kunnen overschakelen naar volledig gewapende moordenaars die ons beschermen tegen hardnekkige infecties en kanker, maar ook bijdragen aan auto-immuniteit, vaatbeschadiging en transplantaatafstoting. De review betoogt dat leren hoe deze cellen gevolgd kunnen worden, te voorspellen wanneer ze zullen helpen of schaden, en hun gedrag aan te passen met medicatie of geïngineerde therapieën, de manier waarop we een breed scala aan chronische ziekten behandelen kan hervormen — van hepatitis en HIV tot artritis, colitis, hartziekte en leukemie. In plaats van het immuunsysteem simpelweg harder of zachter te zetten, kunnen toekomstige therapieën steeds meer werken door krachtige celtypen zoals cytotoxische CD4 T-cellen te sturen naar nuttige doelen en weg van onze eigen weefsels.
Bronvermelding: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Trefwoorden: cytotoxische CD4 T-cellen, plasticiteit van immuuncellen, chronische ontsteking, kankerimmunotherapie, auto-immuunziekte