Clear Sky Science · nl
IFFO1 remt borstkanker door mitochondriale splitsing en vetzuursynthese te coördineren via de LaminA/C‑PGC1α-as
Waarom dit onderzoek ertoe doet
Borstkanker blijft een van de belangrijkste doodsoorzaken door kanker bij vrouwen, grotendeels omdat sommige tumoren blijven groeien, uitzaaien en huidige behandelingen omzeilen. Deze studie onthult een tot nu toe ondergewaardeerd cellulaire "rem" genaamd IFFO1 die borstkanker vertraagt door twee kernmotoren van tumorgroei te beteugelen: de energiecentrales van de cel, de mitochondriën, en het vermogen van de cel om vetten te maken en op te slaan. Inzicht in deze rem biedt een nieuw aangrijpingspunt voor therapieën die mogelijk effectief zijn bij meerdere subtypes van borstkanker.
Een verborgen beschermer binnen borstcellen
De onderzoekers begonnen met het onderzoeken van monsters van 30 vrouwen met borstkanker, evenals grote openbare kankerdatabanken. Ze ontdekten dat de niveaus van het eiwit IFFO1 consequent lager waren in tumorweefsel dan in aangrenzend normaal borstweefsel. Hoe geavanceerder het stadium van de kanker, hoe minder IFFO1 aanwezig was, en patiënten van wie de tumoren meer IFFO1 bevatten, hadden doorgaans een langere overleving. In gekweekte borstkankercellen verminderde het geforceerd overexpressen van IFFO1 scherp hun vermogen om te groeien, zich te delen en te migreren—gedragingen die nodig zijn voor tumorexpansie en -uitzaaiing. IFFO1 dempte ook een cellair programma dat bekend staat als epitheliaal–mesenchymale transitie, dat kankercellen helpt los te komen en andere weefsels binnen te dringen.
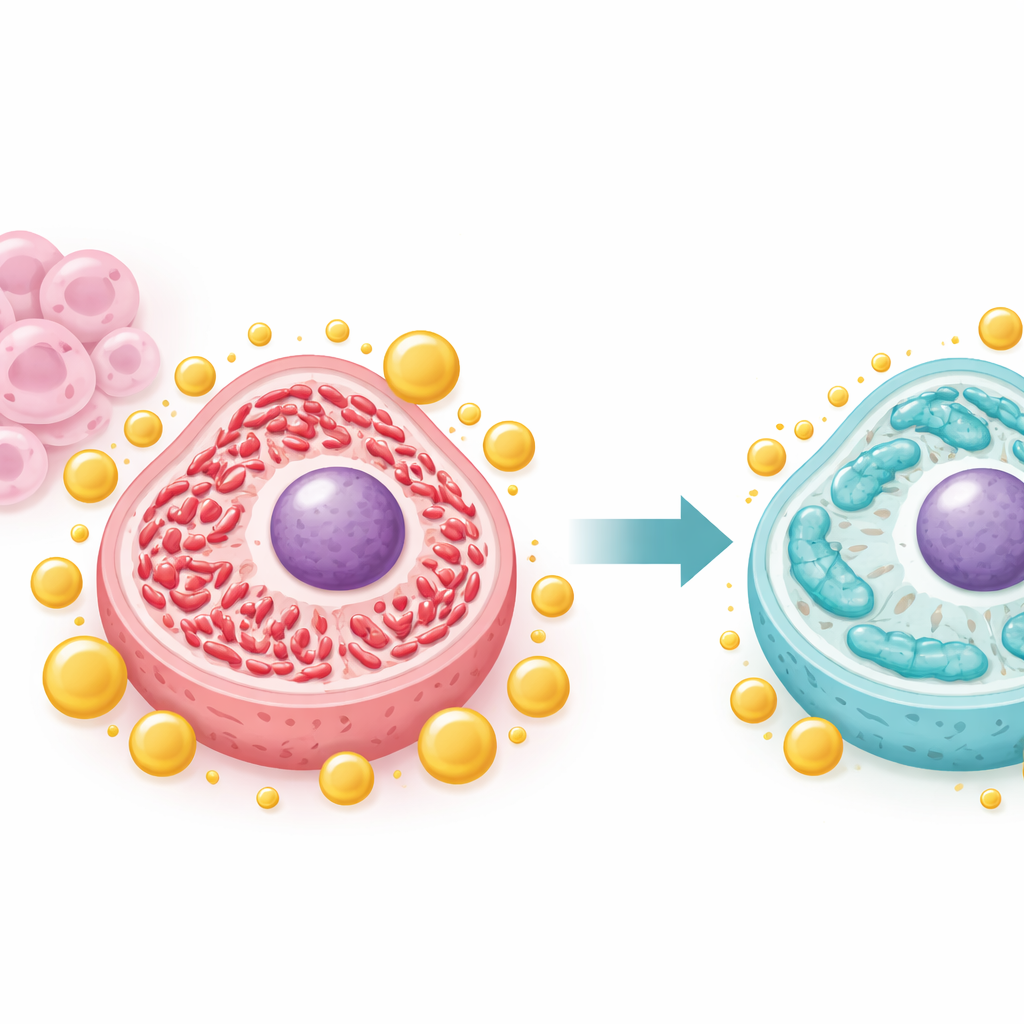
Het kalmeren van overactieve energiecentrales
Kankercellen hervormen vaak hun mitochondriën, de kleine energiecentrales in cellen, om snelle groei te ondersteunen. Het team toonde aan dat IFFO1 dit evenwicht verschuift weg van een sterk versnipperde, "fission"-toestand naar een meer uitgerekte, "fusion"-toestand die over het algemeen geassocieerd is met gezondere, stabielere mitochondriën. Wanneer IFFO1 overvloedig aanwezig was, daalden sleutelproteïnen voor fission zoals Drp1 en Fis1, terwijl fusie-eiwitten toenamen. Microscopen lieten zien dat mitochondriën langer en minder gefragmenteerd werden, en metingen van mitochondriaal DNA en energieproductie daalden ten opzichte van de abnormaal hoge niveaus die in agressieve cellen werden gezien. Deze veranderingen suggereren dat IFFO1 voorkomt dat mitochondriën in een hyperactieve configuratie komen die ongecontroleerde tumorgroei ondersteunt.
De vettoevoer afsluiten
Snelgroeiende tumoren hebben niet alleen energie nodig; ze hebben ook een constante toevoer van vetten om nieuwe membranen en signaalmoleculen op te bouwen. De studie vond dat IFFO1 ook deze metabole versnellingsknop indrukt. In cellen met extra IFFO1 waren kernbouwproteïnen voor vet—waaronder FASN, SREBP‑1, SCD1 en anderen—verminderd. Enzymtests bevestigden een lagere vet-synthetiserende activiteit, en chemische analyses toonden dalingen in vrije vetzuren, triglyceriden en cholesterol. Beeldvormende kleurstoffen die vetopslag zichtbaar maken, toonden minder lipidedruppels en minder neutrale vetten in de kankercellen. Omgekeerd had het verhogen van het fission-eiwit Drp1 het tegengestelde effect en stimuleerde het vetproductie, terwijl het stilleggen van Drp1 die productie remde—wat een direct verband ondersteunt tussen mitochondriale morfologie en vetvoorziening bij kanker.
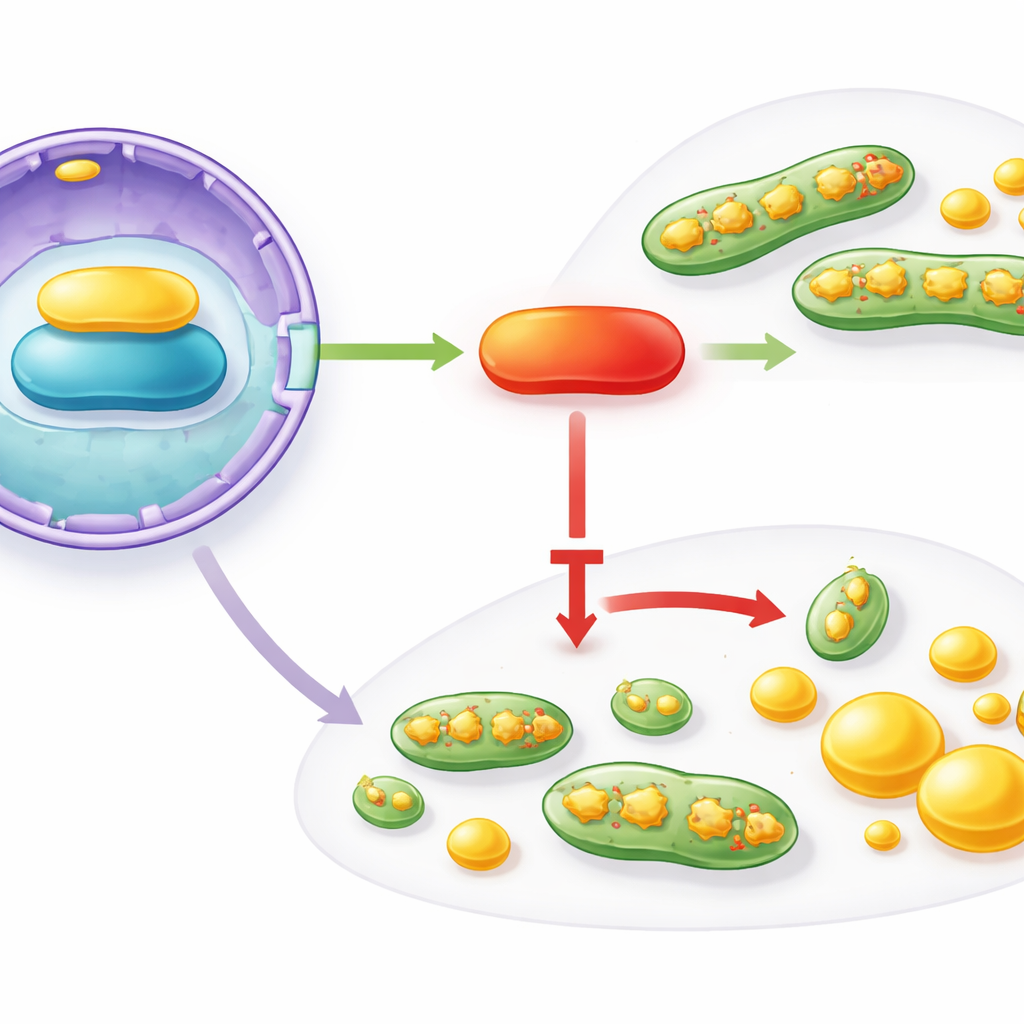
Een signaleringsketen van de kern naar de mitochondriën
Hoe orkestreert IFFO1 deze brede veranderingen? De auteurs brachten een keten van interacties in kaart die begint in de celkern en eindigt bij de mitochondriën en het vetmaakmachinerie. IFFO1 bindt fysiek aan een structureel eiwit van de kernomhulling genaamd Lamin A/C en verhoogt diens niveau. Lamin A/C ondersteunt op zijn beurt de activiteit van PGC1α, een meesterregelaar die mitochondriale gezondheid en metabolisme bewaakt. In borstkankertissues en -cellen bleken zowel Lamin A/C als PGC1α verlaagd te zijn, wat de afname van IFFO1 weerspiegelt. Toen de wetenschappers IFFO1 kunstmatig verhoogden, stegen Lamin A/C en PGC1α, nam mitochondriale fission af en verminderde vetzuursynthese. Het onderdrukken van Lamin A/C maakte deze voordelen ongedaan, maar het herstellen van PGC1α bracht ze terug, waarmee een functionele IFFO1 → Lamin A/C → PGC1α-as wordt aangetoond die tumorbevorderende mitochondriale en lipideveranderingen remt.
De rem testen in levende dieren
Om te zien of deze cellulaire effecten zich vertalen naar echte tumoren, plaatste het team humane borstkankercellen met of zonder extra IFFO1 in muizen. Tumoren met verhoogd IFFO1 groeiden langzamer, wogen minder bij het experimentele eindpunt en vertoonden minder tekenen van vetophoping. In een apart model waarin kankercellen in de bloedbaan werden geïnjecteerd om longmetastasen te zaaien, vormden cellen die te veel IFFO1 produceerden aanzienlijk minder longknobbels. Weefselanalyses van deze muizen weerspiegelden de celkweekbevindingen: hogere Lamin A/C en PGC1α, minder mitochondriale fission en lagere vetzuursynthese.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk presenteert dit werk IFFO1 als een meervoudig werkende tumorsuppressor die het cellulaire skelet, de energiecentrales en de vetmaakmachinerie met elkaar verbindt. Door Lamin A/C te stabiliseren en PGC1α te versterken, voorkomt IFFO1 dat mitochondriën te veel fragmenteren en snijdt het de overproductie van vetten af waarop kankercellen vertrouwen. Voor niet‑specialisten is de kernboodschap dat dit eiwit fungeert als een interne rem op zowel de energie als de bouwstenen die borstkankergroei en -uitzaaiing voeden. Medicijnen die IFFO1-niveaus verhogen of de effecten ervan op de Lamin A/C–PGC1α-route nabootsen, zouden op een dag nieuwe opties kunnen bieden, vooral voor agressieve of therapieresistente vormen van borstkanker.
Bronvermelding: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Trefwoorden: borstkanker, mitochondriale dynamiek, vetzuursynthese, tumormetabolisme, PGC1α-route