Clear Sky Science · nl
De oncogene controle van nucleotide-synthese
Waarom kankercellen geven om bouwstenen
Kanker wordt vaak omschreven als cellen die niet stoppen met delen. Maar om zichzelf te kopiëren hebben deze cellen een constante toevoer nodig van kleine bouwstenen genaamd nucleotiden, die DNA en RNA vormen en ook veel celprocessen van energie voorzien. Dit overzicht legt uit hoe kankerverwekkende genen de celchemie herschakelen om de nucleotideproductie hoog te houden, hoe tumoren schakelen tussen verschillende manieren om deze moleculen te verkrijgen, en hoe artsen deze trucs kunnen benutten met oude en nieuwe medicijnen.
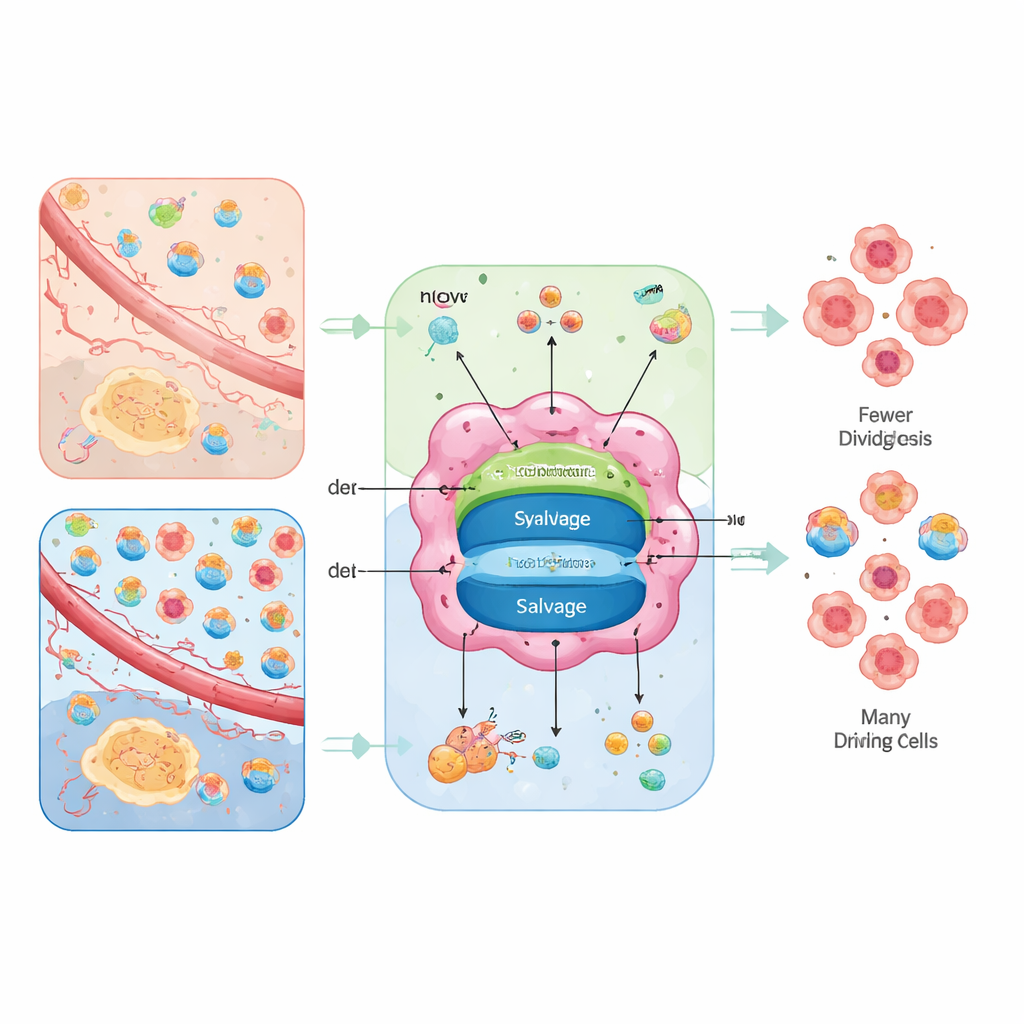
Twee wegen naar dezelfde bouwstenen
Cellen kunnen nucleotiden from scratch maken of recyclen. De "from scratch"-route, de zogenaamde de novo-synthese, bouwt ringen uit basisnutriënten zoals glucose, aminozuren, kooldioxide en bicarbonaat, via energie-intensieve meerstapsreacties. De recyclingroute, salvage genoemd, neemt afgebroken basen en nucleosiden uit de omgeving of uit celafval en zet die tegen veel lagere energiekosten terug in bruikbare nucleotiden. Tumoren gebruiken beide opties, maar de balans ertussen hangt af van hun interne energievoorziening en wat het omringende weefsel levert.
Hoe de tumoromgeving de keuze stuurt
De auteurs kaderen de nucleotidevoorziening als een "omgeving-gestuurde routering". In slecht gevoede gebieden waar aminozuren aanwezig zijn maar vrije nucleosiden schaars, leunen kankercellen sterk op de novo-paden en worden ze kwetsbaar voor middelen die deze stappen blokkeren. In beter doorbloede regio's, waar het bloed veel nucleosiden levert of waar mitochondriën zwak zijn, kunnen tumoren meer op salvage vertrouwen en gevoelig worden voor blokkering van transporters die nucleoside-opname verhinderen. Wanneer beide opties openstaan, vertonen tumoren metabole flexibiliteit en kunnen ze monotherapieën ontwijken; wanneer beide gesloten zijn, stagneert DNA-replicatie, hoopt schade zich op en kunnen cellen sterven of overschakelen naar meer gerijpte, minder agressieve toestanden.
Verborgen aanvoerlijnen die nucleotidevoorziening voeden
Het draaiende houden van nucleotidefabrieken vereist meerdere ondersteunende circuits. De pentosefosfaatroute levert het suikerruggengraat en reducerende kracht; glutamine en de energieproducerende cyclus in mitochondriën verschaffen stikstof en aspartaat; serine-, glycine- en folaatchemie doneren één-koolstofeenheden die de ringen voltooien; bicarbonaat brengt essentiële koolstoffen in. Kankeraanstuwers zoals PI3K–AKT–mTORC1, RAS–MAPK en MYC zetten deze paden gezamenlijk hoger, versterken sleutelenzymen en assembleren soms multi-enzymcomplexen die onstabiele intermediairen efficiënt kanaaliseren. Terughouders zoals LKB1–AMPK en p53 werken juist als remmen en verminderen normaal gesproken nucleotide-output wanneer energie of DNA-integriteit in gevaar is—remmen die veel tumoren uitschakelen.
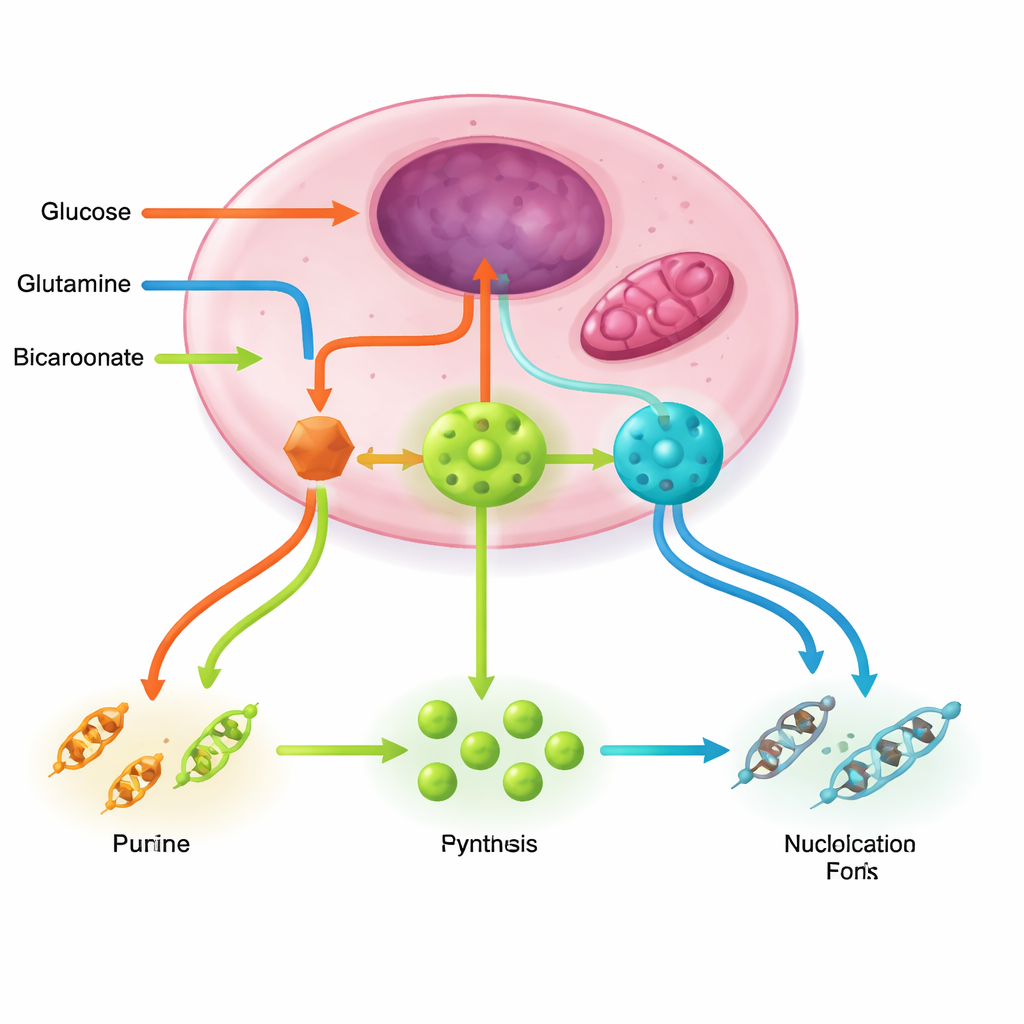
Oude chemotherapie, nieuwe metabole logica
Aangezien snelgroeiende cellen zo afhankelijk zijn van nucleotiden, richtte een aantal van de vroegste chemotherapieën zich op deze zwakte. Klassieke middelen zoals methotrexaat, 5‑fluorouracil, cytarabine, gemcitabine en diverse purine-analoogmoleculen blokkeren ofwel folaatgebruik, remmen specifieke enzymen, of doen zich voor als foutieve bouwstenen die DNA en RNA vergiftigen. Het overzicht bekijkt deze medicijnen opnieuw door de bril van het routeringsmodel en legt uit waarom bijwerkingen en resistentie veel voorkomen: niet-kankervrije weefsels hebben ook nucleotiden nodig, en tumoren kunnen vaak het flux omleiden via salvage of parallelle paden wanneer één knooppunt wordt geblokkeerd.
Next-generation strategieën en open vragen
Nieuwere benaderingen streven naar meer selectiviteit door de meest kankergebiaste onderdelen van het netwerk aan te vallen. Experimentele middelen worden ontwikkeld tegen mitochondriale één-koolstofenzymen zoals MTHFD2, het pyrimidine-enzym DHODH, en purine-enzymen zoals IMPDH en PAICS, vaak in combinaties die ook salvage-transporters blokkeren. De auteurs stellen praktische markers voor—zoals transporter-niveaus, dichtheid van bloedvaten, mitochondriale fitheid en expressie van specifieke metabole enzymen—om te bepalen welke tumoren meer op de novo of op salvage vertrouwen en om patiënten te matchen met padgerichte therapieën. Vooruitkijkend benadrukken ze sleutelvragen, waaronder hoe deze routes in ruimte en tijd verschuiven binnen werkelijke tumoren, hoe omgevende immuun- en stroma-cellen nucleotidebeschikbaarheid vormen, en hoe tolerabele doseringsschema's te ontwerpen die replicatiestress exploiteren zonder normale weefsels te overweldigen. Gezamenlijk bepleit dit werk dat het begrijpen en doelgericht aanpakken van nucleotidemetabolisme een fundamentele eis van celdeling kan omzetten in een krachtig, gepersonaliseerd instrument tegen kanker.
Bronvermelding: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Trefwoorden: nucleotidemetabolisme, kankermetabolisme, de novo synthese, salvage routes, metabole therapieën