Clear Sky Science · nl
Transcriptomische profilering van co-gecultiveerde kanker- en gastheercellen identificeert hypoxie als drijfveer van het anti-proliferatieve effect van skeletspiercellen op kankercellen
Waarom sommige weefsels resistent zijn tegen kankerspreiding
Kanker wordt doorgaans dodelijk wanneer tumorcellen hun oorspronkelijke locatie verlaten en zich in verre organen vestigen. Vreemd genoeg zijn sommige weefsels, zoals de longen, frequente aankomstplaatsen, terwijl andere, zoals skeletspier, bijna nooit gekoloniseerd worden ondanks dat ze een groot deel van het lichaamsgewicht uitmaken. Deze studie stelt een eenvoudige maar belangrijke vraag voor patiënten en artsen: wat is het aan spier dat het zo slecht maakt als voedingsbodem voor kankercellen, en kan inzicht in deze natuurlijke verdediging onze benadering van de behandeling van metastasen veranderen?
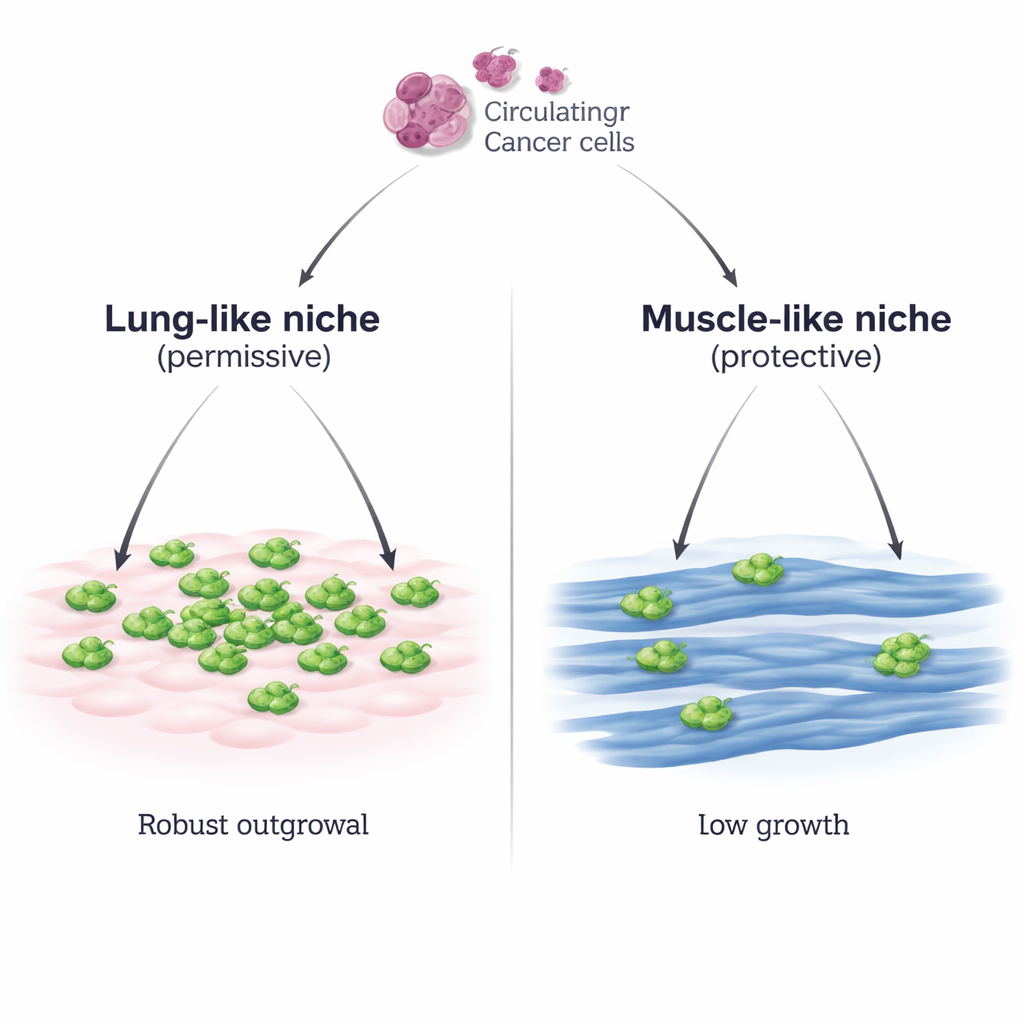
Twee buurten voor reizende tumorcellen
De onderzoekers ontwikkelden een gecontroleerd laboratoriumsysteem dat twee verschillende buurten nabootst die een borstkankercel kan tegenkomen: een longachtig milieu bestaande uit longbindweefselcellen (MLg), en een spierachtig milieu bestaande uit rijpe skeletspiervezels (C2C12-myotubes). Ze plaatsten muis-borstkankercellen bovenop elke laag en observeerden wat er gebeurde. Op de longachtige cellen hechtten kankercellen goed en vermenigvuldigden zich vervolgens snel, waarbij ze dichte gebieden vormden. Op de spiercellen hechtten ze even goed, maar bleef hun groei schaars en traag, zelfs wanneer het aanvangsaantal kankercellen sterk werd verhoogd of wanneer een tweede borstkankercellijn werd gebruikt. Een aparte skeletspierrij (Sol8) toonde hetzelfde vermogen om kankergroei terug te houden, wat benadrukt dat dit een algemeen kenmerk van spiercellen is en geen eigenaardigheid van één celtype.
Hoe kanker- en gastheercellen hun activiteit herprogrammeren
Om te begrijpen wat er in de cellen gebeurde, isoleerde het team kankercellen en gastheercellen uit deze gemengde culturen en seqeunceerden hun RNA, een maat voor welke genen aan of uit staan. Kankercellen die op spiervezels zaten, ondergingen veel uitgebreidere veranderingen in genactiviteit dan die groeiden op longcellen, wat suggereert dat de spieromgeving hen dwingt zich sterk aan te passen. In de spiersituatie schakelden kankercellen programma’s in die gekoppeld zijn aan spierachtige kenmerken, energieprocessing en, verrassend genoeg, reacties op lage zuurstof (hypoxie). Tegelijkertijd werden de gebruikelijke genprogramma’s die snelle celdeling aansturen naar beneden bijgesteld. Daarentegen behielden kankercellen op longcellen een sterk op groei gericht profiel en vroegen veel minder herprogrammering, wat overeenkomt met het idee dat de longachtige niche permissief en gemakkelijk te exploiteren is voor tumorcellen.
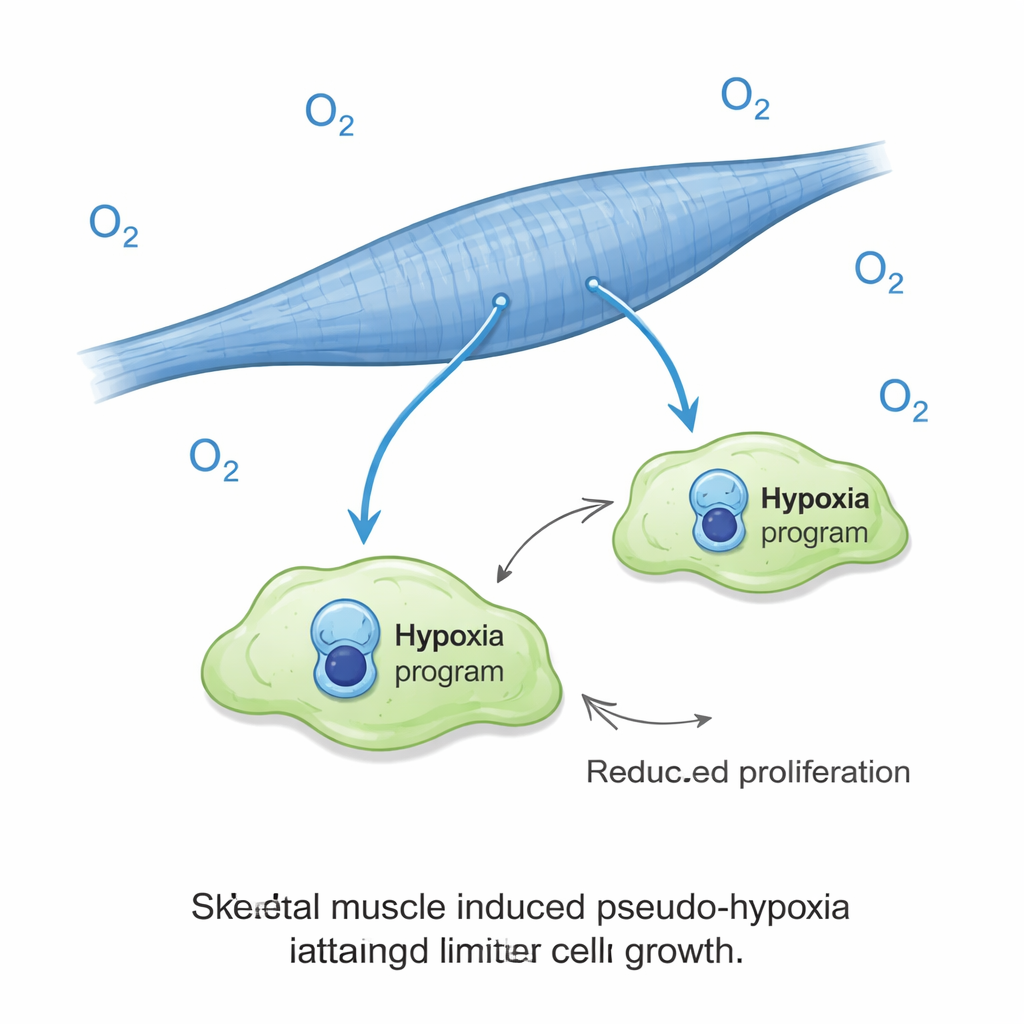
Een verrassende rol voor signalen van lage zuurstof
Een van de meest opvallende bevindingen was dat kankercellen op spiervezels een hypoxie-achtig genhandtekening inschakelden, hoewel ze onder normale zuurstofniveaus werden gekweekt. In de meeste tumoren is hypoxie een slecht teken, meestal gekoppeld aan agressief gedrag en slechte uitkomsten. Hier hing het samen met het tegenovergestelde: magere groei. De wetenschappers brachten de culturen vervolgens bloot aan werkelijk lage zuurstof en ontdekten dat dit de expansie van kankercellen op spier bijna uitwist, terwijl het de kankergroei in de longachtige culturen juist versterkte. Met andere woorden: hetzelfde signaal dat gewoonlijk tumoren helpt te gedijen, werd een rem wanneer kankercellen zich in een spieromgeving bevonden. Dit zuurstofeffect leek niet verklaard te kunnen worden door eenvoudige veranderingen in lactaat, zuurgraad of suikerbeschikbaarheid in het kweekmedium.
Meer dan alleen secreties
Het team onderzocht ook of simpele oplosbare stoffen die door spiercellen worden vrijgegeven hun beschermende effect konden verklaren. Het toevoegen van extra lactaat, het wijzigen van de zuurgraad, het veranderen van glucosewaarden of het kweken van kankercellen in medium dat eerder spieren had gebaad reproduceerde niet de sterke onderdrukking die werd gezien in directe contact co-culturen. Dit suggereert dat nauwe fysieke afstand, of zeer kortestralingssignalen aan het celoppervlak, cruciaal zijn voor hoe spiercellen kankercellen in een laag-groeimodus, mogelijk een dormante toestand, duwen. Interessant genoeg bleven spiercellen zelf relatief stabiel in hun genactiviteit wanneer ze met kanker werden geconfronteerd, terwijl longcellen gemakkelijker werden hergeprogrammeerd, wat spier benadrukt als een robuust "metastaseresistent" weefsel.
Wat dit betekent voor patiënten en therapieën
Al met al onthult de studie dat skeletspier fungeert als een vijandige habitat die kankercellen dwingt in een hypoxie-achtige, laag-proliferatieve modus, zelfs wanneer er voldoende zuurstof aanwezig is. Dit helpt verklaren waarom spier zo’n zeldzame locatie is voor metastasen. Het biedt ook een waarschuwende boodschap voor medicijnontwikkeling: therapieën die erop gericht zijn hypoxiesignaalgeving in het hele lichaam te blokkeren, zouden deze natuurlijke spiergebaseerde verdediging onbedoeld kunnen verzwakken, waardoor het voor kankercellen makkelijker wordt te groeien waar ze dat normaal niet zouden doen. Begrijpen en behouden, of zelfs nabootsen, van de beschermende eigenschappen van spierweefsel zou nieuwe wegen kunnen openen om metastatische ziekte te voorkomen of te beheersen.
Bronvermelding: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Trefwoorden: kankermetastase, skeletspier, hypoxie, tumormicro-omgeving, kankerdormantie