Clear Sky Science · nl
Vetzuuropname gemedieerd door FABP4 bevordert de veroudering (senescentie) van CD8+ T-cellen via lipideperoxidatie in het vetrijke micro‑milieu van eierstokkanker
Waarom vet en immuuncellen van belang zijn bij eierstokkanker
Eierstokkanker verspreidt zich vaak in de buikholte, waar grote vetafzettingen aanwezig zijn. Deze vette omgeving is geen passief decor—ze beïnvloedt actief het gedrag van immuuncellen. In het bijzonder kan zij de CD8‑“killer” T‑cellen verzwakken die tumorcellen zouden moeten aanvallen. In deze studie wordt onderzocht hoe vetafgeleide stoffen deze T‑cellen in een verouderde, uitgeputte toestand duwen, en hoe het blokkeren van een belangrijk vettransporteiwit hun kankervochtende vermogen mogelijk kan herstellen.
Vetrijke omgeving die immuunverdedigers doet verouderen
Artsen merken al langer dat veel vrouwen met gevorderde eierstokkanker vocht ophopen in de buik en tumoren hebben die liggen in vetrijke weefsels zoals het omentum. Door single‑cell RNA‑gegevens van patiënten te analyseren en tumormonsters onder de microscoop te bestuderen, vonden de onderzoekers dat CD8‑T‑cellen nabij deze vetafzettingen vaker kenmerken van cellulaire veroudering, of senescentie, vertoonden. Deze “verouderde” T‑cellen hopen afvalpigmenten op, stoppen met delen en produceren ontstekingssignalen in plaats van kankercellen te doden. Zowel in menselijke monsters als in muismodellen waren CD8‑T‑cellen afkomstig uit vet‑ en vocht‑rijke tumorgebieden duidelijk meer senescent dan die uit lymfeklieren of milt, waarmee het adipocyten‑rijke tumormicro‑milieu direct aan T‑cel veroudering wordt gekoppeld.
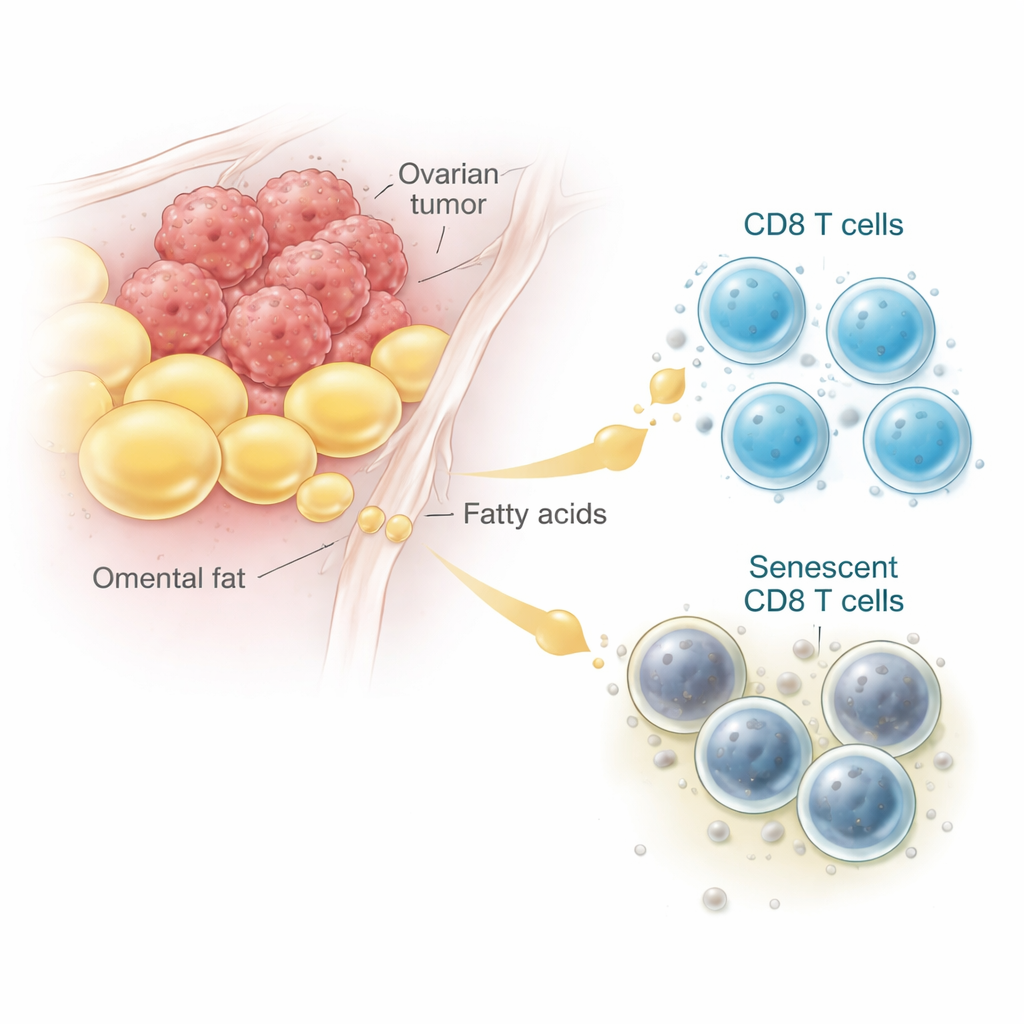
Hoe een veelvoorkomend vetzuur nuttige brandstof in schadelijke stoffen verandert
Om te begrijpen wat vet met T‑cellen doet, herbouwde het team de tumorsituatie in het laboratorium. Ze teelden eierstokkankercellen samen met muis CD8‑T‑cellen en voegden vervolgens ofwel extracten uit vetweefsel toe of een specifiek vetzuur, oliezuur, dat overvloedig aanwezig is in het vocht bij eierstokkanker. Bij matige tot hoge doses zorgde oliezuur ervoor dat meer CD8‑T‑cellen senescent werden—maar alleen wanneer tumorcellen aanwezig waren. In plaats van de binnenkomende vetten te verbranden voor energie, hoopten de T‑cellen lipiden op die chemisch beschadigden, een proces dat bekendstaat als lipideperoxidatie. Gen‑ en lipideanalyses toonden verhoogde markers van geoxideerde vetten en stresstekenen, terwijl energieproductie uit vet onveranderd bleef. Kortom, in aanwezigheid van tumor werd vet dat brandstof zou moeten zijn omgeleid naar schadelijke reacties die T‑cellen verouderen en uitschakelen.
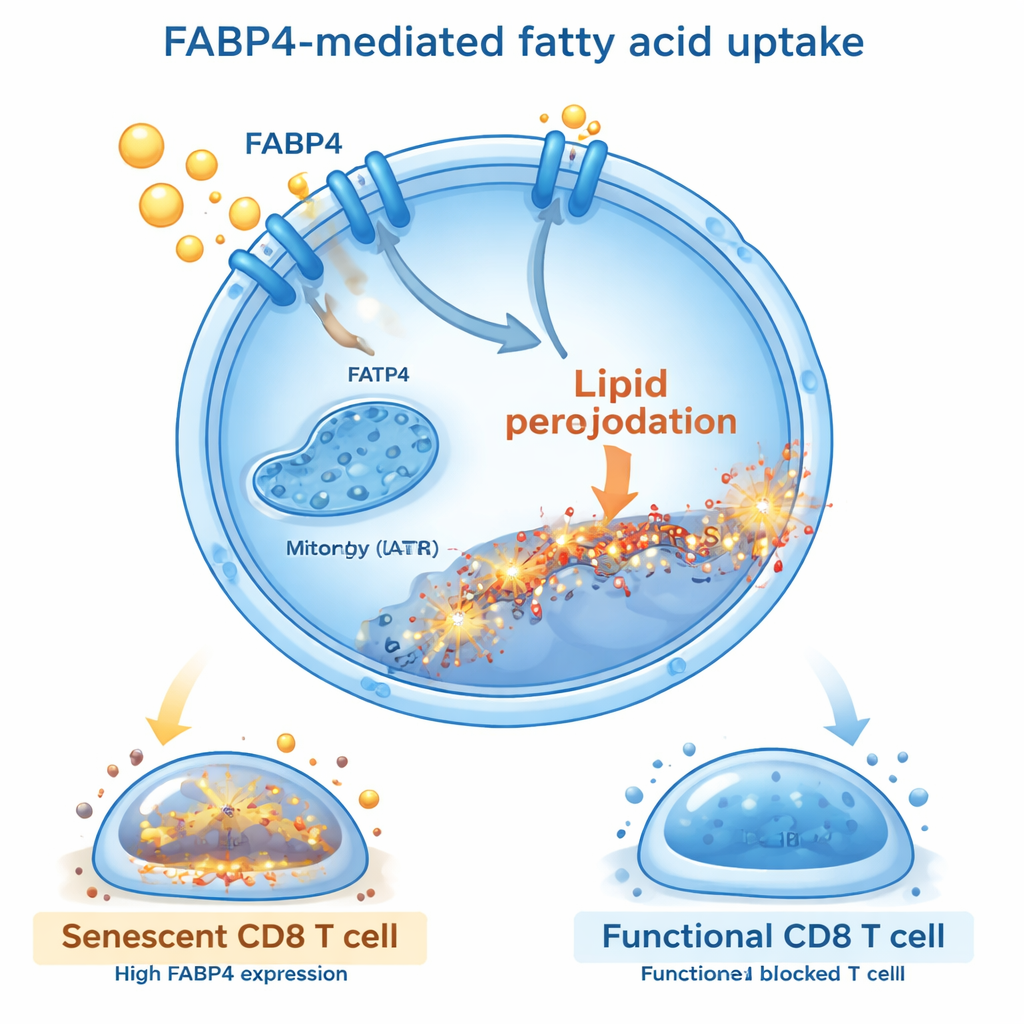
Het vettransporteiwit FABP4 als belangrijke poortwachter
Dieper gravend vroegen de onderzoekers welke moleculen deze schadelijke vetinflux aansturen. Ze ontdekten dat een transporteiwit genaamd FABP4 sterk werd aangezet in CD8‑T‑cellen die werden blootgesteld aan vetextracten of oliezuur. FABP4 werkt als een pendel die langeketenvetzuren de cel in vervoert. Wanneer ze FABP4 blokkeerden met behulp van een kleinmoleculair middel (BMS309403) of door genetische stillegging, namen T‑cellen minder vet op, vertoonden ze minder lipideperoxidatie en werden ze minder snel senescent. Deze beschermde T‑cellen deelden beter, produceerden meer kankerbestrijdende moleculen zoals interferon‑gamma en granzyme B, en scheidden minder onderdrukkende en ontstekingsbevorderende signalen uit. Het herstellen van FABP4‑niveaus keerde deze voordelen om, wat bevestigt dat dit transporteiwit een centrale schakel is die vetopname verbindt met T‑cel veroudering.
Van muisproeven naar een mogelijke behandelstrategie
Het team testte vervolgens FABP4‑blokkade in levende muizen met eierstokkanker die zich in de buikholte had verspreid. Behandeling van muizen met de FABP4‑remmer verminderde vetopname en lipideschade in CD8‑T‑cellen uit het buikvocht, verlaagde het aandeel senescente T‑cellen en verhoogde de niveaus van belangrijke effector‑moleculen. Wanneer de FABP4‑remmer werd gecombineerd met standaard chemotherapie, hadden muizen minder zichtbare tumorknobbels, sterkere T‑celresponsen in milt, lymfeklieren en ascites, en leefden ze langer dan muizen die alleen chemotherapie kregen. Deze bevindingen suggereren dat het gericht ingrijpen in vetmetabolisme bestaande behandelingen effectiever kan maken door de immuunstelsel‑voorposten te herstellen.
Wat dit betekent voor patiënten
Voor niet‑specialistische lezers is de kernboodschap dat bij eierstokkanker niet alleen de tumor zelf van belang is, maar ook de vette buurt waarin zij zich bevindt. Vetafgeleide moleculen, met name bepaalde vetzuren, kunnen killer‑T‑cellen voortijdig doen verouderen en hen beroven van hun vermogen om kanker aan te vallen. Dit werk identificeert het vettransporteiwit FABP4 als een belangrijke dader in dat proces. Door FABP4 te blokkeren, ten minste in muizen, kunnen onderzoekers T‑cel veroudering verminderen, hun dodelijke functie herstellen en de werkzaamheid van chemotherapie verbeteren. Hoewel meer onderzoek nodig is voordat dit een behandeling voor patiënten wordt, opent de studie een nieuw spoor: niet alleen de kanker zelf behandelen, maar ook de metabole valkuilen in het micro‑milieu die het immuunsysteem uitschakelen.
Bronvermelding: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Trefwoorden: eierstokkanker, T‑cel senescentie, vetzuurmetabolisme, tumormicro‑omgeving, FABP4