Clear Sky Science · nl
Veelvoorkomende genmutaties in 103 geverifieerde colorectale kankercellijnen
Waarom deze kankercellijnen van belang zijn
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd, en veel van wat we weten over het gedrag ervan en de behandeling ervan komt uit onderzoek met in het laboratorium gekweekte kankercellijnen. Deze modellen kunnen in de loop van de tijd echter afwijken en veranderen. Deze studie controleerde en catalogueerde zorgvuldig 103 veelgebruikte colorectale kankercellijnen en bracht belangrijke genmutaties in kaart die tumorgroei aansturen. Het resultaat is een gedetailleerde "veldgids" die onderzoekers helpt het juiste model voor de juiste vraag te kiezen, met als doel laboratoriumontdekkingen uiteindelijk meer kans te geven patiënten te helpen.
Een catalogus van kankermodellen
De onderzoekers stelden 103 colorectale kankercellijnen samen die samen de belangrijkste genetische subtypen weerspiegelen die bij patiënten worden gezien. De meeste stammen uit primaire colon- of rectumtumoren, de rest uit uitzaaiingen. Het team verifieerde eerst dat elke cellijn echt was wat ze beweerde te zijn, met behulp van vingerafdrukachtige DNA-markers die korte tandemherhalingen heten. Vervolgens gebruikten ze diepe gerichte sequencing, waarbij geselecteerde DNA-gebieden gemiddeld 575 keer werden gelezen, om 20 genen te onderzoeken die bekend zijn als belangrijk bij colorectale kanker. Die hoge diepte stelde hen in staat zelfs relatief zeldzame mutaties binnen een cellenpopulatie te detecteren en in te schatten hoe vaak elke mutatie voorkomt onder de cellen in een bepaalde lijn.
Verschillende wegen naar genetische chaos
Colorectale kankers kunnen tijdens hun ontwikkeling verschillende genetische routes volgen. Ongeveer vier van de vijf tumoren vertonen chromosomale instabiliteit, met grote stukken DNA die worden gewonnen of verloren. Andere tumoren zijn "hypergemuteerd" en stapelen veel kleine DNA-veranderingen op. Deze studie legde beide patronen vast. Zestien cellijnen toonden microsatellietinstabiliteit, een vorm van hypermutatie veroorzaakt door defecten in DNA-foutcorrectie, wat leidt tot frequente kleine inserties en deleties. Vijf andere lijnen hadden defecten in het DNA-proofreadinggen POLE, wat resulteerde in een zware lading enkelletter-DNA-veranderingen. De overige, niet-hypergemuteerde lijnen hadden minder mutaties maar vaker grootschalige veranderingen in het aantal kopieën van DNA. Deze onderscheidende signaturen leken sterk op die in echte patiënttumoren.
Belangrijke stuurgenen en gevaarlijke combinaties
Over de 20 onderzochte genen kwamen de mutatiepatronen overeen met grote klinische studies van colorectale kanker. Tumorsuppressorgen zoals APC, TP53 en SMAD4 werden vaak getroffen door truncerende mutaties die het eiwit breken, terwijl klassieke kankerbevorderende genen zoals KRAS en BRAF vaker één aminozuurveranderingen droegen die signaalroutes inschakelen. Niet-hypergemuteerde lijnen droegen vaak een groter aandeel duidelijk schadelijke, of pathogene, mutaties die in het merendeel of alle cellen in de kweek aanwezig waren. Daarentegen hadden hypergemuteerde lijnen veel extra "passagiers" en meer subclone mutaties die slechts in een fractie van de cellen voorkomen, wat voortdurende evolutie in de kweek weerspiegelt.
Verborgen patronen in geninteracties
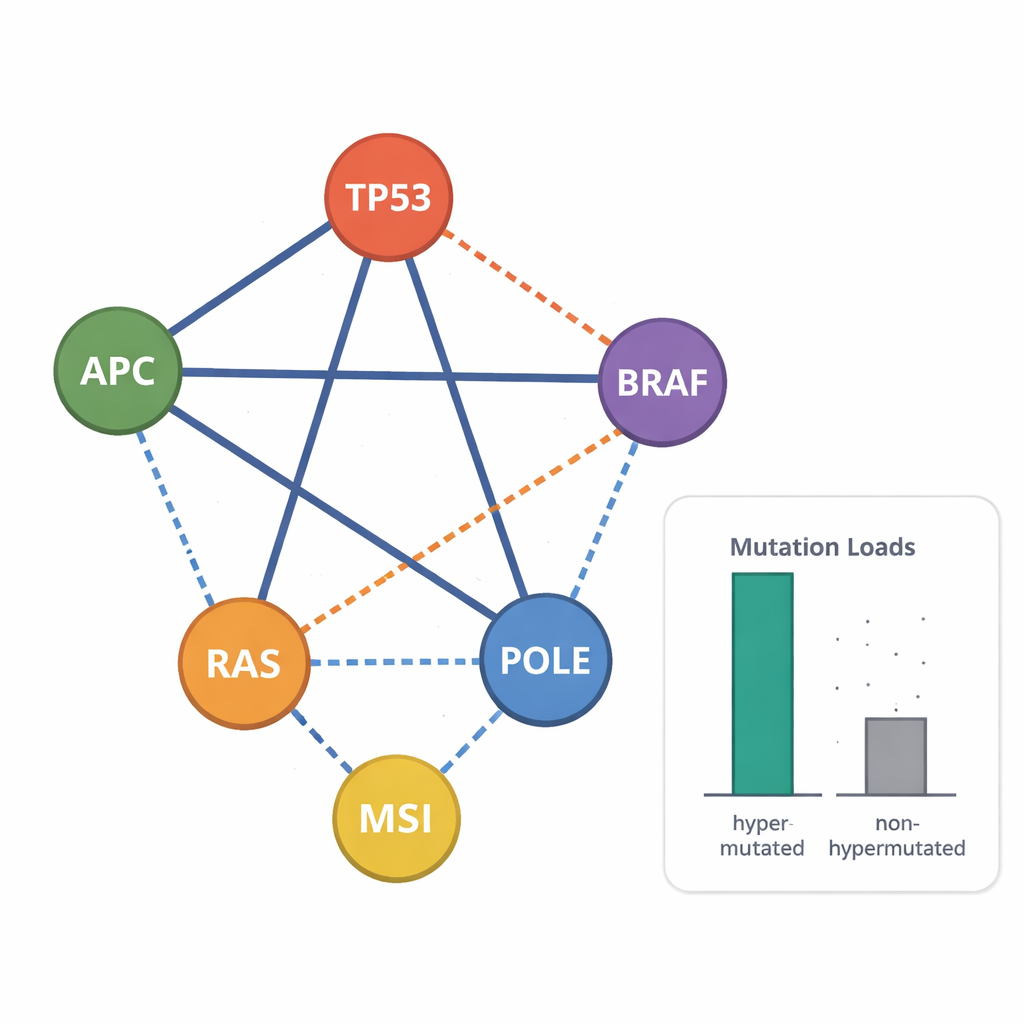
Door te kijken welke mutaties vaak samen voorkomen of elkaar vermijden, konden de wetenschappers genetische combinaties opsporen die gekoppeld zijn aan bijzonder agressieve ziektebeelden. Bijvoorbeeld, de veelvoorkomende hotspotmutatie BRAF p.V600 trad zelden samen op met mutaties in KRAS of NRAS, maar in een paar lijnen kwam ze wel voor naast truncerende APC-mutaties, wat echoot met een subtype met slechte prognose dat bij patiënten is waargenomen. Veel cellijnen hadden drievoudige hits in APC, TP53 en RAS-genen, een andere markering van hoog-risico tumoren. De studie ontdekte ook een karakteristiek "double-hit" patroon in APC: twee truncerende mutaties geplaatst zodat ten minste één β-catenine-bindingsregio behouden blijft, consistent met een "precies-goed" niveau van WNT-routeactivatie dat tumorgroei bevordert. Kopieaantalanalyse toonde frequente amplificaties van groeigerelateerde genen zoals MYC en EGFR, en verlies van hele kopieën van tumorsuppressorgenen, vooral in niet-hypergemuteerde lijnen.
Wat dit betekent voor toekomstig onderzoek
Voor wetenschappers die experimenten ontwerpen is de boodschap dat niet alle colorectale kankercellijnen gelijk zijn. Hypergemuteerde modellen zijn genetisch druk bezet en kunnen veel laag-niveaumutaties bevatten die het effect van een enkele mutatie vertroebelen. Niet-hypergemuteerde lijnen daarentegen dragen meestal minder maar sterkere en meer uniforme stuurmutaties. Door een zorgvuldig gevalideerde kaart te bieden van welke genen veranderd zijn, hoe ze veranderd zijn en hoe vaak elke mutatie voorkomt binnen elke kweek, stelt dit werk onderzoekers in staat de meest geschikte modellen te kiezen voor het testen van geneesmiddelen, het onderzoeken van biologie en het ontwikkelen van nieuwe gerichte therapieën of immunotherapiebenaderingen voor colorectale kanker.
Bronvermelding: Kranjec, C., Eilertsen, I.A., Nunes, L. et al. Common gene mutations in 103 authenticated colorectal cancer cell lines. Oncogenesis 15, 8 (2026). https://doi.org/10.1038/s41389-026-00599-0
Trefwoorden: colorectale kanker, kankercellijnen, genmutaties, tumorsubtypen, precisie-oncologie