Clear Sky Science · nl
Herschikking van het cytoskelet veroorzaakt door een nieuwe K6-K14 keratinefusie bevordert kankerstamcellen en cellulaire plasticiteit via cGAS-STING-selectie
Hoe vormveranderende kankercellen hun omgeving te slim af zijn
Kankercellen groeien niet alleen ongecontroleerd; ze leren ook hun eigen interne “skelet” buigen en verdraaien om te overleven, zich te verbergen en zich te verspreiden. Deze studie laat zien hoe een specifieke structurele afwijking in cellen van hoofd- en halskanker hun kern kan beschadigen, een ingebouwd alarm kan activeren, hen in een sluimerende staat kan duwen en hen uiteindelijk kan helpen terug te keren als agressievere, invasieve, stamcelachtige cellen. Inzicht in deze mechanische route van kankerontwikkeling zou nieuwe mogelijkheden kunnen openen om terugval en metastase te blokkeren.
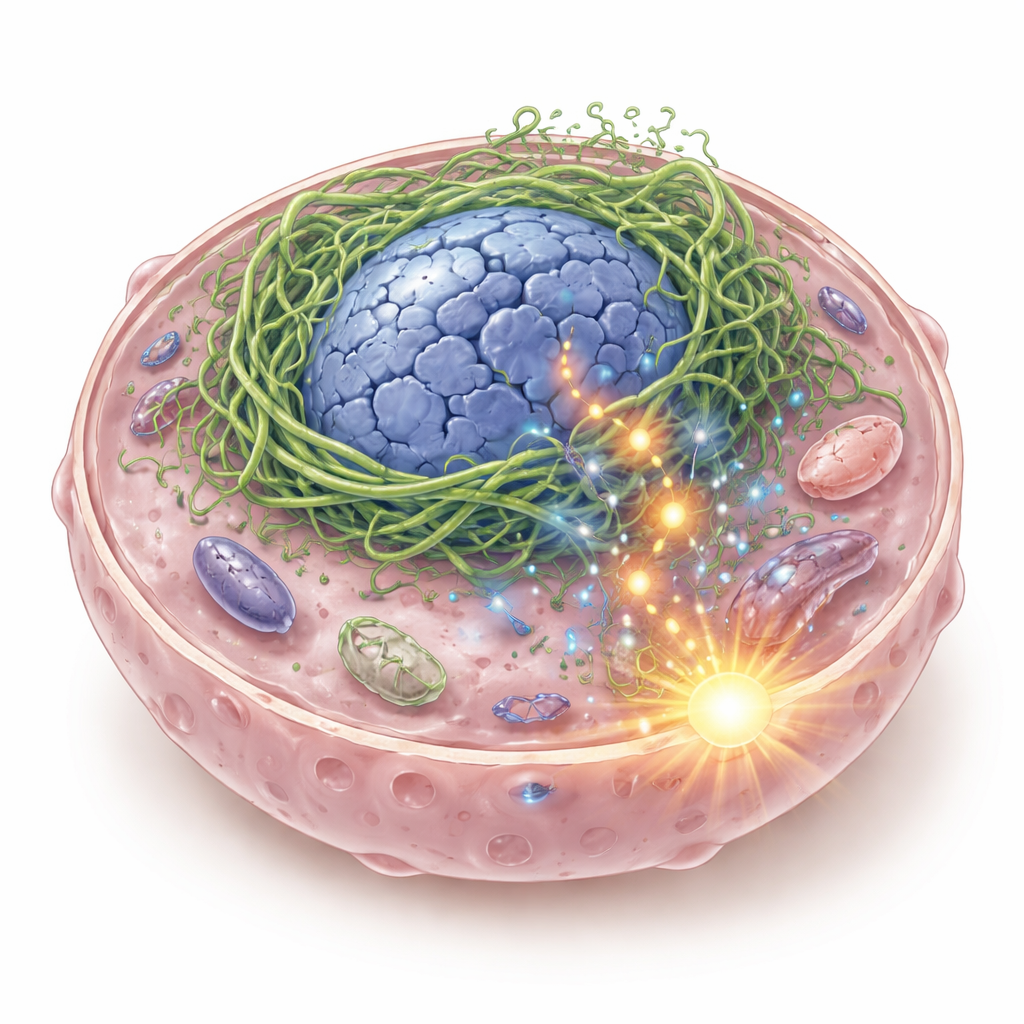
Een gebroken innerlijk geraamte met gevaarlijke gevolgen
In elke cel bevindt zich een flexibel geraamte van eiwitfilamenten dat de cel en haar kern vormgeeft en helpt fysieke krachten waar te nemen. De auteurs concentreerden zich op keratines, een familie van geraamte-eiwitten die veel voorkomen in epitheliale weefsels, waaronder de bekleding van mond en keel. In sommige plaveiselcelcarcinomen van hoofd en hals ontdekten ze een hybride keratine genaamd K6-K14/V5, gevormd wanneer twee keratinegenen samensmelten. Wanneer dit fusie-eiwit in kankercellen wordt geactiveerd, vormt het geen glad ondersteunend netwerk. In plaats daarvan klontert het rond de kern, vervormt die tot holle, misvormde structuren en veroorzaakt het DNA-breuken. Stukjes DNA lekken in het celvocht, waar ze worden gedetecteerd door een immuunsensorisch systeem genaamd cGAS–STING, dat normaal het alarm slaat bij viraal DNA.
Van druk naar celdood naar verborgen overleving
Het onmiddellijke gevolg van deze kernbeschadiging is schadelijk voor de kankercellen: hun groei vertraagt en velen sterven. Een deel weet echter te overleven. Deze overlevenden worden sterk beïnvloed door hun fysieke omgeving. Op standaard platte plastic schalen verdwijnen ze geleidelijk, maar wanneer ze worden gekweekt in een zachte collageengel — dichter bij de textuur van echt weefsel — blijven ze bestaan en verschijnen ze opnieuw als een nieuwe populatie, aangeduid als 3D-V5-cellen. Genexpressieanalyses laten zien dat deze cellen reageren op het aanhoudende DNA-schadealarm door autofagie in te schakelen, een zelfreinigingsprogramma dat beschadigde onderdelen recyclet, met name gebrekkige mitochondriën. Deze reactie helpt hen een sluimerende, laagactieve staat in te gaan die hen in staat stelt stress te doorstaan in plaats van te worden geëlimineerd.
Sluimerende cellen herbedraden en bereiden zich voor om te bewegen
Terwijl ze sluimeren, herschrijven deze overlevende cellen stilletjes hun interne programma's. Ze veranderen de samenstelling van keratine-eiwitten en nemen een “gedeeltelijke” epitheel–mesenchymale transitie (pEMT) aan — een tussentijdse identiteit die enkele epitheliale eigenschappen behoudt maar flexibiliteit en beweeglijkheid wint. Ze worden veel beter in het vormen van bolletjes en het zaaien van nieuwe celclusters, een kenmerk van kanker‑stamcellen. In de loop van de tijd herstellen hun mechanische eigenschappen: ze verzwaren opnieuw hun kernen, herbouwen sterke actinevezels en ontwikkelen lange uitsteeksels die het omringende matrix onderzoeken en vastgrijpen. Ze verhogen ook de productie van enzymen die matrix metalloproteïnases (MMPs) worden genoemd, die het extracellulaire netwerk afbreken en paden voor invasie openen.
Communicatie met buurcellen om een ondersteunend niche te bouwen
Deze hergeprogrammeerde kankercellen handelen niet alleen. Het team observeerde dat 3D‑V5-cellen grote aantallen kleine pakketjes, extracellulaire vesikels genoemd, in hun omgeving vrijgeven. Wanneer deze vesikels dichtbij gelegen orale fibroblasten — bindweefselcellen — bereiken, verandert de genactiviteit van die fibroblasten en worden ze meer vergelijkbaar met kankergeassocieerde fibroblasten die tumorgroei ondersteunen. Veel van de uitgewisselde signalen draaien rond de FGF–FGFR-as, een familie van groeifactoren en hun receptoren die bekendstaan om het stimuleren van celproliferatie, plasticiteit en resistentie. Zowel in kweek als in muizen met tumoren verminderde het blokkeren van FGFR-activiteit dit groeivoordeel. In dieren waren tumoren gevormd door 3D‑V5-cellen slecht gedifferentieerd, invasiever, rijk aan stamcelmarkers en vatbaarder om zich buiten de injectieplaats te verspreiden.
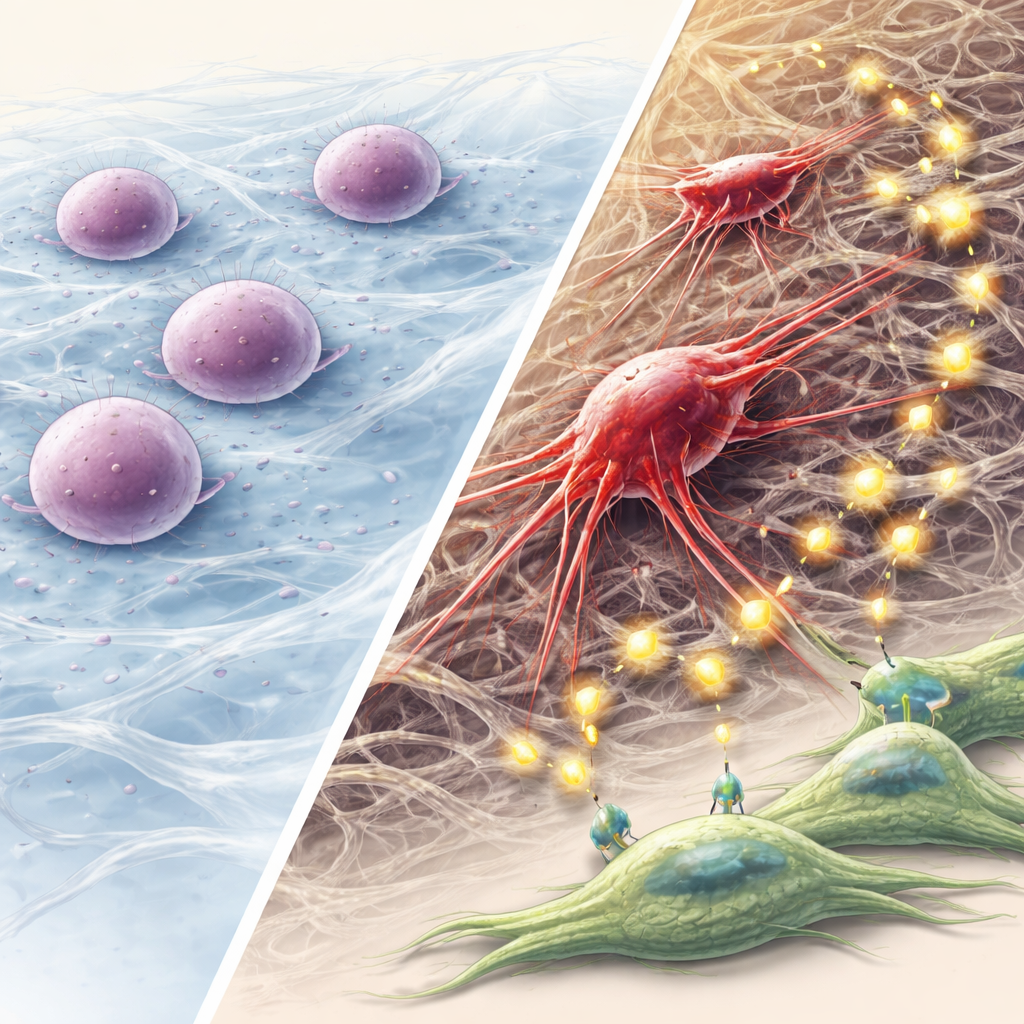
Waarom deze mechanische route naar agressieve kanker ertoe doet
Dit werk stelt een stapsgewijs model voor: een keratinefusie verstoort het interne geraamte van de cel, verplettert de kern en activeert een DNA‑schadealarm; autofagie stelt vervolgens een paar cellen in staat in dormantie te gaan in plaats van te sterven; in de loop van de tijd reorganiseren deze overlevenden hun skelet, verwerven ze stamcelachtige en invasieve eigenschappen en herschikken ze hun omgeving via vesikels en FGF‑signaalgeving. Voor niet‑specialisten is de kernboodschap dat fysieke krachten en structurele eiwitten binnen cellen net zo belangrijk kunnen zijn als genen en chemische signalen in het aandrijven van kankerontwikkeling. Het gericht aanpakken van deze mechanische stress–autofagie–FGF‑route, vooral in hoofd‑ en halskankers met keratinefusies, kan nieuwe strategieën bieden om te voorkomen dat sluimerende tumorcellen opnieuw ontwaken en zich verspreiden.
Bronvermelding: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Trefwoorden: kanker-stamcellen, celcytoskelet, tumordormantie, hoofd- en halstumor, mechanotransductie