Clear Sky Science · nl
De rol van histon-demethylase PHF2 als tumorsuppressor bij hepatocellulair carcinoom door regulatie van SRXN1
Waarom deze studie naar leverkanker ertoe doet
Leverkanker behoort tot de dodelijkste kankersoorten wereldwijd, en bestaande medicijnen verlengen voor veel patiënten de levensduur slechts beperkt. Deze studie stelt een andere vraag: in plaats van de gebruikelijke kankergendrivers te targeten, kunnen we de manier waarop DNA in levercellen verpakt en chemisch gemarkeerd is benutten om nieuwe, meer precieze behandelingsopties te vinden? De onderzoekers richten zich op een weinig bekend eiwit, PHF2, en onthullen hoe het mogelijk helpt voorkomen dat levercellen kankerachtig worden.
Zoeken naar kwetsbaarheden in het controlemechanisme van kanker
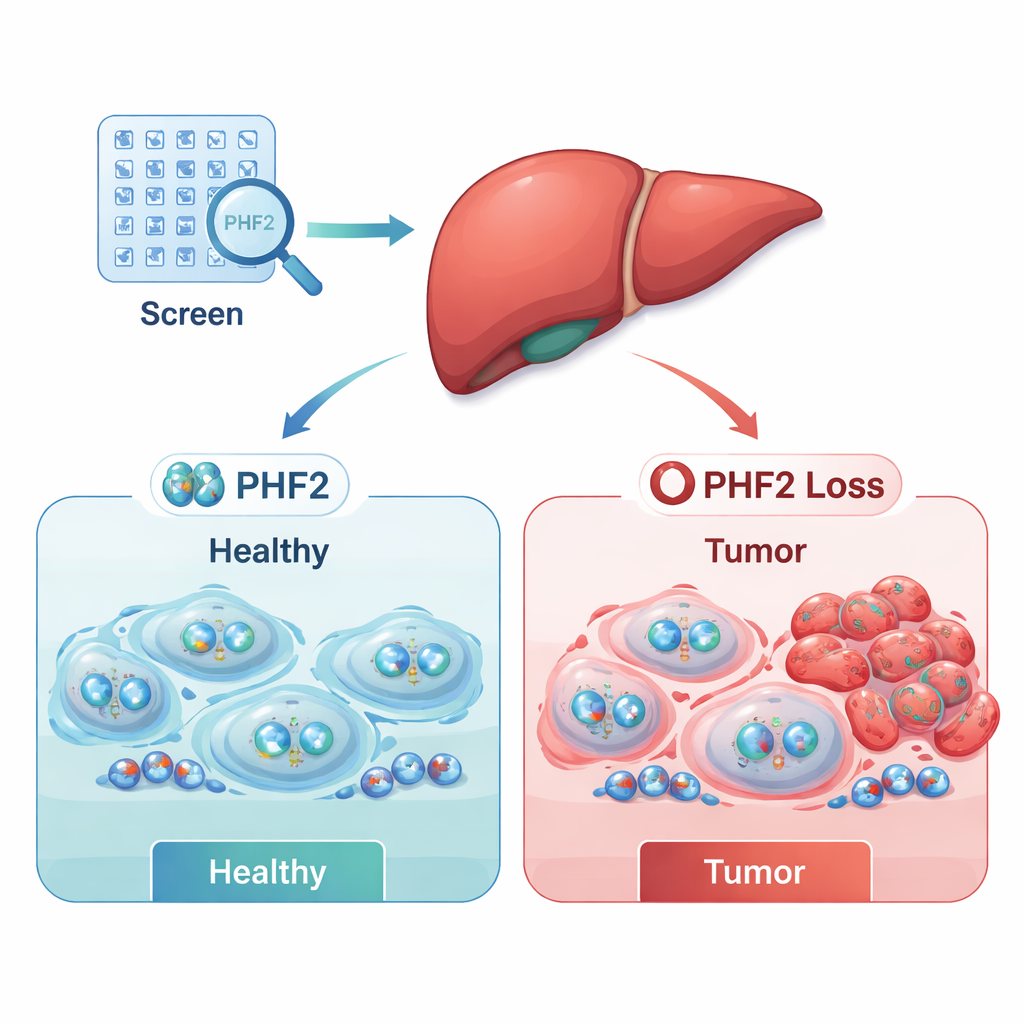
Kanker wordt niet alleen gedreven door kapotte genen; het wordt ook aangedreven door foutieve "epigenetische" controles—de chemische labels en eiwitcomplexen die bepalen welke genen aan- of uitgezet worden. Bij hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, zijn veel van zulke regulatoren verstoord. Het team testte systematisch 497 epigenetische regulatoren in zes leverkankercellijnen, met behulp van RNA-hulpmiddelen om elke regulator tijdelijk te verminderen en vervolgens te meten hoe goed de kankercellen overleefden. Deze grote screening was erop gericht te onthullen op welke regulatoren kankers vertrouwen om te groeien en welke normaal gesproken als remmen van tumorvorming fungeren.
Nieuwe kankerversterkers en -beschermers ontdekken
De screening bracht twee brede groepen aan het licht: potentiële kankerver"snellers" (oncogenen) waarvan verlies de overleving van kankercellen schaadde, en potentiële "remmen" (tumorsuppressoren) waarvan verlies de kankercellen juist beter liet groeien. Door hun laboratoriumgegevens te combineren met grote openbare patiëntdatasets, konden de onderzoekers de lijst terugbrengen tot een paar klinisch relevante kandidaten. Twee regulatoren, SUPT7L en SMARCC1, bleken in tumoren vaak actiever en waren geassocieerd met slechtere overleving. Daarentegen was één regulator—PHF2—vaak minder actief in levertumoren, en patiënten van wie de tumoren hogere PHF2-niveaus behielden, leefden over het algemeen langer. Deze patronen suggereerden dat PHF2 mogelijk als tumorsuppressor fungeert bij menselijke leverkanker.
Hoe verlies van PHF2 leverkankercellen verandert
Om PHF2 grondiger te testen, maakten de onderzoekers leverkankercellen die stabiel minder van dit eiwit produceerden en volgden hun gedrag in de tijd. Cellen met verminderde PHF2 groeiden sneller en vertoonden hogere niveaus van Ki-67, een marker voor actieve celdeling, wat aangeeft dat PHF2 normaal gesproken helpt proliferatie te beperken. Deze effecten waren het sterkst in al agressieve leverkankercellijnen, wat impliceert dat het alleen verlies van PHF2 misschien niet op zichzelf kanker start, maar wel de groei van kwaadaardige cellen kan versnellen zodra tumoren gevormd zijn.
Een verrassende koppeling met de stressverdediging van de cel
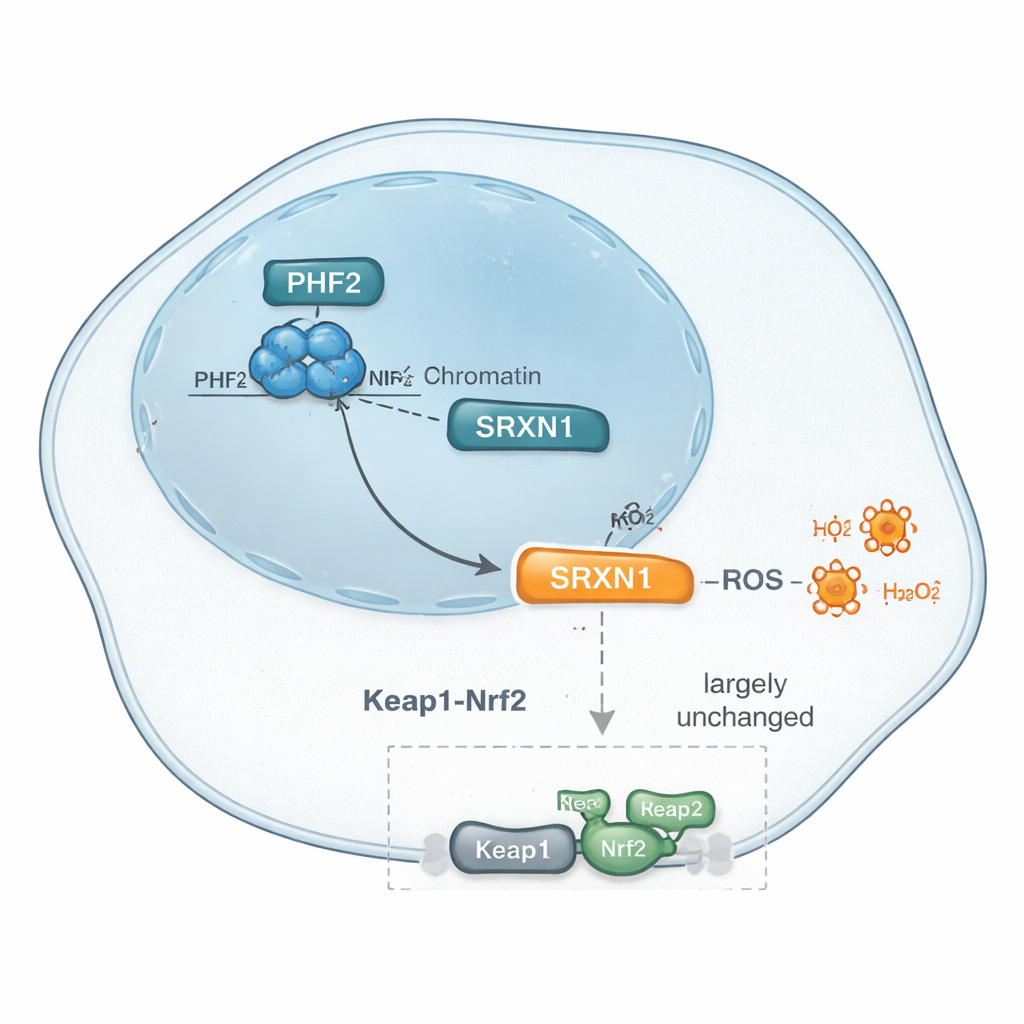
Vervolgens gebruikten de onderzoekers moderne eiwitprofileringstechnieken om duizenden eiwitten te catalogiseren waarvan de niveaus veranderden toen PHF2 werd verminderd. Tussen vele subtiele verschuivingen viel één patroon op: de niveaus van een stressbeschermend eiwit genaamd SRXN1 daalden consequent wanneer PHF2 verloren ging. SRXN1 helpt cellen reactieve zuurstofsoorten te beheersen—chemisch reactieve bijproducten die DNA en eiwitten kunnen beschadigen, maar die kankercellen ook dwingen zich aan te passen. De gegevens suggereerden dat PHF2 helpt SRXN1-niveaus te behouden, en dat het verstoren van dit evenwicht kan beïnvloeden hoe leverkankercellen reageren op interne stress en uiteindelijk hoe snel ze groeien.
Handelen buiten een bekend stresspad
SRXN1 wordt doorgaans gereguleerd door een hoofdschakelaar voor stressrespons genaamd Nrf2, die veel antioxidantgenen activeert wanneer cellen oxidatieve stress ervaren. Omdat SRXN1 daalde wanneer PHF2 werd onderdrukt, vroegen de onderzoekers of PHF2 mogelijk gewoon via dit bekende Nrf2-pad werkt. Ze onderzochten belangrijke Nrf2-gerelateerde genen en eiwitten, behandelden cellen met geneesmiddelen die Nrf2 activeren door zijn remmer Keap1 te blokkeren, en gebruikten genetische hulpmiddelen om Keap1 direct te verminderen. In al deze tests leek de respons van PHF2-deficiënte cellen veel op die van normale cellen, en bredere pathway- en transcriptiefactoranalyses wezen Nrf2 niet aan als hoofdrolspeler. In plaats daarvan kwamen andere factoren, waaronder ZNF384 en Nrf1—beide eerder in verband gebracht met leverkanker—naar voren als kandidaten. Samen suggereren de bewijzen dat PHF2’s controle over SRXN1 en antioxidantresponsen het klassieke Nrf2-signaalvermogen kan omzeilen, wat wijst op een aparte route voor stressregulatie in deze tumoren.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Voor niet-specialisten is de belangrijkste conclusie dat deze studie PHF2 identificeert als een veelbelovende beschermende factor bij leverkanker: wanneer PHF2 aanwezig en actief is, groeien tumorcellen langzamer; wanneer het verminderd is, verkrijgen ze een groeivoordeel en veranderen ze hoe ze omgaat met cellulaire stress. Omdat PHF2 zelf mogelijk moeilijk te remmen of te versterken is met conventionele kleine-molecuulmedicijnen, wijzen de auteurs op opkomende strategieën zoals RNA-gebaseerde therapieën of geneesmiddelen die de activiteit van PHF2 versterken via upstream signaalpartners. Ze benadrukken ook dat de effecten van PHF2 context-afhankelijk zijn—de impact kan variëren met andere mutaties zoals de p53-status—dus elke toekomstige therapie zal waarschijnlijk zorgvuldige patiëntselectie vereisen. Al met al verfijnt het werk ons begrip van hoe epigenetische regulatoren het gedrag van leverkanker vormen en opent het nieuwe wegen voor het ontwerpen van behandelingen die PHF2’s tumorsuppressieve invloed herstellen of nabootsen.
Bronvermelding: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Trefwoorden: hepatocellulair carcinoom, epigenetische regulatie, PHF2, SRXN1, behandeling van leverkanker