Clear Sky Science · nl
TRIM21-gemedieerde afbraak van HILPDA overwint anti‑PD‑1-immunotherapie‑resistentie bij borstkanker door PD‑L1-palmitoylatie te beperken
Waarom sommige kankerimmunotherapieën ophouden te werken
Geneesmiddelen die het immuunsysteem loslaten, zoals anti‑PD‑1-therapieën, hebben de behandeling van meerdere kankers veranderd, waaronder agressieve vormen van borstkanker. Toch reageren veel tumoren nooit of vinden ze na verloop van tijd manieren om te ontsnappen. Deze studie onderzoekt één zo’n ontsnappingsroute bij triple‑negatieve borstkanker en laat zien hoe het herconfigureren van het lipidenmetabolisme van tumoren — en een herbestemd middel genaamd fenretinide — de deur voor het immuunsysteem kan heropenen wanneer standaardimmunotherapie faalt. 
Een verborgen helper die tumoren beschermt
De onderzoekers concentreerden zich op een weinig bekend eiwit genaamd HILPDA, eerder in verband gebracht met hoe cellen vetten verwerken onder stress. Door muizenborstkankers te vergelijken die gevoelig bleven voor anti‑PD‑1‑therapie met tumoren die resistent waren geworden, ontdekten ze dat HILPDA‑niveaus veel hoger waren in de resistente kankers. Analyses van grote patiëntenbanken en tumorbiopten van vrouwen met borstkanker bevestigden dat HILPDA meer voorkomt in tumoren dan in normaal borstweefsel, vooral bij triple‑negatieve ziekte, en dat patiënten van wie de tumoren meer HILPDA tot expressie brengen doorgaans slechter af zijn. Tumoren van mensen die niet profiteerden van PD‑1‑blokkerende middelen hadden ook meer HILPDA, waarmee dit eiwit rechtstreeks aan behandelingsfalen werd gekoppeld.
Hoe tumoren het immuunsysteem tegen ons keren
Om te zien wat HILPDA daadwerkelijk in tumoren doet, manipuleerde het team borstkankercellen zodat ze het eiwit ofwel overproduceren of er juist tekort aan hebben, en kweekte die vervolgens met menselijke immuuncellen of in muizen. Wanneer HILPDA hoog was, trokken tumoren meer regulatorische T‑cellen, myeloïde‑afgeleide onderdrukkende cellen en M2‑achtige macrofagen aan — immuunceltypen die de aanval dempen en kankers helpen zich te verbergen. Tegelijkertijd daalden aantallen en activiteit van dodelijke CD8‑T‑cellen en natural killer‑cellen, en werd hun vermogen om toxische moleculen en ontstekingssignalen af te geven verzwakt. Het stilleggen van HILPDA keerde dit beeld om: tumoren huisvesten minder onderdrukkende cellen, meer actieve dodelijke cellen, groeiden trager en vormden minder uitzaaiingen. Cruciaal was dat, wanneer dieren met lage‑HILPDA‑tumoren anti‑PD‑1‑therapie kregen, hun tumoren meer krimpten en de muizen langer leefden, wat aantoont dat HILPDA bepaalt hoe goed immunotherapie werkt.
Vetproductie, moleculair pantser en immuunontsnapping
Dieper gravend onthulden de wetenschappers hoe HILPDA het tumormetabolisme herschikt om immuunverdedigingen te versterken. Binnen kankercellen hecht HILPDA zich aan een chaperone-eiwit genaamd HSP90 om een transcriptiefactor, KLF5, te stabiliseren die vetproductie aanjaagt. Dit drietal verhoogt de synthese van vetzuren, vooral palmitaat, en vult tumorcellen met lipidedruppels. Eén van deze vetten wordt vervolgens aan PD‑L1 gehecht, het remmende controle‑eiwit op het tumormembraan dat immuuncellen een "val aan te vallen" signaal stuurt. Het team toonde aan dat het toevoegen van palmitaat op een specifieke plaats van PD‑L1 als een moleculaire lijm werkt: het helpt PD‑L1 stabiel in het celmembraan te blijven zitten en voorkomt afbraak. Het muteren van deze enkele aanhechtingsplaats kapte de stabiliteit van PD‑L1 weg en verzwakte zijn vermogen om kankercellen te beschermen, zelfs wanneer HILPDA overvloedig aanwezig was. Met andere woorden, door HILPDA gedreven vetproductie voedt een chemische aanpassing van PD‑L1 die het immuunschild van de tumor van kwetsbaar tot versterkt staal maakt.
De ingebouwde rem die kan worden aangetrokken
Elke accelerator heeft een rem nodig, en hier is de rem een ander eiwit genaamd TRIM21. De auteurs ontdekten dat TRIM21 HILPDA herkent en het markeert met moleculaire "vlaggen" die het naar het afbraaksysteem van de cel sturen. In borsttumoren van patiënten neigden TRIM21‑niveaus laag te zijn wanneer HILPDA hoog was, en lage TRIM21 hing samen met slechtere uitkomsten, wat suggereert dat dit natuurlijke remsysteem vaak verzwakt is in kanker. Het team zocht daarna naar geneesmiddelen die TRIM21 konden versterken en identificeerde fenretinide, een retinoïde die al bij mensen is getest. In cel‑ en diermodellen van triple‑negatieve borstkanker verhoogde fenretinide de TRIM21‑activiteit, versnelde de afbraak van HILPDA, verminderde vet‑synthese en de beschermende modificatie van PD‑L1, en vertraagde tumorgroei en -uitzaaiing. Het meest opvallend was dat de combinatie van fenretinide met anti‑PD‑1‑therapie tumoren gevoeliger maakte voor immuunaanvallen, met een toename van dodelijke T‑ en natural killer‑cellen en een afname van onderdrukkende cellen in het tumormicro‑milieu. 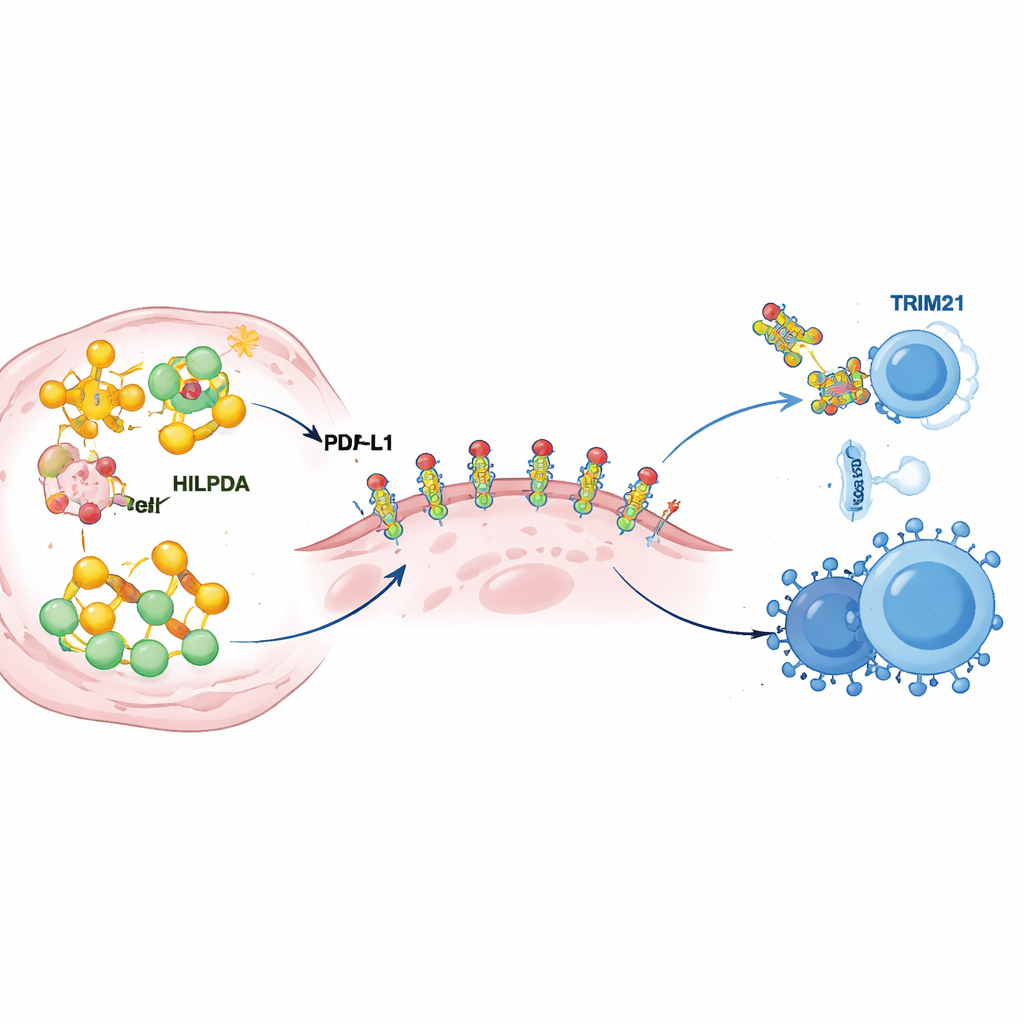
Wat dit betekent voor de toekomst van kankerzorg
Dit werk onthult een keten van gebeurtenissen waarbij gestreste borstkankercellen HILPDA omhoogschakelen, vetproductie opvoeren en PD‑L1 chemisch versterken op hun oppervlak, waardoor ze immuuncellen blijven onderdrukken zelfs bij PD‑1‑blokkerende middelen. TRIM21 fungeert als een interne waarborg die HILPDA kan afbreken, maar is in tumoren vaak te zwak. Door aan te tonen dat fenretinide deze waarborg kan reactiveren, wijst de studie op een praktische manier om een metabolisch middel te combineren met bestaande immunotherapie om resistentie te overwinnen. Als dit wordt bevestigd in klinische onderzoeken, zou het richten op de TRIM21–HILPDA–PD‑L1‑as patiënten met moeilijk behandelbare triple‑negatieve borstkanker een tweede kans kunnen geven om te profiteren van immuun-gebaseerde behandelingen.
Bronvermelding: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Trefwoorden: triple-negatieve borstkanker, resistentie tegen immunotherapie, PD-L1-palmitoylatie, tumor lipidenmetabolisme, fenretinide