Clear Sky Science · nl
Cereblon (CRBN) remt uitzaaiing van prostaatkanker door negatieve regulatie van 6‑fosfogluconaatdehydrogenase (6PGD)
Waarom dit onderzoek ertoe doet
Wanneer prostaatkanker vanuit de prostaat naar andere organen uitzaait, wordt de behandeling veel moeilijker en is de ziekte vaak dodelijk. Deze studie laat zien hoe een weinig bekend cellulair ‘kwaliteitscontrolemolecuul’, cereblon (CRBN), helpt voorkomen dat prostaatkanker uitzaait door een metabool enzym dat agressief gedrag aanwakkert, te ontmantelen. Het begrip van dit ingebouwde remsysteem opent nieuwe mogelijkheden om uitzaaiing te vertragen of te stoppen, vooral bij moeilijk behandelbare vormen van de ziekte.
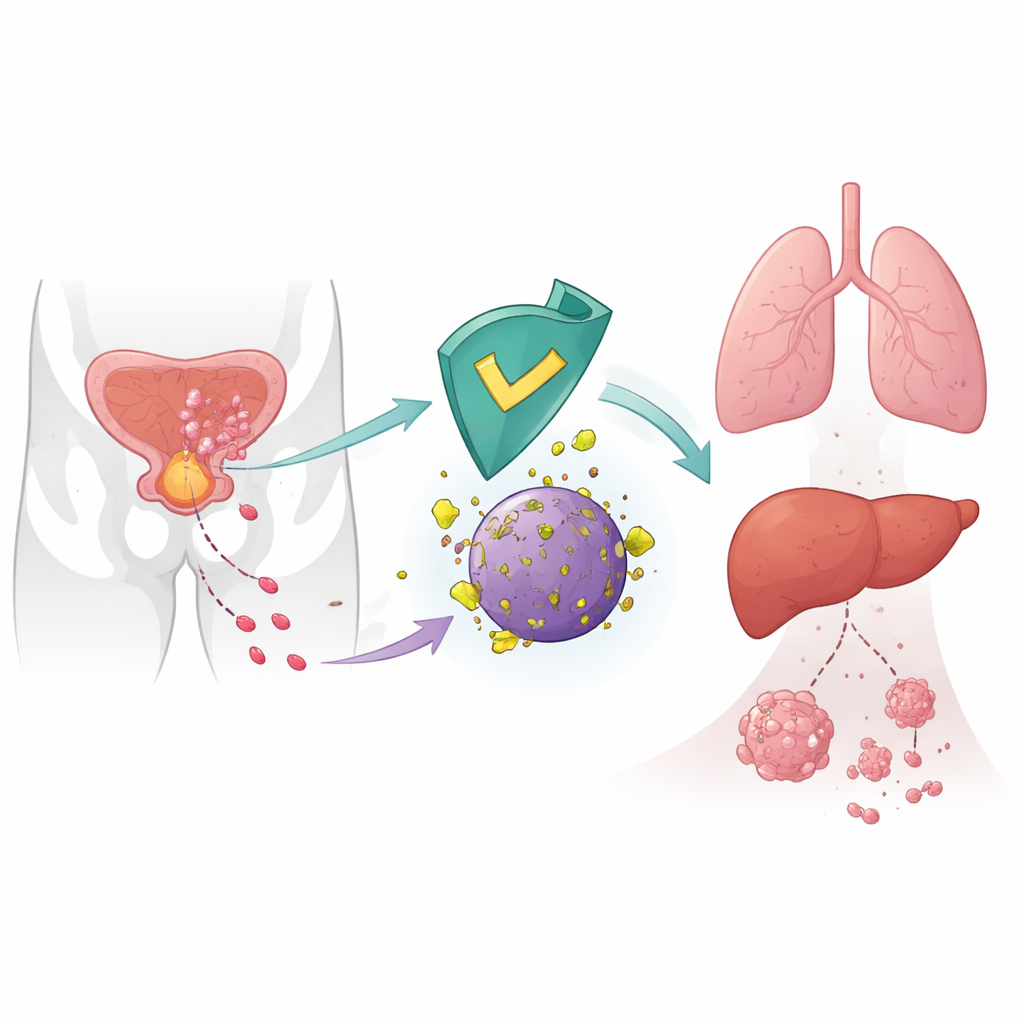
Een interne rem op kankeruitzaaiing
Kankercellen zaaien niet willekeurig uit; ze herschikken hun interne machinerie om te bewegen, binnen te dringen en afgelegen organen te koloniseren. De auteurs richtten zich op CRBN, een eiwit dat vooral bekend is als doelwit van geneesmiddelen zoals thalidomide die in bloedkankers worden gebruikt. In gezonde cellen maakt CRBN deel uit van een moleculaire afvalmachine die bepaalde eiwitten markeert voor afbraak. Eerder onderzoek suggereerde dat lage CRBN‑niveaus in tumoren geassocieerd zijn met slechtere uitkomsten, maar de directe rol in uitzaaiing was onduidelijk. Hier tonen de onderzoekers aan dat CRBN fungeert als een natuurlijke onderdrukker van prostaatkankeruitzaaiing door het metabole enzym 6‑fosfogluconaatdehydrogenase (6PGD) te richten op afbraak.
Een metabole motor die kanker kaapt
6PGD bevindt zich in een metabole route die bekendstaat als de oxidatieve pentosefosfaatroute, die cellen helpt NADPH te genereren — een molecuul dat zowel bouwstoffen als anti‑oxidatieve kracht levert. Veel tumoren zetten deze route hoger om sneller te groeien en stress te weerstaan. Het team vond dat prostaatkankermonsters van patiënten doorgaans minder CRBN en meer 6PGD bevatten dan normaal prostaatweefsel, en dat deze onbalans vooral uitgesproken is bij agressieve ziekte. In prostaatkankercellijnen leidde het terugschakelen van CRBN of het afbreken ervan met een ontworpen verbinding tot hogere 6PGD‑eiwitniveaus en enzymactiviteit, wat NADPH versterkte. Het herstellen van CRBN had het tegenovergestelde effect: 6PGD en NADPH daalden zonder dat het onderliggende 6PGD‑genbericht veranderde, wat wijst op regulatie op eiwitniveau.
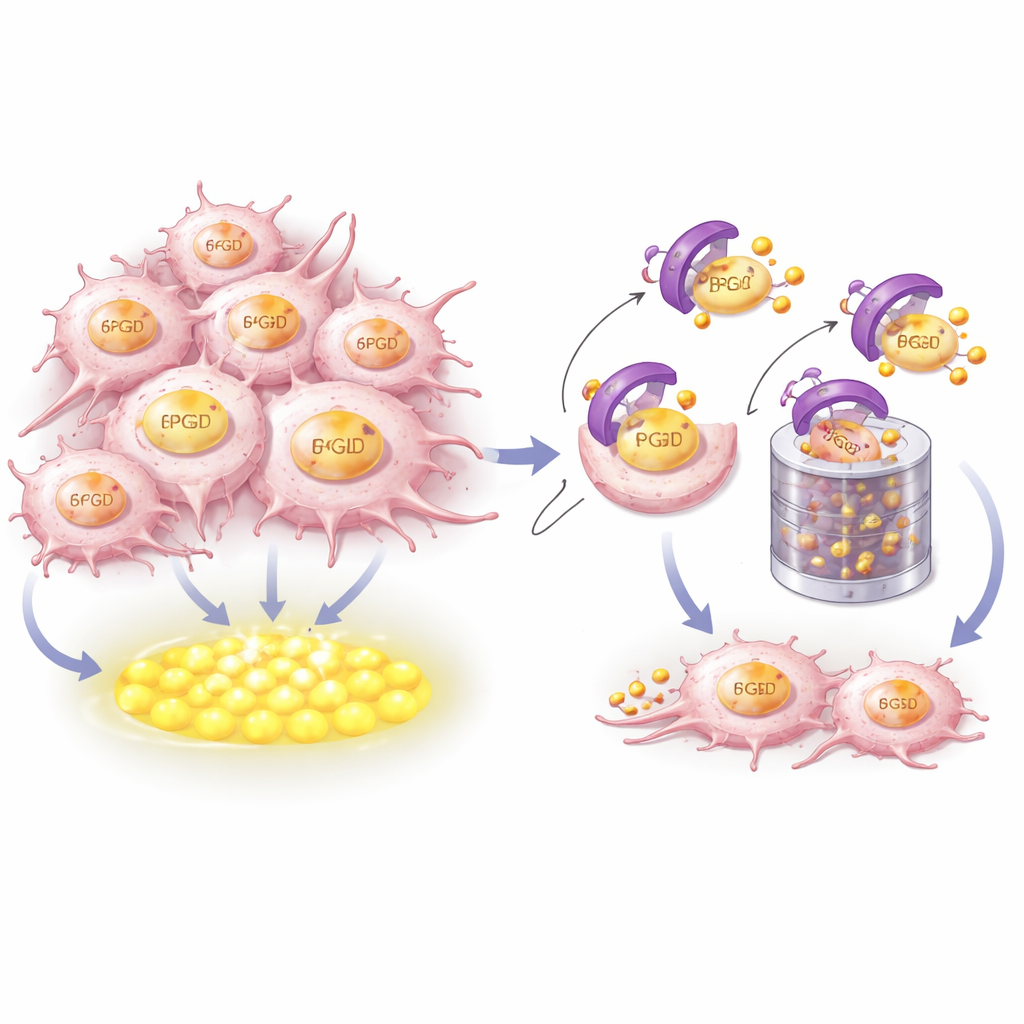
Hoe CRBN de brandstof herkent en vernietigt
Om te begrijpen hoe CRBN 6PGD controleert, combineerden de onderzoekers structurele modellering met biochemische experimenten. Ze lieten zien dat CRBN fysiek een korte, sterk geconserveerde helicale sectie nabij de staart van 6PGD vastgrijpt. Belangrijke aminozuren op beide eiwitten vormen een nauw aansluitend dockingsvlak. Wanneer deze contactpunten werden veranderd, kon CRBN niet langer aan 6PGD binden, de kleine ubiquitine‑labels aanbrengen die het markeren voor afbraak, of het afleveren bij de cellulair versnipperaar, het proteasoom. Opmerkelijk is dat dit herkenningsoppervlak gescheiden is van het pocket waar immuunmodulerende geneesmiddelen aan CRBN binden, wat betekent dat CRBN’s controle over 6PGD deel uitmaakt van zijn oorspronkelijke huishoudelijke functie en niet het gevolg is van een geneesmiddelgeïnduceerd effect.
Van veranderd metabolisme naar rondzwervende cellen
De gevolgen van deze moleculaire handdruk manifesteren zich in het gedrag van cellen. In prostaatkankercellen zonder CRBN gingen verhoogde 6PGD en NADPH gepaard met meer beweging en invasie door kunstmatige barrières — kenmerken van metastatische potentie. Wanneer CRBN werd overgeproduceerd, werden cellen minder mobiel en invasief, hoewel hun groeisnelheid niet veranderde. Profilering van genactiviteit toonde aan dat CRBN de niveaus van CDH1 verhoogde, geassocieerd met dicht opeengepakte epitheelcellen, en de niveaus van MMP1 verlaagde, gekoppeld aan weefselafbraak en migratie. Belangrijk is dat deze verschuivingen directe CRBN–6PGD‑binding vereisten en omkeerbaar waren door de enzymactiviteit van 6PGD te blokkeren, waarmee veranderingen in metabolisme werden verbonden met veranderingen in metastatisch gedrag.
Bewijs uit diermodellen en andere kankers
Het team testte deze ideeën in muizen door prostaatkankercellen in de bloedbaan of milt te injecteren. Cellen die waren aangepast om extra CRBN te produceren vormden veel minder metastatische knobbeltjes in lever en longen dan controlecellen, wat een anti‑metastatische rol in levende dieren bevestigt. Muizen zonder CRBN toonden hogere 6PGD‑eiwitniveaus in meerdere organen. Vergelijkbare patronen verschenen in glioblastoom-, long‑ en nierkankercellijnen: het verwijderen van CRBN verhoogde 6PGD en versterkte celbeweging en invasie, terwijl genetische of geneesmiddelgemedieerde remming van 6PGD dit agressieve gedrag afremde. Deze waarnemingen suggereren dat de CRBN–6PGD‑rem op uitzaaiing niet uniek is voor prostaatkanker.
Wat dit kan betekenen voor toekomstige behandelingen
Al met al stelt de studie dat CRBN fungeert als een metabole poortwachter die de energietoevoer beperkt die kankercellen nodig hebben om losser te raken, te migreren en nieuwe tumoren te zaaien. Wanneer CRBN verloren gaat of laag is, stapelt 6PGD zich op, stijgt de NADPH‑productie en zijn cellen eerder geneigd veranderingen te ondergaan die uitzaaiing bevorderen. Voor patiënten wijst dit op twee mogelijkheden: het meten van CRBN‑ en 6PGD‑niveaus kan helpen tumoren met een hoog uitzaaiingsrisico te signaleren, en therapieën die CRBN‑functie versterken — of selectief 6PGD dempen in CRBN‑arme tumoren — kunnen nieuwe manieren bieden om de verspreiding van prostaat- en andere kankers te vertragen of te voorkomen.
Bronvermelding: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Trefwoorden: uitzaaiing van prostaatkanker, kankermetabolisme, cereblon, 6PGD‑enzym, NADPH‑route