Clear Sky Science · nl
L1TD1 bevordert de progressie van mucineuze colorectale adenocarcinoom door de stabiliteit van ABCC3-mRNA te vergroten
Waarom deze slijmrijke kanker ertoe doet
Colorectale kanker is wereldwijd een van de belangrijkste oorzaken van kankersterfte. Binnen deze ziekte valt een subtype op dat mucineus adenocarcinoom wordt genoemd, omdat de tumoren gevuld zijn met dik slijm dat meer dan de helft van de tumormassa kan uitmaken. Die slijmlaag kan kankercellen helpen zich te verbergen voor chemotherapie en de afweer van het lichaam. Deze studie stelt een fundamentele maar cruciale vraag: wat regelt al dat slijm, en kunnen we het stilleggen om de tumorgroei te vertragen en behandelingen effectiever te maken?
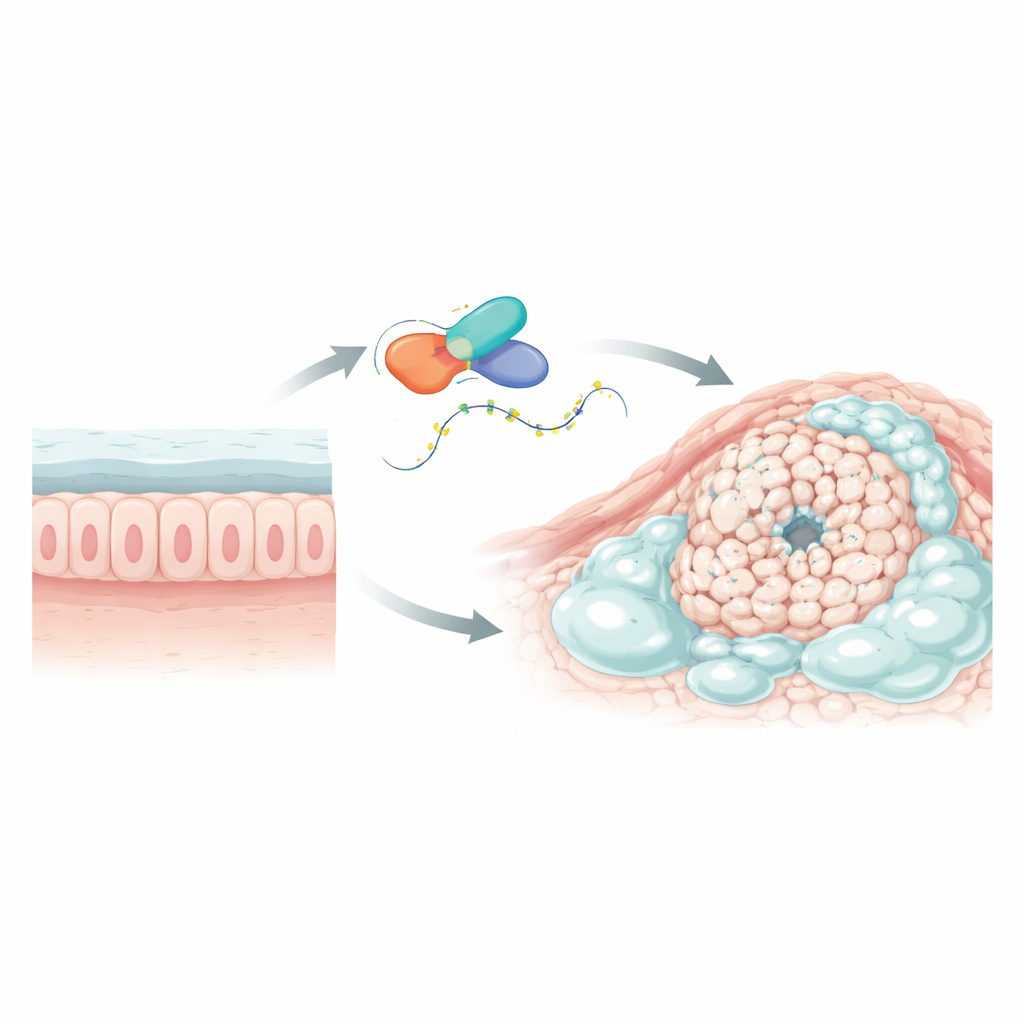
Het vinden van een sleutelgen dat problemen veroorzaakt
De onderzoekers doorzochten eerst grote kankerdatabases en single-cell-sequencinggegevens om genen te identificeren die anders reageren in slijmrijke colorectale tumoren vergeleken met gewone colorectale kankers en het omliggende gezonde weefsel. Één gen, L1TD1 genaamd, sprong er duidelijk uit. Het was sterk verhoogd in mucineuze tumoren maar niet in reguliere tumoren en was hoger in tumorweefsel dan in het aangrenzende normale colon. L1TD1 codeert voor een eiwit dat aan RNA bindt, het molecuul dat genetische boodschappen van DNA naar het eiwitmakende apparaat van de cel draagt. Omdat RNA-bindende eiwitten nauwkeurig kunnen regelen hoe lang boodschappen blijven bestaan en hoe sterk ze worden afgelezen, was L1TD1 een sterke kandidaat om als masterregulator te fungeren in deze slijmrijke kankers.
Hoe L1TD1 de groei en uitzaaiing van kanker bevordert
Om te testen wat L1TD1 daadwerkelijk doet, gebruikte het team colonkankercellijnen en muismodellen. Toen ze de hoeveelheid L1TD1 in kankercellen verhoogden, deelden de cellen sneller, bewogen ze gemakkelijker en drongen ze agressiever door door weefselachtige barrières. Het terugdraaien van L1TD1 had het tegengestelde effect: de groei vertraagde en de invasie nam af. In muizen die waren geïnjecteerd met cellen met hoge L1TD1-niveaus, werden tumoren groter en verspreidden ze zich vaker naar de lever en de buikholte. Tumoren met meer L1TD1 bleken ook vaak groter, minder goed gedifferentieerd en in een meer gevorderd stadium bij patiënten, wat dit gen koppelt aan ernstiger ziektegedrag in de kliniek.
Het inschakelen van slijmproductie en medicijnresistentie
Slijm zelf bleek centraal te staan in de effecten van L1TD1. Cellen met meer L1TD1 produceerden hogere hoeveelheden belangrijke slijmvormende eiwitten, vooral MUC2 en MUC5AC, en vertoonden kenmerken van gobletcellen, de normale slijmproducerende cellen van de darm. 3D-culturen en weefselkleuringen van zowel patiënten als muizen bevestigden dat hogere L1TD1 samenhing met dikkere en overvloediger slijmlaag. Belangrijker nog, dit slijm was niet slechts bijzaak. Toen de onderzoekers selectief MUC2 verminderden, verdwenen de extra groei-, invasie- en chemotherapie-resistentie-effecten die door L1TD1 werden veroorzaakt grotendeels. Cellijnen met veel L1TD1 waren moeilijker te doden met het veelgebruikte middel oxaliplatin, en tumoren met deze cellen krompen minder in behandelde muizen, wat het slijm onderstreept als een schild dat L1TD1 helpt opbouwen.
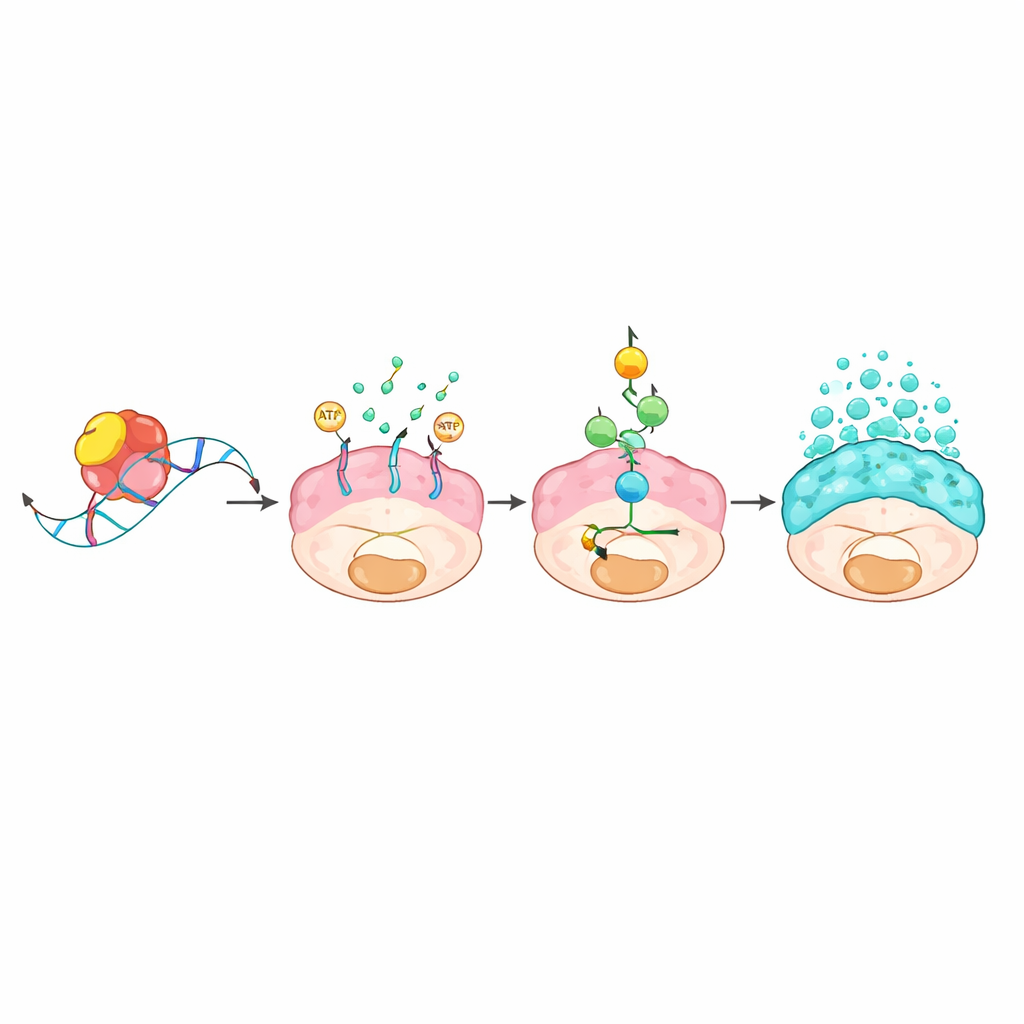
Een moleculaire keten die RNA-regulatie koppelt aan slijmovervloed
Het team vroeg zich vervolgens af hoe een RNA-bindend eiwit zulke dramatische veranderingen kon veroorzaken. Door RNA-moleculen die fysiek aan L1TD1 gebonden waren op te vissen en genactiviteit te vergelijken met en zonder L1TD1, identificeerden ze een transportergen genaamd ABCC3 als een belangrijk doelwit. L1TD1 hechtte zich aan een kort „GUGU”-motief in het staartgedeelte van het ABCC3-RNA-bericht en stabiliseerde het, waardoor de cel meer van het ABCC3-eiwit maakte, bekend als MRP3. Deze transporter bevindt zich in het celmembraan en verbruikt energie om stoffen uit de cel te pompen. De resulterende energietekorten activeerden een metabool alarmsysteem rond de sensor AMPK, die op zijn beurt een klassieke groeien stressroute bekend als MAPK inschakelde. Eenmaal geactiveerd verhoogde deze cascade de productie en afgifte van slijmeiwitten en versterkte ze het vermogen van kankercellen om te groeien, te migreren en bestand te zijn tegen geneesmiddelen. Het genetisch blokkeren van ABCC3 of het remmen met een experimentele verbinding, evenals het remmen van de MAPK-route, verminderde alle het slijmproductie en verzwakte de tumoren.
Wat dit betekent voor patiënten
Samengevoegd onthult het werk een stapsgewijs controlesysteem voor slijmrijke colorectale kanker: L1TD1 stabiliseert ABCC3-RNA, ABCC3 put cellulaire energie uit, het AMPK–MAPK-pad wordt geactiveerd, en de tumor reageert door overmatige slijmproductie en door agressiever en geneesmiddelenresistenter te worden. Voor patiënten suggereert dit meerdere veelbelovende invalshoeken. L1TD1- en ABCC3-niveaus zouden kunnen helpen tumoren te identificeren die waarschijnlijk agressief zijn of resistent tegen standaardchemotherapie. Belangrijker nog, geneesmiddelen die de L1TD1–ABCC3-interactie verstoren, de pompactiviteit van MRP3 blokkeren of de downstream signaalroute targeten, zouden de slijmlaag kunnen verminderen, tumorgroei kunnen vertragen en bestaande behandelingen effectiever kunnen maken voor deze uitdagende vorm van colorectale kanker.
Bronvermelding: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Trefwoorden: mucineus colorectaal kanker, L1TD1, ABCC3 MRP3, mucineproductie, chemoresistentie