Clear Sky Science · nl
De multifunctionele RNA-helicase DDX39A stimuleert glioblastoomprogressie door alternatieve splicing van WISP1 te moduleren, wat een immunosuppressieve macrofaagpolarizatie induceert
Waarom deze studie over hersenkanker belangrijk is
Glioblastoom is een van de dodelijkste vormen van hersenkanker, berucht vanwege terugkeer na behandeling en weerstand tegen geneesmiddelen. Deze studie onthult hoe een enkele moleculaire "schakelaar" in tumorcellen niet alleen de groei van de kanker bevordert, maar ook omliggende immuuncellen ertoe brengt hun aanval te staken en de tumor te beschermen. Door deze keten van gebeurtenissen terug te volgen, identificeren de onderzoekers ook een bestaand antipsychoticum dat mogelijk kan worden hergebruikt om dit schadelijke netwerk te doorbreken.
Een belangrijke helper binnen hersentumorcellen
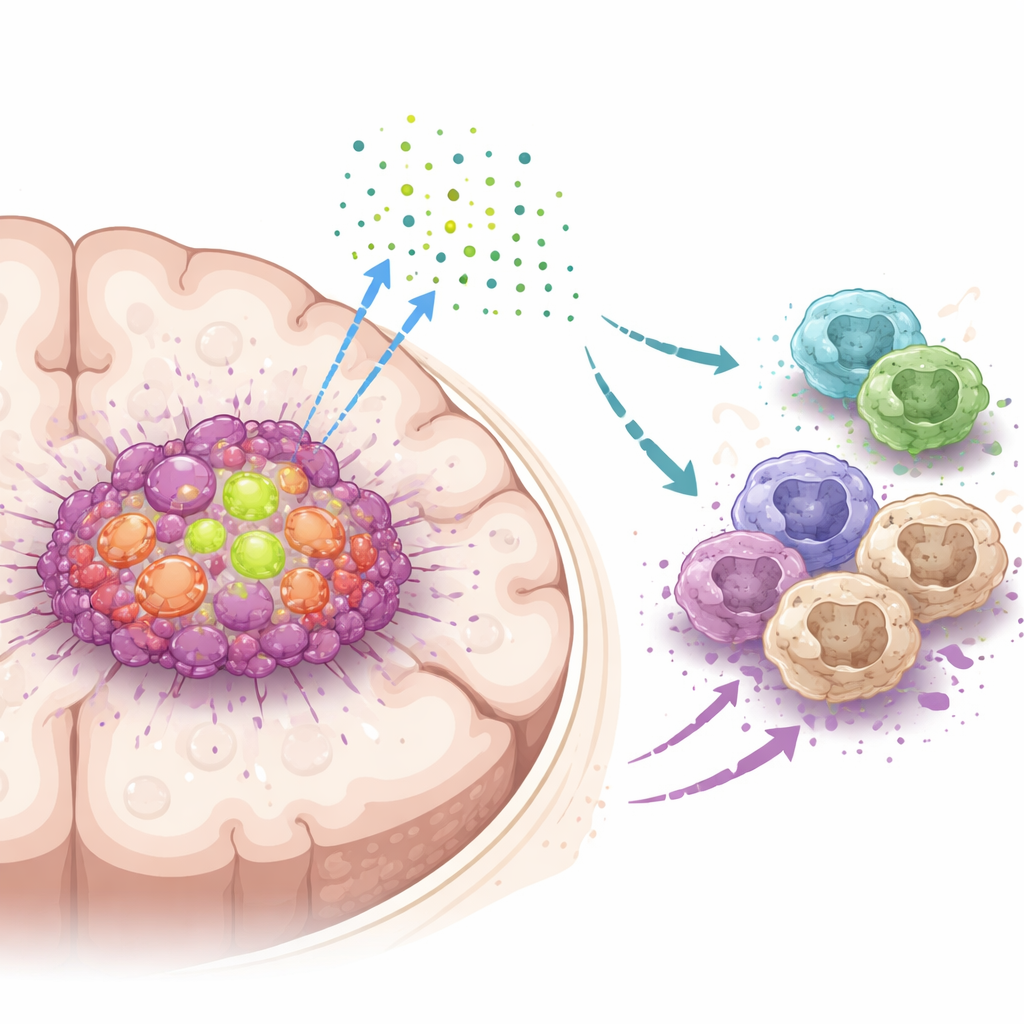
Het team richtte zich op een eiwit genaamd DDX39A, een moleculaire machine die cellen helpt RNA te verwerken, de werkende kopie van genetische informatie. Door grote patiëntendatasets en tumormonsters te analyseren, vonden ze dat DDX39A veel actiever is in glioblastoom dan in normaal hersenweefsel, en dat de niveaus toenemen met het tumorniveau. Enkelcelanalyses toonden aan dat DDX39A vooral overvloedig is in snel delende tumorcellen en in bepaalde immuuncellen die macrofagen worden genoemd binnen de tumormassa. Patiënten met tumoren die meer DDX39A toonden, hadden doorgaans slechtere uitkomsten, wat suggereert dat dit eiwit nauw verbonden is met agressieve ziekte.
Hoe deze helper groei en verspreiding aanjaagt
Om te testen wat DDX39A daadwerkelijk doet, gebruikten de onderzoekers genetische technieken om de expressie ervan te verlagen in glioblastoom-stamachtige cellen die in het laboratorium werden gekweekt en in muismodellen van hersentumoren. Wanneer DDX39A werd verminderd, groeiden tumorcellen langzamer, drongen ze minder effectief omliggend weefsel binnen en waren ze gevoeliger voor geprogrammeerde celdood. De kankerstamachtige cellen verloren ook veel van hun vermogen om nieuwe tumorsferen te vormen, een teken dat hun zelfvernieuwingscapaciteit was aangetast. Bij muizen waren tumoren met verlaagd DDX39A kleiner en leefden de dieren langer, wat bevestigt dat dit eiwit actief tumorprogressie aanstuurt en niet slechts een passieve marker is.
Een geheim signaal dat immuunverdedigers ontwapent
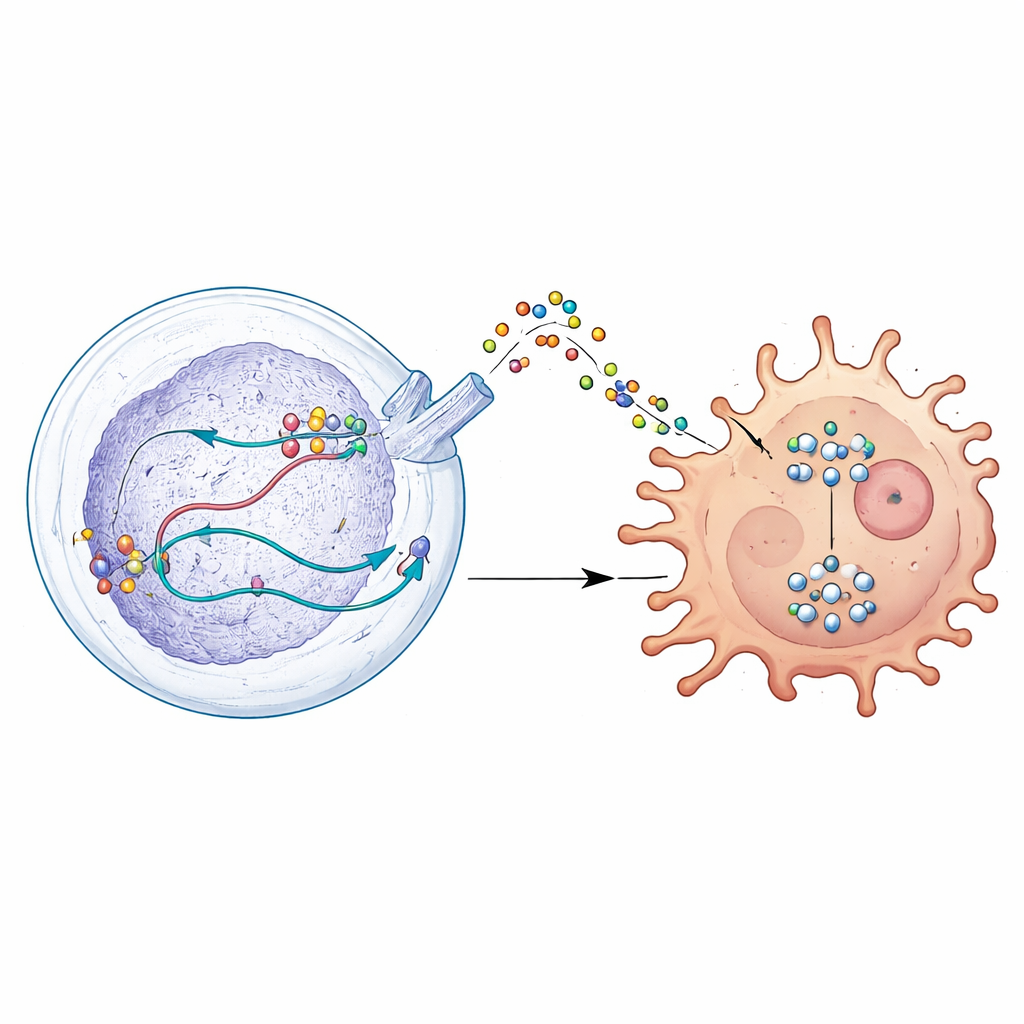
Verder onderzoek liet zien dat DDX39A verandert hoe een gen genaamd WISP1 wordt verwerkt. In plaats van WISP1 simpelweg aan of uit te zetten, helpt DDX39A de RNA-bewerking zodanig te vormen dat het bericht wordt gestabiliseerd en de productie van het WISP1-eiwit toeneemt. Tumorcellen geven vervolgens WISP1 af in hun omgeving, waar het fungeert als een misleidend signaal. Omliggende macrofagen, die tumoren kunnen aanvallen of ondersteunen, reageren op dit signaal door over te schakelen naar een immunosuppressieve, tumorbevorderende staat. Deze omschakeling wordt aangedreven door activatie van een groeiregulerend pad binnen cellen dat bekendstaat als AKT. Wanneer DDX39A of WISP1 werd gereduceerd, werd dit pad stilgelegd, werden tumorcellen minder agressief en keerden macrofagen terug naar een meer tumorbestrijdend profiel.
Een psychiatrisch middel omvormen tot een wapen tegen kanker
Gewapend met deze routeschema's doorzochten de onderzoekers medicijnendatabases op moleculen die de activiteit van DDX39A zouden kunnen verstoren. Ze richtten zich op fluphenazine, een langgebruikt antipsychoticum dat bekendstaat om zijn vermogen de hersenen te bereiken. Computermodellering en bindingsproeven toonden aan dat fluphenazine direct aan DDX39A kan binden. In tumorcellen verzwakte het medicijn de binding van DDX39A aan WISP1-RNA, verlaagde het WISP1-niveaus en remde het AKT-signaal. Behandelde cellen deelden minder, drongen minder binnen, vormden minder tumorsferen en waren gevoeliger voor celdood. In muismodellen vertraagde fluphenazine de groei van hersentumoren, verminderde het aantal tumorondersteunende macrofagen en verlengde het overleven, en dat alles bij doses vergelijkbaar met die al bij mensen voor andere aandoeningen worden gebruikt.
Wat dit betekent voor toekomstige behandelingen
In gewone bewoordingen laat deze studie zien dat glioblastoomcellen DDX39A uitbuiten om een boodschap (WISP1) fijn te stellen die zowel hun eigen veerkracht vergroot als omliggende immuuncellen herprogrammeert tot lijfwachten in plaats van strijders. Het blokkeren van deze helper, ofwel genetisch of met een middel zoals fluphenazine, verzwakt de kanker op twee fronten: de tumorcellen zelf en het beschermende schild van immunosuppressieve macrofagen. Hoewel veel extra onderzoek nodig is voordat deze strategie patiënten kan bereiken, opent het werk een veelbelovende weg om een bekend medicijn te hergebruiken en een nieuw ontdekt zwak punt in een van de meest hardnekkige hersenkankers te raken.
Bronvermelding: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Trefwoorden: glioblastoom, RNA-splicing, tumormicro-omgeving, macrofaagpolarizatie, hergebruik van geneesmiddelen