Clear Sky Science · nl
PMM2 interacteert met TRIM28 om E2F4 te rekruteren en KIFC3-gemedieerde tumorglycolyse en colorectale kankervordering te bevorderen
Waarom dit kankerverhaal ertoe doet
Colorectale kanker is een van de dodelijkste vormen van kanker wereldwijd, deels omdat veel tumoren leren de energievoorziening van het lichaam te kapen om ongecontroleerde groei aan te jagen. Deze studie onthult hoe een nauwelijks bekende enzym, PMM2, colorectale tumoren helpt suiker agressiever te verbranden en uit te zaaien, en waarom dat het tot een veelbelovend nieuw doelwit voor toekomstige geneesmiddelen en diagnostische tests maakt.
Een suikergierige tumormotor
Kankercellen herbedraden vaak hun gebruik van glucose en geven de voorkeur aan een snelle, weinig efficiënte vorm van suikerverbranding die bekendstaat als glycolyse. De onderzoekers begonnen met het vergelijken van duizenden genen in colorectale tumormonsters met nabijgelegen gezond weefsel. PMM2, een enzym dat normaal gesproken betrokken is bij het koppelen van suikerketens aan eiwitten, viel op als een van de sterkst verhoogde genen in kanker. Tumorcellen met extra PMM2 groeiden sneller, vormden meer kolonies en verspreidden zich gemakkelijker in kweekschalen, terwijl cellen waarin PMM2 was uitgeschakeld langzamer groeiden, minder migreerden en gevoeliger waren voor celdood.
Hoe tumorcellen suikergebruik superladen
Toen het team PMM2-niveaus in colorectale kankercellen verlaagde, namen de cellen minder glucose op, produceerden ze minder ATP (hun belangrijkste energievaluta) en scheidden ze minder lactaat uit, het afvalproduct van glycolyse. Gevoelige metabole metingen bevestigden dat de algehele verzuring van het omliggende medium daalde, terwijl zuurstofgebruik toenam, wat betekent dat de cellen verschoven van turbo-glycolyse naar meer normale ademhaling. Belangrijke glycolyse-hulp-eiwitten, PKM2 en LDHA, namen ook af. Verrassend genoeg kon zelfs een katalytisch "dode" versie van PMM2 dit suikergierige gedrag nog steeds stimuleren, wat aantoont dat de rol van het enzym in kanker niet afhangt van zijn gebruikelijke chemische activiteit, maar van de partners waaraan het zich binnen de cel bindt.
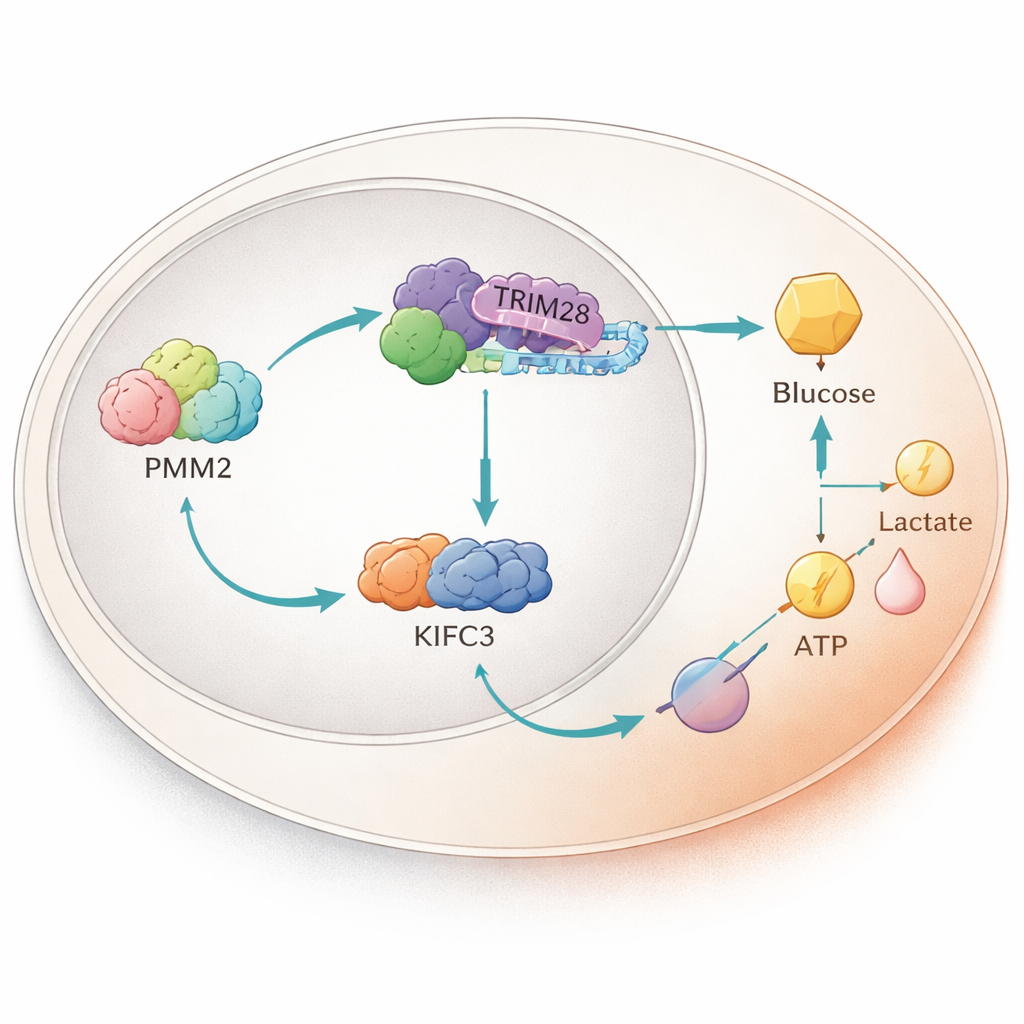
Een eiwit-estafette binnen de kern
Dieper onderzoek toonde aan dat PMM2 fysiek bindt aan een ander eiwit genaamd TRIM28, dat de celkern kan binnengaan en genactiviteit kan beïnvloeden. PMM2 helpt TRIM28 zich in de kern op te hopen, waar TRIM28 samenwerkt met een transcriptiefactor, E2F4. Gezamenlijk versterken deze drie de productie van een motorproteïne genaamd KIFC3 door te binden aan een specifiek stuk van de DNA-regioregeling ervan. Experimenten die het PMM2-deel dat nodig is voor TRIM28-binding verwijderden, haalden PMM2’s vermogen om glycolyse en celgroei op te voeren weg, wat benadrukt dat deze eiwitpartnerschap — niet de klassieke enzymfunctie van PMM2 — de tumorvoorsprong aandrijft.
Een belangrijke metabole schakelaar hoger zetten
KIFC3, beter bekend om zijn rol bij het transporteren van lading langs het intracellulaire ‘skelet’, bleek een cruciale metabole schakelaar te zijn. Toen de onderzoekers KIFC3-niveaus verlaagden, consumeerden colorectale kankercellen minder glucose, produceerden ze minder ATP en lactaat en vertoonden ze zwakkere glycolytische activiteit, terwijl hun zuurstofgebruik toenam. Belangrijk is dat het stilleggen van KIFC3 de glycolyseboost en het groeivoordeel dat normaal door PMM2 wordt veroorzaakt, gedeeltelijk tenietdeed. In muizen waarin menselijke colorectale kankercellen waren geïmplanteerd, groeiden tumoren met extra PMM2 groter, maar dit effect werd afgezwakt wanneer KIFC3 werd gereduceerd. Tumormonsters van deze dieren toonden hogere niveaus van PMM2, KIFC3 en glycolysemarkers, waarmee de hele keten van gebeurtenissen ook in levend weefsel werd bevestigd.
Van laboratoriummodellen naar patiëntmonsters
Om het werk dichter bij de kliniek te brengen, creëerde het team minuscule driedimensionale tumoren, organoïden genoemd, uit patiënt-colorectale kankers. Organoïden met hogere PMM2- en KIFC3-niveaus groeiden sneller en produceerden meer ATP en lactaat dan die met lagere niveaus. Het geforceerd verhogen van PMM2 in organoïden verhoogde KIFC3 en glycolyse, terwijl het verlagen van PMM2 het omgekeerde effect had. Analyses van patiëntentumorarrays toonden bovendien aan dat hoge PMM2-niveaus geassocieerd waren met gevorderdere ziekte, uitzaaiing naar lymfeklieren en kortere algehele overleving, waarmee PMM2 naar voren komt als een sterke kandidaat-biomarker.
Wat dit betekent voor toekomstige zorg
In eenvoudige bewoordingen toont deze studie aan dat veel colorectale tumoren PMM2 lijken in te schakelen in een nucleaire eiwit-estafette — via TRIM28 en E2F4 — om KIFC3 en daarmee hun suikerverbrandingsmachinerie op te voeren. Die metabolische opleving helpt kankers groeien en zich te verspreiden. Omdat deze route afhankelijk is van eiwitinteracties in plaats van de gebruikelijke enzymfunctie van PMM2, opent dat nieuwe wegen voor therapie: kleine moleculen, peptiden of degrader-geneesmiddelen die de binding van PMM2 aan TRIM28 verstoren, E2F4’s toegang tot DNA blokkeren of KIFC3-activiteit dempen, zouden in principe tumoren van hun favoriete brandstof kunnen beroven. Hoewel dergelijke behandelingen nog niet beschikbaar zijn, komt de PMM2–TRIM28–E2F4–KIFC3-keten nu naar voren als een veelbelovende routekaart voor meer gerichte en op metabolisme gerichte strategieën tegen colorectale kanker.
Bronvermelding: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Trefwoorden: colorectale kanker, tumormetabolisme, glycolyse, oncogene signalering, biomarker