Clear Sky Science · nl
ULK1 bevordert metastatische progressie in experimentele modellen van epitheliale eierstokkanker
Waarom dit onderzoek ertoe doet
Epitheliale eierstokkanker wordt vaak pas ontdekt nadat ze zich geruisloos door de buikholte heeft verspreid, waardoor het een van de dodelijkste vormen van kanker bij vrouwen is. Een belangrijk stadium in die verspreiding is de vorming van kleine klompjes tumorcellen, zogenoemde sferoïden, die in buikvocht zweven, chemotherapie overleven en nieuwe tumoren zaaien. Deze studie stelt een gerichte vraag met grote implicaties: helpt een cellulaire "overlevingsschakelaar" genaamd ULK1 deze klompjes te laten volhouden en verspreiden, en zou het uitschakelen ervan nieuwe behandelopties voor gevorderde eierstokkanker kunnen openen?
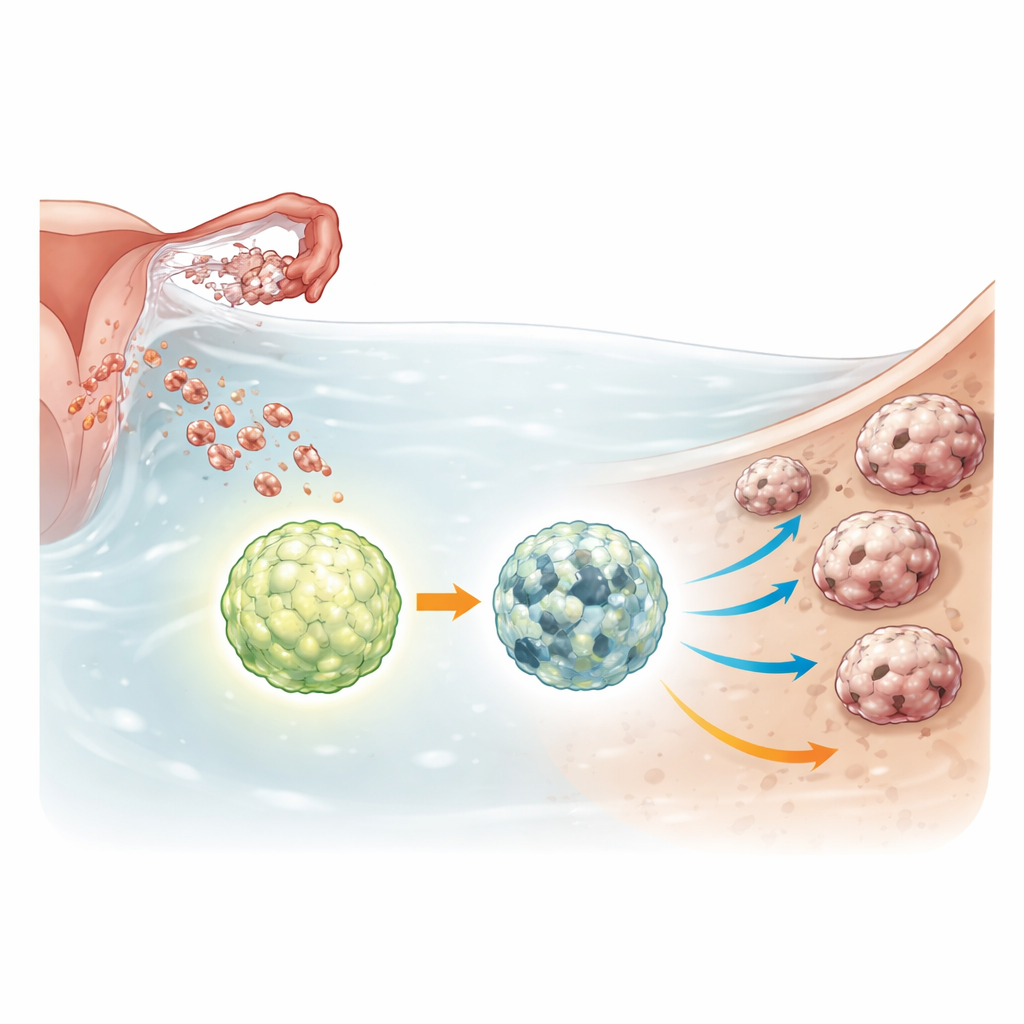
Een overlevingsschakelaar binnen kankercelklonters
Eierstokkankersferoïden doorstaan zware omstandigheden: weinig voedingsstoffen, gebrek aan hechting en blootstelling aan chemotherapie. Om hiermee om te gaan, zetten ze een recyclingsproces hoger, bekend als autofagie, dat interne componenten afbreekt en hergebruikt om cellen onder stress in leven te houden. ULK1 is een hoofdschakelaar die dit recyclesysteem aanzet. De onderzoekers gebruikten genbewerkingstools om ULK1 volledig te verwijderen uit meerdere eierstokkankercellijnen en uit een niet-kankerverwekkende eileiderbuiscelijn die vroege, precancereuze stadia voorstelt. Ze vergeleken vervolgens hoe normale en ULK1-deficiënte cellen zich gedroegen wanneer ze werden gekweekt als vrij zwevende sferoïden of als driedimensionale mini-tumoren, organoïden genoemd.
Wat er gebeurt als de schakelaar wordt uitgezet
Toen ULK1 in eierstokkankercellen werd verwijderd, was hun vermogen om autofagie uit te voeren binnen sferoïden sterk aangetast, zoals bleek uit veranderingen in belangrijke recycling-eiwitten. Deze ULK1-loze sferoïden bevatten minder levende cellen en vertoonden meer tekenen van geprogrammeerde celdood, wat aangeeft dat de kankerkolonies minder goed bestand waren tegen stressvolle omstandigheden. Interessant genoeg leidde het weghalen van ULK1 uit de niet-kankercellen van de voorganger niet tot een even grote uitschakeling van het recyclingsysteem, wat suggereert dat kankercellen meer afhankelijk zijn van ULK1 dan hun gezonde tegenhangers. Deze kankerspecifieke afhankelijkheid maakt ULK1 een aantrekkelijk therapeutisch doelwit.
Verspreiding vertragen en tumorposten verzwakken
Naast overleving in suspensie moeten sferoïden zich hechten aan en invasie plegen van de gladde bekleding van de buikholte om nieuwe tumoren te vormen. Met laboratoriummodellen die deze vroege stap van metastase nabootsen, toonde het team aan dat ULK1-deficiënte sferoïden veel minder goed waren in het opzij duwen en binnendringen van een laag mesotheliale cellen, die normaal gesproken buikorganen bekleden. Wanneer gekweekt als organoïden ingebed in een gelachtige matrix, vormden ULK1-loze kankercellen ook kleinere, minder robuuste tumorstructuren. In muismodellen waarin menselijke eierstokkankercellen in de buikholte werden geïnjecteerd, leidde verlies van ULK1 tot minder tumordeposities en minder vochtophoping, beide kenmerken van gevorderde ziekte, hoewel de algehele overleving van de dieren niet verbeterde.
Belangrijke signalen verzwakken en effect van gerichte medicijnen vergroten
Om te begrijpen hoe ULK1 kanker ondersteunt buiten recycling, brachten de onderzoekers eiwitveranderingen in kaart in sferoïden zonder ULK1. Ze vonden dat grote groeiregulatie- en overlevingsroutes in de cel—vooral de MEK–MAPK- en PI3K–AKT–mTOR-pathways—verstoord waren. Deze routes helpen kankercellen normaal gesproken weerstand te bieden aan celdood en door te blijven delen. Toen het team ULK1-deficiënte sferoïden behandelde met middelen die MEK of mTOR blokkeren, werden de kankerkolonies veel kwetsbaarder, met sterk verminderde levensvatbaarheid en herklevingsvermogen. Daarentegen maakte het verwijderen van ULK1 standaard chemotherapiemiddelen zoals carboplatin, paclitaxel of de PARP-remmer olaparib niet effectiever en leek het onder sommige omstandigheden hun voordeel juist te verminderen.
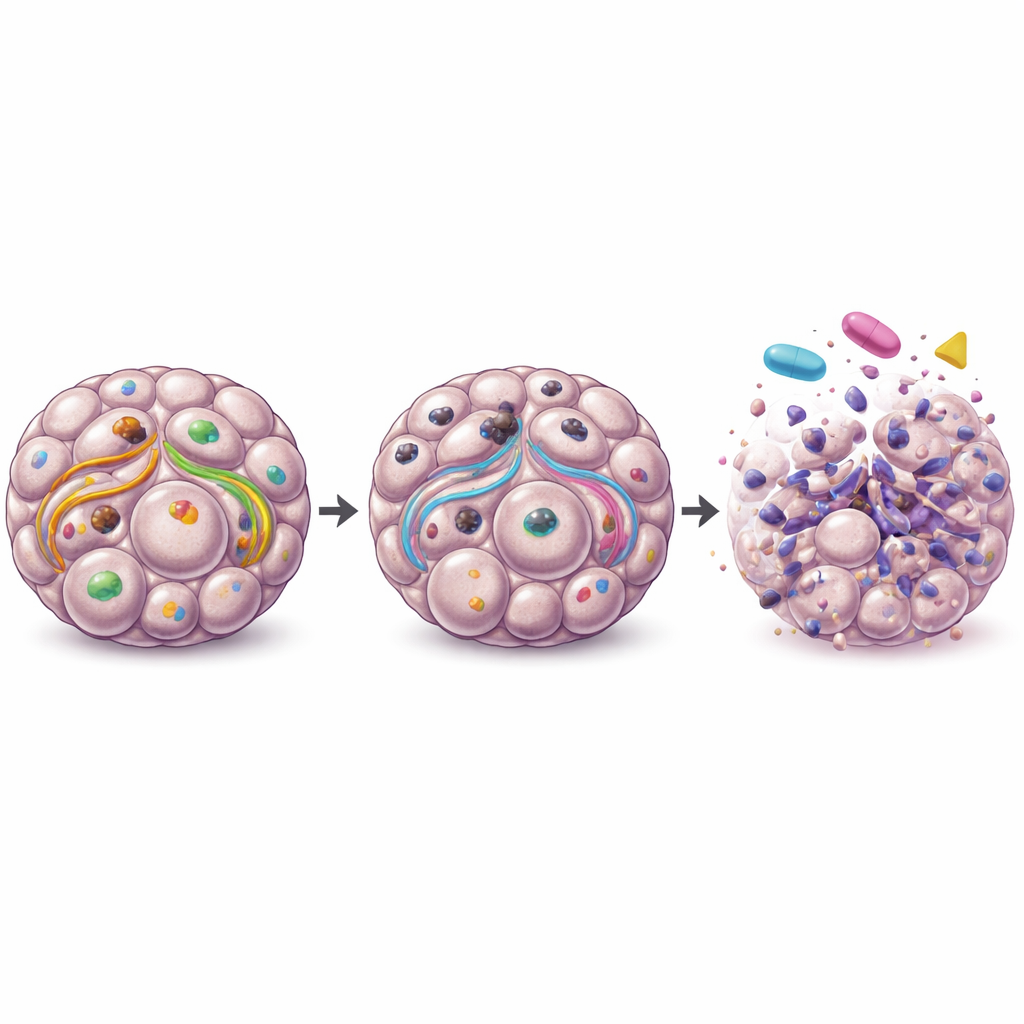
Aanwijzingen uit patiëntentumoren en miniatuurpatiëntmodellen
Bij het bekijken van grote openbare datasets van eierstokkankers vonden de auteurs dat hogere ULK1-genactiviteit gekoppeld was aan slechtere langetermijnoverleving en vooral verhoogd was in metastatische monsters vergeleken met primaire tumoren en normaal weefsel. Om dichter bij de kliniek te komen, testten ze een klinische ULK1-blokkerende pil, DCC-3116, op patiënt-afgeleide organoïden gekweekt uit metastatische tumormonsters. In een deel van deze patiëntmodellen verminderde het blokkeren van ULK1 alleen, of het gebruik van MEK- of mTOR-remmers alleen, de overleving van organoïden, hoewel het combineren van de middelen niet consequent extra voordeel gaf. Andere patiëntorganoïden waren resistent tegen alle behandelingen, wat onderstreept hoe divers eierstokkankers kunnen zijn en hoe belangrijk biomerkers zijn om te bepalen wie baat kan hebben.
Wat dit betekent voor toekomstige zorg
Samengevat schetsen de bevindingen ULK1 als een centrale helper van eierstokkankerverspreiding: het voedt het interne recyclen dat sferoïdeclusters in leven houdt, ondersteunt hun vermogen om nieuwe sites binnen te dringen en helpt krachtige groeisignalen in stand te houden. Het uitzetten van ULK1 verzwakt deze processen, verkleint experimentele tumoren en maakt kankercelklusters gevoeliger voor bepaalde gerichte medicijnen, maar niet voor standaard chemotherapie. Voor patiënten suggereert dit werk dat ULK1 onderdeel zou kunnen worden van een precisiegeneeskundestrategie—vooral bij patiënten met ULK1-rijke, metastatische ziekte—waarbij gerichte remmers van ULK1 worden gecombineerd met MEK- of mTOR-blokkers om tumorgroei en -verspreiding te beperken, mits aandachtige tests kunnen vaststellen welke tumoren het meest waarschijnlijk reageren.
Bronvermelding: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Trefwoorden: eierstokkanker, metastase, autofagie, ULK1, gerichte therapie