Clear Sky Science · nl
POM121 O-GlcNAcylatie bevordert botmetastasen bij niet-kleincellig longkanker via versterkte c-MYC-nucleaire import en ECM-herprogrammering
Waarom dit onderzoek ertoe doet
Wanneer longkanker zich naar de botten verspreidt, veroorzaakt dat hevige pijn, botbreuken en een sterk verkorte overleving, maar artsen hebben nog weinig middelen om deze dodelijke stap te stoppen. Deze studie onderzoekt de interne werking van longkankercellen om te ontdekken hoe sommige cellen een specifiek voordeel verwerven waarmee ze van de long naar het bot kunnen migreren en daar kunnen groeien. Door dit proces terug te voeren tot kleine veranderingen aan één poorteiwit aan de rand van de celkern, identificeren de auteurs een nieuwe reeks gebeurtenissen die mogelijk gericht kan worden om botmetastasen bij patiënten met niet-kleincellig longkanker beter te voorspellen, te voorkomen of te behandelen.
Een suikerlabel dat het kankergedrag verandert
De onderzoekers richtten zich op post-translationele modificaties, kleine chemische veranderingen die eiwitten ondergaan nadat ze zijn gemaakt. Eén dergelijke wijziging, O-GlcNAcylatie genoemd, betreft de aanhechting van een kleine suiker aan specifieke plaatsen op eiwitten. Met longkankercellijnen en muismodellen vergeleek het team gewone tumorcellen met subpopulaties die herhaaldelijk geselecteerd waren op hun vermogen bot te koloniseren. Ze vonden dat deze botzoekende cellen veel hogere totale niveaus van O-GlcNAcylatie hadden, aangedreven door verhoogde activiteit van het enzym OGT, dat het suikerlabel aanbrengt. Van de honderden gewijzigde eiwitten viel er één op: POM121, een kerncomponent van de nucleaire porie, de structuur die het verkeer in en uit de celkern regelt.
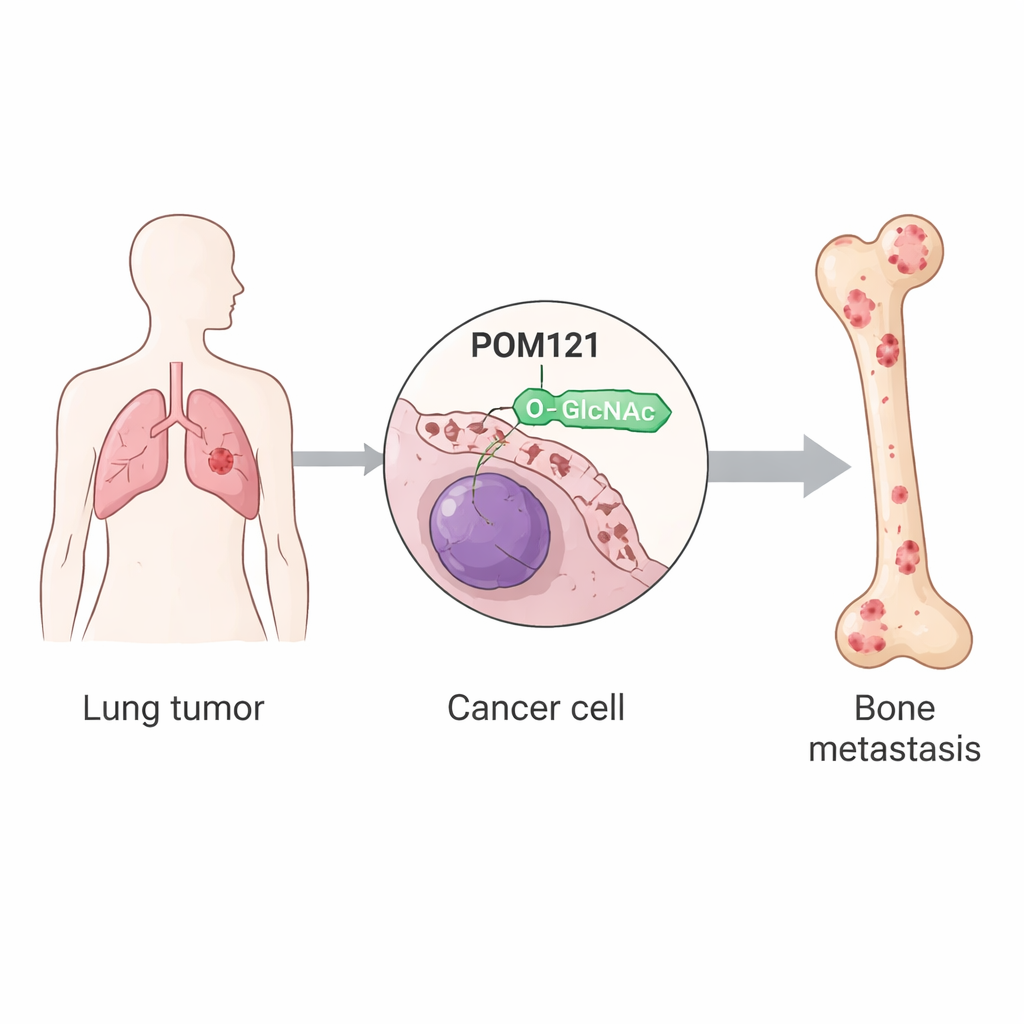
De nucleaire poortwachter POM121 wordt gestabiliseerd
POM121 bevindt zich in het membraan dat de kern omgeeft en vormt deel van het kanaal waarlangs veel signaaleiwitten moeten passeren. In longkankercellen met botmetastasen droeg POM121 een grote hoeveelheid O-GlcNAc op één aminozuurpositie, serine 199 genoemd. Wanneer deze plaats werd gewijzigd zodat hij niet langer gemodificeerd kon worden, werd het eiwit onstabiel en snel afgebroken door het opruimmachinerie van de cel. De studie toont aan dat het suikerlabel POM121 beschermt tegen markering voor vernietiging door een enzym dat TRIM21 heet, dat normaal ubiquitine-"afvoer"-etiketten aanbrengt. Met O-GlcNAc aanwezig kan TRIM21 niet goed binden, neemt ubiquitinatie af en hoopt POM121 zich op bij de nucleaire porie zonder van locatie te veranderen.
De deur openen voor een krachtige kankerveroorzaker
Welk verschil maakt extra stabiel POM121? De sleutel ligt bij een bekend kankerversterkend eiwit, de transcriptiefactor c-MYC. c-MYC moet de kern binnengaan om genen aan te zetten, maar zijn doorgang hangt af van nucleaire poriecomponenten zoals POM121. De auteurs toonden aan dat wanneer POM121 overvloedig en O-GlcNAc-gemodificeerd was, meer c-MYC in de kern werd aangetroffen; wanneer POM121-niveaus werden verminderd of zijn suikerlabel werd verwijderd, daalde de nucleaire import van c-MYC sterk. In muizen vormden longkankercellen met de niet-modificeerbare POM121-mutant veel minder en kleinere botmetastasen, terwijl het herstellen van c-MYC in POM121-deficiënte cellen veel van hun vermogen om bot te koloniseren terugbracht. Dit plaatst POM121 stroomopwaarts van c-MYC in een kritisch metastatisch pad.
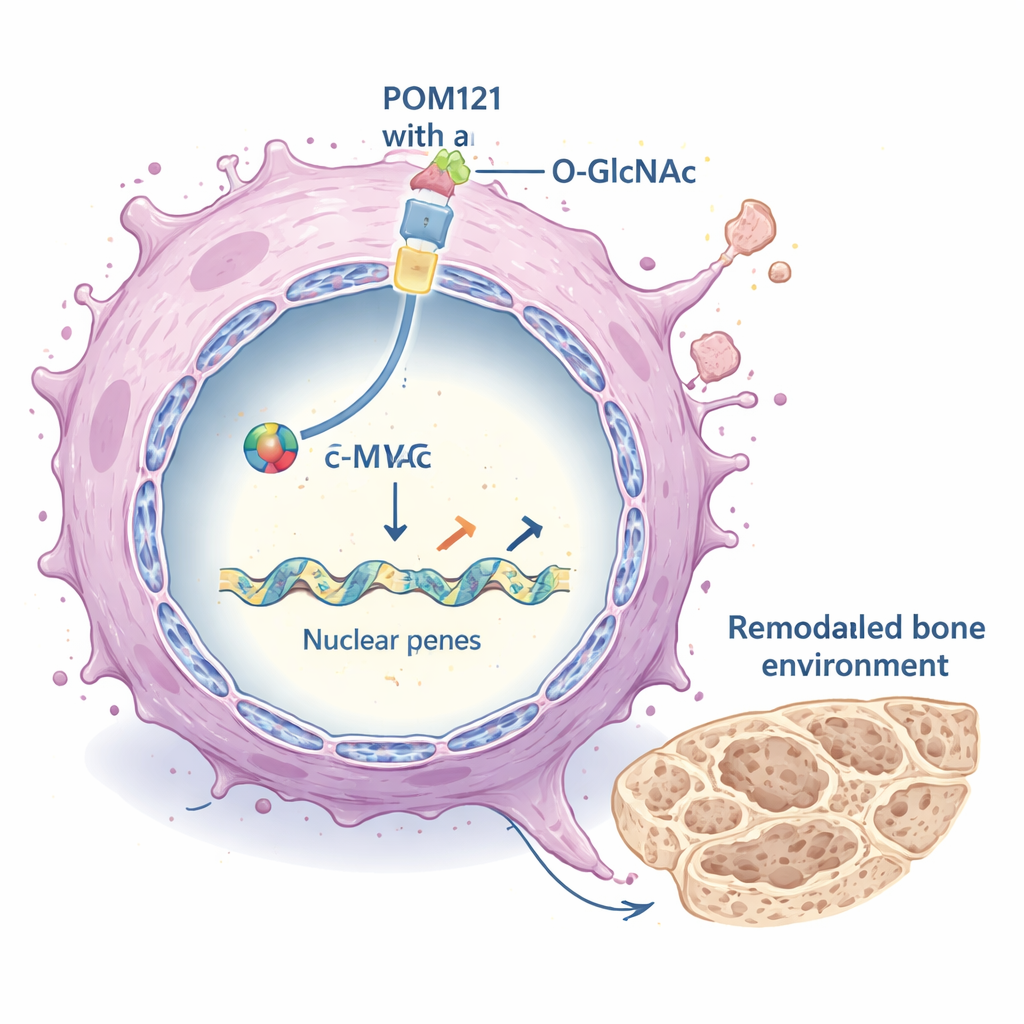
Het tumoromgivingsweefsel herbedraden
Eens binnen in de kern fungeert c-MYC als een meesterchakelaar voor veel genen. Hier bleek het sterk een reeks genen te activeren die de extracellulaire matrix (ECM) vormen — het skelet van eiwitten rond cellen. Deze ECM-genen, waaronder verschillende collagens en enzymen die de weefselstructuur herstructureren, werden omlaag gereguleerd wanneer POM121 of c-MYC werden geblokkeerd, en omhoog wanneer O-GlcNAcylatie en POM121 hoog waren. De gewijzigde ECM versterkte op haar beurt belangrijke groeipaden binnen de kankercellen, met name de PI3K–AKT–mTOR-signaleringscascade, die overleving, groei en uitzaaiing ondersteunt. Vergelijkbare patronen kwamen naar voren in meerdere longkankermodellen, wat suggereert dat dit mechanisme niet beperkt is tot één cellijn.
Van laboratoriumontdekking naar impact voor patiënten
Bij onderzoek van patiëntgegevens vonden de onderzoekers dat hoge niveaus van OGT, POM121 en c-MYC, evenals de ECM-genen die zij reguleren, geassocieerd waren met slechtere uitkomsten en met longtumoren die zich al naar het bot hadden verspreid. Gecombineerd schetst het werk een OGT–POM121–c-MYC–ECM-as: extra O-GlcNAcylatie stabiliseert de nucleaire poortwachter POM121, die meer c-MYC naar de kern brengt, die vervolgens het weefselraamwerk en groeisignalen herbedraad om botmetastase te bevorderen. Voor patiënten suggereert dit nieuwe soorten biomarkers om degenen met risico op botuitzaaiing te signaleren, en nieuwe therapeutische invalshoeken — van het blokkeren van OGT- of POM121-functie tot het temperen van c-MYC of ECM-remodellering — die mogelijk op termijn kunnen helpen voorkomen dat longkanker het skelet bereikt.
Bronvermelding: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Trefwoorden: longkanker botmetastase, POM121, O-GlcNAcylatie, c-MYC, extracellulaire matrix