Clear Sky Science · nl
Verstoring van interacties tussen androgeenreceptor en cofactoren door het RNA‑bindende eiwit FUS/TLS verandert androgeensignalering bij prostaatkanker
Waarom dit onderzoek belangrijk is voor de gezondheid van mannen
Prostaatkanker is sterk afhankelijk van mannelijke hormonen, androgenen genaamd, en van een eiwit dat ze detecteert, de androgeenreceptor. De meeste moderne behandelingen werken door deze hormonen weg te nemen of de receptor te blokkeren. Toch ontsnappen veel tumoren uiteindelijk aan deze controle en keren ze terug in een moeilijker te behandelen vorm. Deze studie onthult hoe een ander eiwit, FUS/TLS, in vroege prostaatkanker als een krachtige rem op androgeensignalering kan fungeren — en hoe die rem lijkt te falen naarmate de ziekte agressiever wordt.
Een verkeersregelaar voor hormoonsignalen
De androgeenreceptor werkt als een moleculaire schakelaar. Wanneer androgenen eraan binden, verhuist de receptor naar de kern van de cel, hecht zich aan DNA en schakelt genen in die de groei van prostaatcellen bevorderen. Hij werkt niet alleen: hulpstoffen kunnen zijn activiteit versterken of juist dempen. De auteurs richtten zich op FUS/TLS (kortweg FUS), een eiwit bekend om rollen in RNA‑verwerking en genregulatie, dat eerder in verband werd gebracht met vertraagde tumorgroei. Met behulp van in het laboratorium gekweekte prostaatkankercellen lieten ze zien dat veel van de door FUS gereguleerde genen overlappen met genen die door de androgeenreceptor worden gereguleerd, wat suggereert dat FUS direct bepaalt hoe hormoonsignalen worden vertaald naar groeiregels.
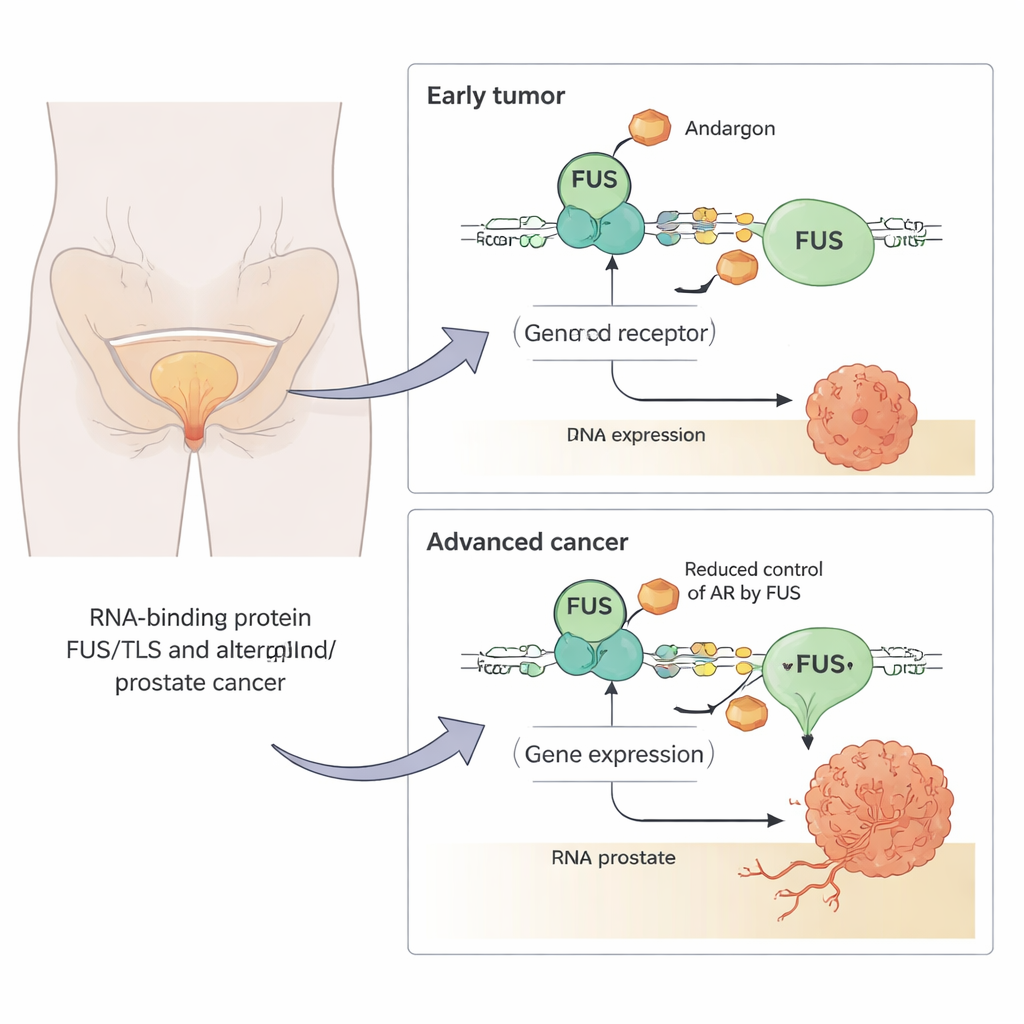
Hoe FUS de rem zet op tumorgedreven genen
Om te zien wat FUS doet, brachten de onderzoekers de hoeveelheid ervan kunstmatig omhoog of omlaag in prostaatkankercellen en volgden welke genen veranderden als reactie op een krachtig androgeenachtig middel. Ze ontdekten dat FUS androgeen‑gereguleerde genen in beide richtingen kan sturen, soms de respons versterkend en soms verzwakkend. Het dominante effect was echter repressie: klassieke androgeen‑gestimuleerde genen zoals PSA (KLK3) en TMPRSS2 werden naar beneden bijgestuurd wanneer FUS hoog was en omhoog wanneer FUS werd verwijderd. Reporter‑tests — eenvoudige metingen van androgeenreceptoractiviteit — bevestigden dat het verhogen van FUS de receptoractiviteit in verschillende celtypen globaal met ongeveer de helft tot twee derde verminderde.
Een fysieke blokkade van het hormoonapparaat
De wetenschappers vroegen zich vervolgens af hoe FUS deze controle uitoefent. Microscopen en interactietests toonden aan dat FUS en de androgeenreceptor elkaar in de kern ontmoeten en fysiek binden. FUS hecht aan een specifiek deel van de receptor via zijn RNA‑herkenningsdomein. Het bindt ook aan meerdere sleutelhulpstoffen die normaal gesproken de receptoractiviteit zouden versterken. Gedetailleerde experimenten bij een bekend androgeen‑responsief gen toonden aan dat FUS de receptor er niet van weerhoudt DNA te grijpen; in plaats daarvan voorkomt het dat het volledige team van hulpstoffen en de basale transcriptiemachines daar samenkomt. Met andere woorden: FUS laat de “schakelaar” op het DNA zitten maar haalt de onderdelen weg die nodig zijn om de genexpressie volledig op te voeren.
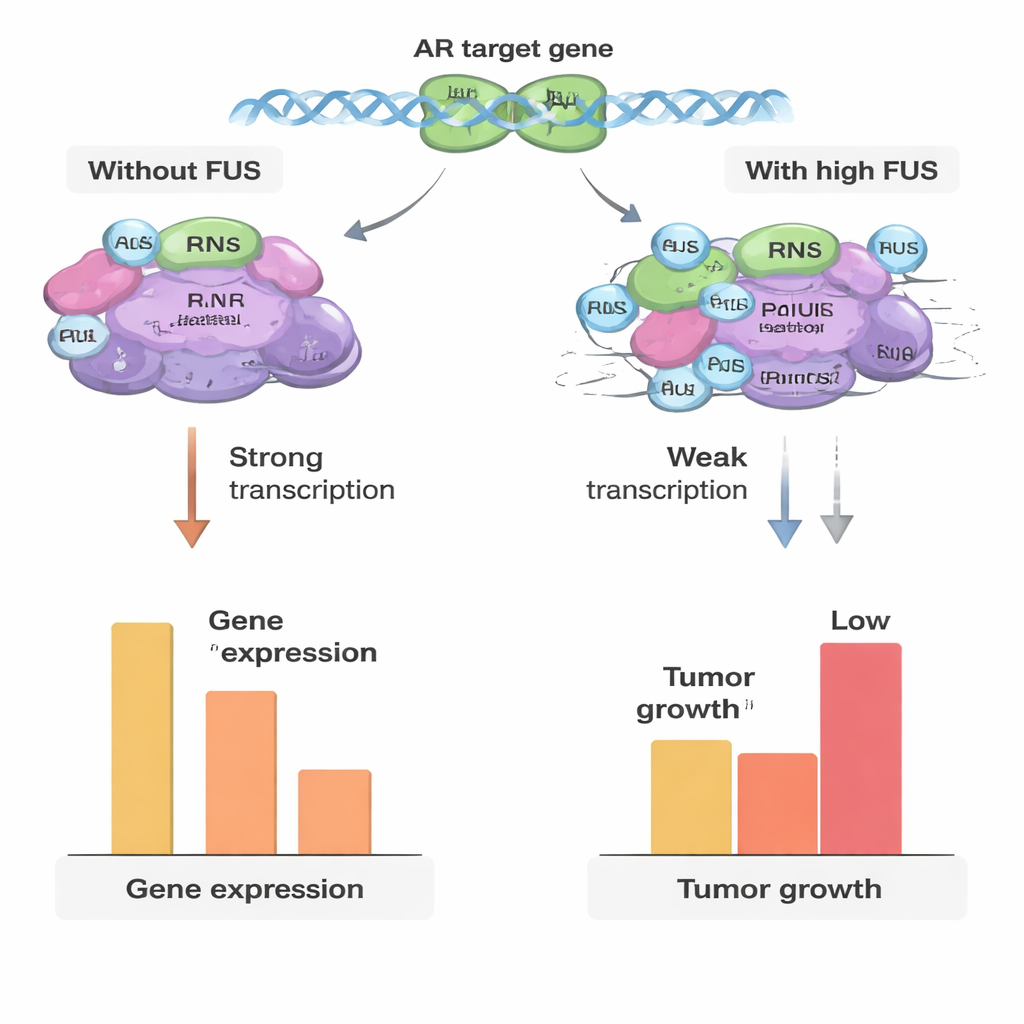
Een veranderende rol naarmate de kanker vordert
Aangezien resistentie tegen behandeling bij prostaatkanker vaak samenhangt met veranderingen in deze hulpstoffen, onderzochten de auteurs FUS‑niveaus in cellijnen en in patiëntmateriaal variërend van goedaardig weefsel en primaire tumoren tot gevorderde castratie‑resistente prostaatkanker (CRPC). In vroege tumoren waren de FUS‑eiwitniveaus over het algemeen lager dan in goedaardige monsters, wat past bij het idee dat tumoren deze natuurlijke rem omlaag brengen om makkelijker te groeien. Verrassend genoeg stegen de FUS‑niveaus weer in gevorderde CRPC en waren ze hoger dan in primaire tumoren. Toch veranderde in een CRPC‑achtig celmodel het verhogen van FUS niet langer sterk de androgeenafhankelijke genen, hoewel het nog steeds de algehele celdeling vertraagde. Dit suggereert dat, naarmate de kanker evolueert, het androgeennetwerk wordt herbedraad zodat FUS veel van zijn greep op de receptor verliest, terwijl het mogelijk via andere groeigerelateerde paden werkt.
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat FUS zich gedraagt als een ingebouwd veiligheidsmechanisme dat normaal voorkomt dat mannelijk‑hormoonsignalen prostaatcellen te hard aanjagen. In vroege kanker helpt het verlagen van FUS tumoren sneller te groeien; in gevorderde ziekte verandert het hormoonsysteem zodanig dat FUS wel aanwezig kan zijn maar de androgeenreceptor niet langer effectief remt. Precis begrijpen hoe deze rem werkt — en waarom hij faalt — zou nieuwe strategieën kunnen inspireren die ofwel zijn controle herstellen of zijn vermogen nabootsen om het hormoon‑gedreven groeimechanisme uit te schakelen, wat mogelijk de behandelingen voor mannen met gevorderde prostaatkanker kan verbeteren.
Bronvermelding: Brooke, G.N., Leach, D.A., Culley, R.L. et al. Disruption of androgen receptor-cofactor interactions by the RNA-binding protein FUS/TLS alters androgen signalling in prostate cancer. Oncogene 45, 757–773 (2026). https://doi.org/10.1038/s41388-026-03682-3
Trefwoorden: prostaatkanker, androgeenreceptor, resistentie tegen hormoontherapie, RNA‑bindende eiwitten, FUS TLS