Clear Sky Science · nl
Sortiline vertoont tumorremmende-achtige activiteit door de transductiefunctie van EGFR te beperken
Waarom dit belangrijk is voor kankerbehandeling
Longkanker is de belangrijkste oorzaak van sterfte door kanker wereldwijd, en veel moderne medicijnen richten zich op een molecuul genaamd EGFR dat tumorgroei aanstuurt. Deze geneesmiddelen werken vaak aanvankelijk goed, maar tumoren worden vaak resistent. Deze studie onthult een natuurlijke "rem" binnen longkankercellen — een onverwachte rol voor een eiwit genaamd sortiline — dat de kankerbevorderende signalen van EGFR kan temperen. Inzicht in deze relatie kan helpen verklaren waarom sommige patiënten beter reageren op EGFR-gerichte therapieën en kan nieuwe manieren aandragen om die behandelingen langer effectief te houden. 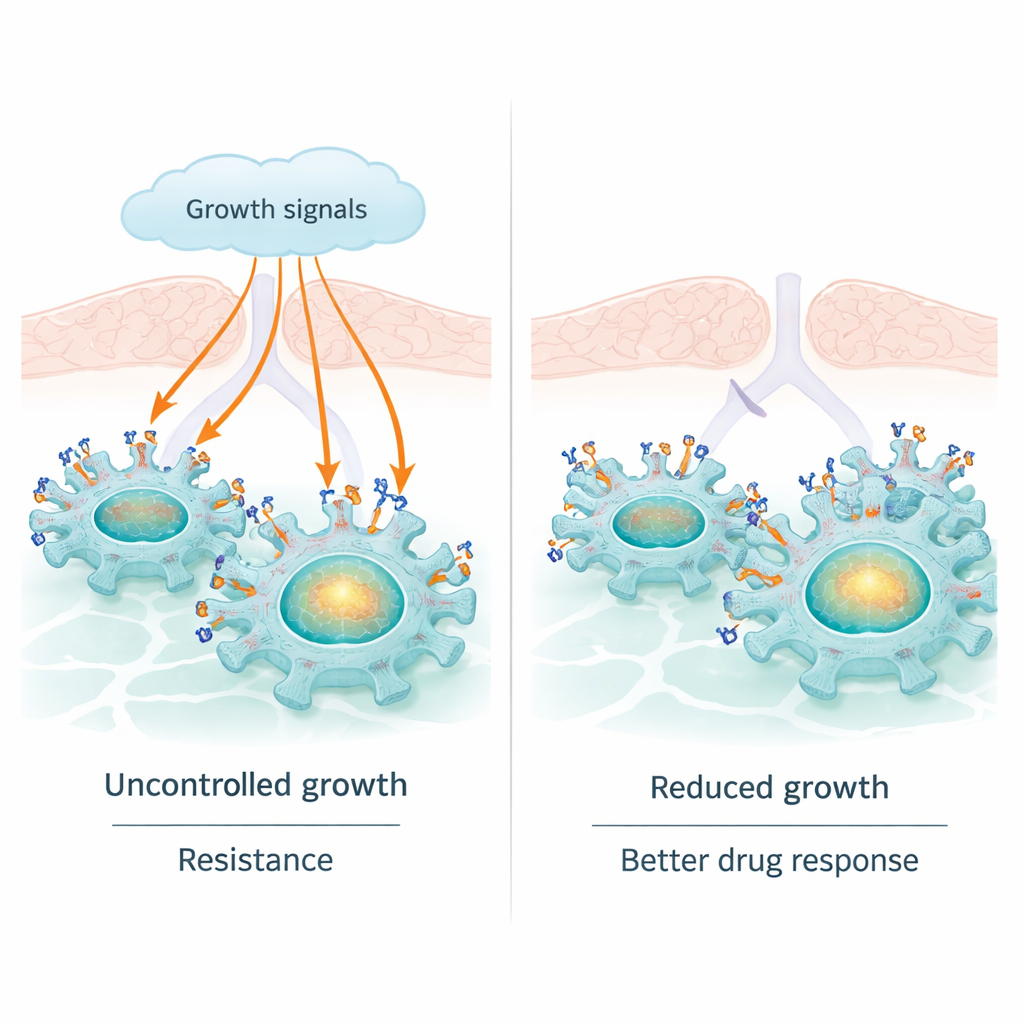
Een groeischakelaar die op overdrive staat
EGFR is een receptor op het celoppervlak die groeisignalen uit de omgeving waarneemt. In een groot deel van de longadenocarcinomen is EGFR veranderd zodat het permanent aanstaat. Dit voedt constante groei en deling, en verklaart waarom EGFR-blokkerende pillen, tyrosinekinaseremmers genoemd, tumoren kunnen laten krimpen. Maar EGFR heeft een minder gewaardeerde kant: het kan naar de celkern reizen en direct op DNA inwerken, waarbij het genen zoals cMYC en CCND1 activeert die groei, overleving en therapieresistentie verder versterken. Deze kernfunctie van EGFR kan helpen verklaren waarom tumoren ontsnappen, zelfs wanneer zijn oppervlakteactiviteit chemisch wordt geblokkeerd.
Sortiline volgt EGFR de kern in
Sortiline stond eerder vooral bekend als een sorteereiwit dat helpt EGFR van het celoppervlak te internaliseren en naar degradatie te sturen, waardoor zijn groeisignalen verzwakken. In dit werk tonen de auteurs aan dat sortiline EGFR ook volgt naar de kern wanneer longkankercellen gestimuleerd worden. Met behulp van microscopie met hoge resolutie en biochemische fractiëring zagen zij complexen van EGFR en sortiline kort na activatie in kernen vormen. Belangrijk is dat wanneer EGFR de kern niet kon binnengaan, sortiline ook buiten bleef, wat aangeeft dat EGFR als het ware het "toegangskaartje" van sortiline voor dit compartiment is. Eenmaal daar werden EGFR–sortilinecomplexen gevonden gebonden aan DNA-streken dicht bij de startplaatsen van belangrijke groeiregulerende genen, waaronder cMYC en CCND1.
Een ingebouwde rem op kankergenen
Om te begrijpen wat deze complexen doen, brachten de onderzoekers hun binding over het genoom in kaart en maten ze veranderingen in genactiviteit. Ze vonden dat EGFR op zichzelf de activatie van groeigerelateerde genen bevordert, terwijl de aanwezigheid van sortiline op dezelfde DNA-regio’s dit effect dempt. Wanneer sortiline kunstmatig werd verlaagd, nam de EGFR-binding aan doelgenen toe en werden kankerveroorzakende genen zoals cMYC en CCND1 actiever. Omgekeerd had het verhogen van sortiline het tegenovergestelde effect: EGFR’s greep op DNA verzwakte, de rekrutering van het transcriptieapparaat daalde en de expressie van deze oncogene genen nam af. In muismodellen groeiden longtumoren die meer sortiline produceerden langzamer en toonden ze verlaagde niveaus van cMYC en CCND1. 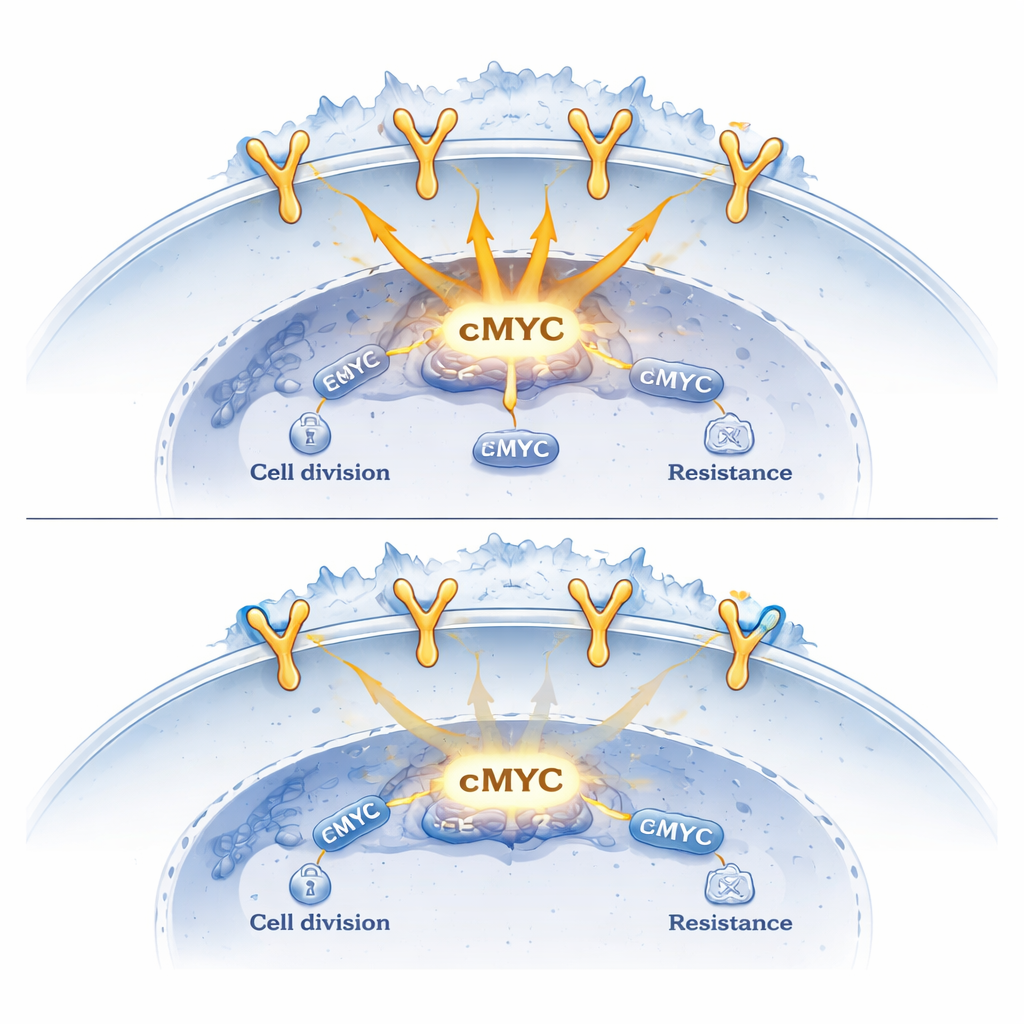
Interacties met EGFR-medicijnen
De studie onderzocht ook hoe dit mechanisme samenhangt met osimertinib, een veelgebruikt EGFR-gericht medicijn dat ontworpen is om schadelijke EGFR-mutaties te blokkeren. Verrassend genoeg bewoog de receptor nog steeds naar de kern, zelfs wanneer osimertinib de enzymatische activiteit van EGFR uitschakelde. Daar bleef het DNA binden, vooral in de buurt van het cMYC-gen. Sortiline hoopt zich onder deze omstandigheden echter ook in de kern op. Wanneer sortiline overvloedig aanwezig was, daalden de cMYC-niveaus sterker als reactie op osimertinib en werden kankercellen minder levensvatbaar. Analyse van patiëntentumoren en grote openbare kankerdatasets toonde dat sortiline-niveaus vaak lager zijn in longadenocarcinomen dan in normaal longweefsel, en dat hogere sortiline-expressie consequent gepaard gaat met lagere cMYC-expressie.
Wat dit betekent voor patiënten
Gezamenlijk presenteren de bevindingen sortiline als een soort tumoronderdrukkende partner die met EGFR de kern binnengaat en het daarna in toom houdt. Door EGFR’s vermogen te beperken om krachtige groeigenen zoals cMYC aan te zetten, kan sortiline de tumorgroei vertragen en de effectiviteit van EGFR-blokkerende geneesmiddelen vergroten. Omdat veel longtumoren verminderde sortiline hebben, ontbreekt hen mogelijk deze interne rem, wat kan verklaren waarom sommige kankers bijzonder agressief zijn of snel resistent worden tegen medicijnen. Het meten van sortiline-niveaus in tumoren zou kunnen helpen voorspellen hoe goed een patiënt zal reageren op EGFR-gerichte therapieën, en strategieën die sortiline-activiteit verhogen zouden een nieuwe manier kunnen bieden om EGFR-gedreven kankers beter langdurig te beheersen.
Bronvermelding: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Trefwoorden: longkanker, EGFR, sortiline, cMYC, resistentie tegen gerichte therapie