Clear Sky Science · nl
RO4938581, een negatieve allosterische modulator van GABAA-α5 herstelde gedrags- en EEG-fenotypes in een muismodel van Dup15q-syndroom
Waarom dit hersenonderzoek ertoe doet
Het Dup15q-syndroom is een zeldzame genetische aandoening die vaak autisme, epileptische aanvallen en ernstige leerproblemen veroorzaakt. Voor gezinnen is er weinig meer dan ondersteunende zorg, en er is geen behandeling die de onderliggende biologie aanpakt. Deze studie gebruikte muizen met hetzelfde extra DNA-segment als mensen met Dup15q om te onderzoeken wat er misgaat in de hersenen — en om te testen of een nauw gericht experimenteel middel dat probleem kan terugschakelen. Het werk belicht een specifiek type hersenreceptor als een veelbelovend, toetsbaar doelwit voor toekomstige precisiegeneesmiddelen.
Te veel remmen in de hersenen
Onze hersenen vertrouwen op een fijn afgestemde balans tussen "ga"-signalen die neuronen opwekken en "stop"-signalen die ze tot rust brengen. Bij het Dup15q-syndroom is een stuk van chromosoom 15 gedupliceerd. Dat gebied bevat drie genen die onderdelen bouwen van een belangrijke "stop"-receptor in de hersenen, de GABAA-receptor, en met name een variant die het alpha-5-eiwit bevat. De onderzoekers creëerden muizen met hetzelfde soort duplicatie en ontdekten dat deze dieren ongeveer 50% meer van de alpha-5–bevatte receptoren maakten in hersengebieden die belangrijk zijn voor geheugen, emotie en beweging, waaronder de hippocampus en cortex. Meerdere methoden — van genexpressie tot receptorbeeldvorming — kwamen tot dezelfde conclusie: dit specifieke remsysteem is overopgebouwd in het Dup15q-model.
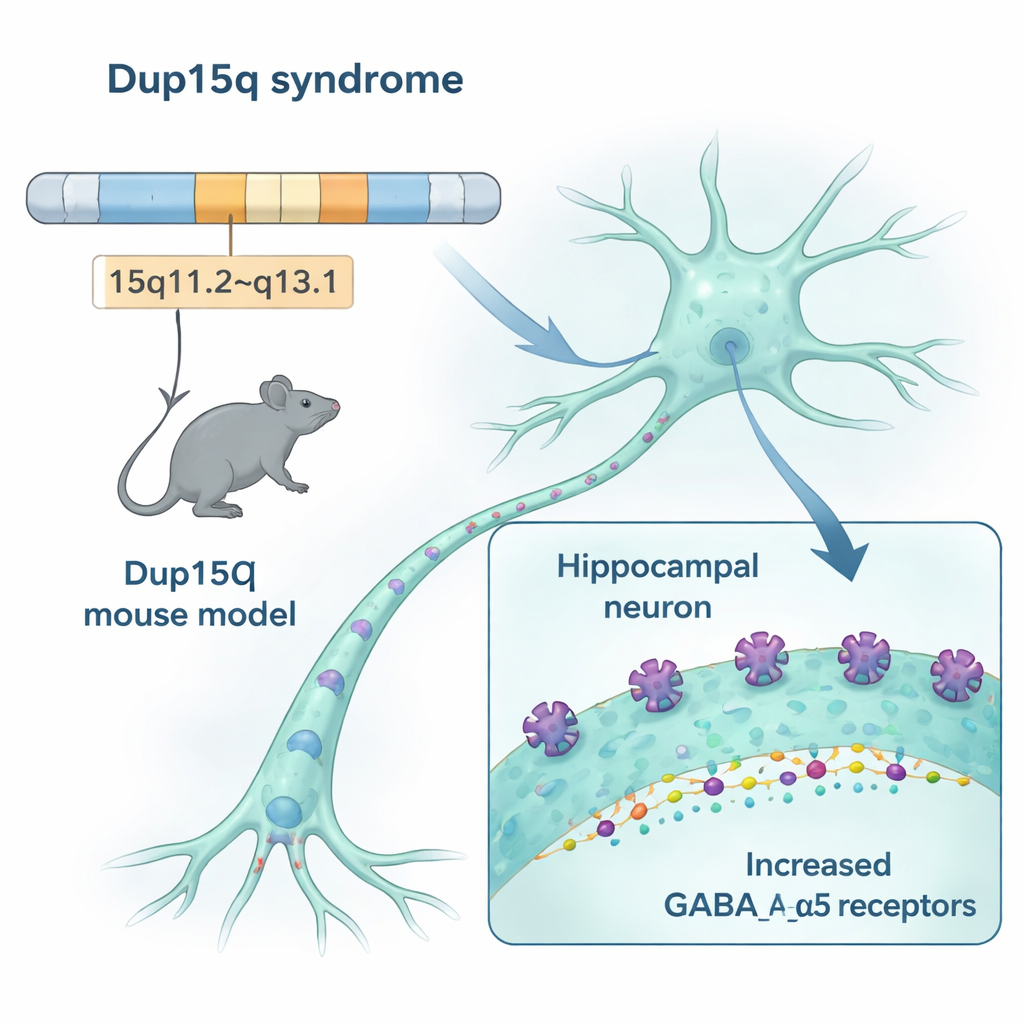
Hoe extra receptoren hersensignalen veranderen
Meer remmende receptoren zijn alleen van belang als ze daadwerkelijk veranderen hoe circuits vuren. In dunne hersenschijfjes uit de hippocampus maten de onderzoekers de kleine elektrische stromen die remmende neuronen naar andere cellen sturen. Bij de Dup15q-muizen traden deze remmende stroompjes vaker op, wat suggereert dat neuronen een sterker voortdurende rem ervoeren, ook al was de grootte van elk individueel signaal ongewijzigd. Een aparte test van circuitgedrag, genaamd paired-pulse inhibition, toonde ook aan dat netwerken in deze muizen sterker gedempt waren dan die van hun gezonde nestgenoten. Gezamenlijk wijzen de gegevens erop dat de extra receptoren remmende circuits dominanter maken, waardoor de balans verschuift weg van flexibele informatieverwerking.
Gedrag en hersengolven bij aangetaste muizen
De wetenschappers vroegen zich vervolgens af of deze gewijzigde bedrading zich vertaalde naar gedragingen die menselijke symptomen weerspiegelen. In een reeks tests toonden de Dup15q-muizen aanwijzingen voor sociale en communicatieve verschillen en, het duidelijkst, problemen met cognitieve flexibiliteit. In een waterruimte-labyrint leerden zowel normale als Dup15q-muizen waar een verborgen platform zich bevond. Maar wanneer het platform werd verplaatst, waren de Dup15q-dieren traag met het verlaten van de oude locatie en met het aanpassen aan de nieuwe — een laboratoriumparallel van de rigide routines die vaak bij autisme worden gezien. Het team nam ook elektro-encefalografie (EEG) op, de samengevoegde ritmes van veel neuronen. Zoals bij mensen met Dup15q vertoonden de muizen buitengewoon sterke bètaband-activiteit, een snel ritme dat vaak wordt versterkt door middelen die GABAA-receptoren versterken, wat het idee versterkt dat hun remmende systeem overactief is.
Een gericht medicijn dat de remmen versoepelt
Om te onderzoeken of ze dit overmatig remmen konden normaliseren, gebruikten de onderzoekers RO4938581, een experimentele verbinding die selectief alpha-5–type GABAA-receptoren verzwakt zonder andere vormen te beïnvloeden. In hippocampale schijfjes verminderde het middel de hoeveelheid remmende ladingsoverdracht in Dup15q-neuronen, waarmee het de excessieve rem compenseerde. Dagelijks oraal toegediend gedurende enkele weken verbeterde dezelfde verbinding de prestaties van de dieren in de omkeerfase van het waterruimtaken, waardoor ze zich aanpasten aan het verplaatste platform meer als gezonde muizen. Het bracht ook hun sociale interacties dichter bij normaal. In EEG-opnames verminderde een acute dosis gedeeltelijk de overdreven bètakracht bij Dup15q-muizen en schoof hun hersenritmes richting het typische patroon.
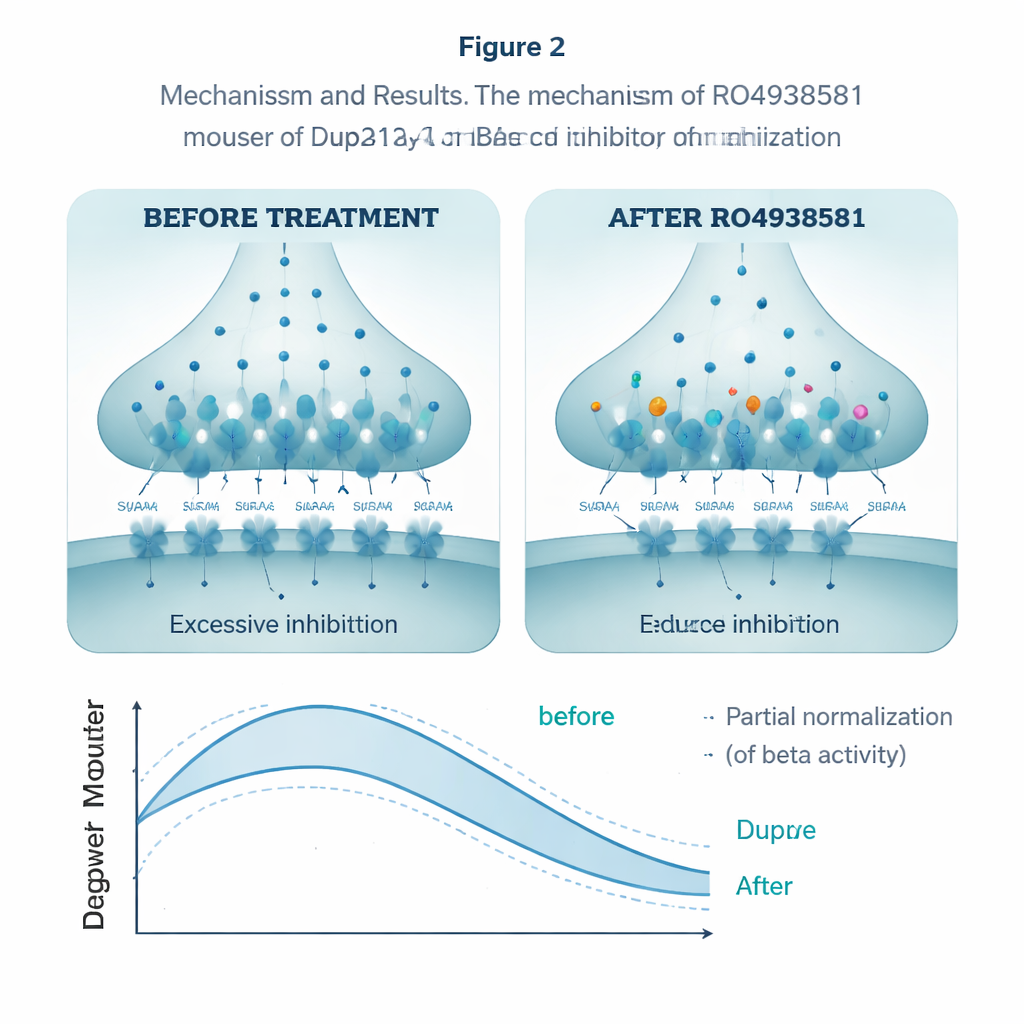
Wat dit kan betekenen voor toekomstige behandelingen
Voor gezinnen die met het Dup15q-syndroom leven, betekenen deze bevindingen geen directe genezing, maar ze bieden wel een concreet aanknopingspunt. Het werk wijst één specifieke receptor-subtype aan — GABAA-receptoren met het alpha-5-eenheid — als zowel overgeproduceerd als functioneel belangrijk in een relevant diermodel. Het matig terugschakelen van deze receptor met een negatieve modulator zoals RO4938581 loste niet alles op, maar verbeterde wel flexibele leerprestaties, sociaal gedrag en een belangrijk EEG-biomarker. Die combinatie van veranderingen in hersenfunctie, gedrag en biomarker versterkt het argument om veiligere, voor mensen geschikte alpha-5–gerichte middelen te testen als precisiebehandelingen voor Dup15q en mogelijk verwante neuroontwikkelingsstoornissen.
Bronvermelding: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Trefwoorden: Dup15q-syndroom, GABAA alpha-5 receptor, neuroontwikkelingsstoornis, EEG-bètakracht, muismodel