Clear Sky Science · nl
Cascadevormige inertiële microfluidica voor hoogwaardige, multiscale verrijking van tumorcellen en intacte clusters ter verbetering van maligniteitsdiagnostiek
Waarom het scheiden van kankercellen in vloeistof belangrijk is
Wanneer kanker zich verspreidt, ontsnappen tumorcellen vaak in de vloeistoffen die onze organen omgeven. Bij mensen met longkanker kan dit onder andere het vocht zijn dat zich rond de longen ophoopt, pleuravocht genoemd. Verborgen in dit vocht zitten zeldzame enkele tumorcellen en compacte celklonten. Deze clusters worden als bijzonder gevaarlijk beschouwd omdat ze sterk geassocieerd zijn met agressieve ziekte en slechte uitkomsten. Huidige laboratoriummethoden hebben echter moeite om zowel individuele cellen als clusters zacht en efficiënt uit grote hoeveelheden patiëntmateriaal te isoleren. Deze studie introduceert een nieuwe chip-gebaseerde technologie die deze cellen snel en voorzichtig uit pleuravocht kan scheiden, en daarmee de weg vrijmaakt voor betrouwbaardere kankerdetectie en beter inzicht in hoe tumoren zich verspreiden.
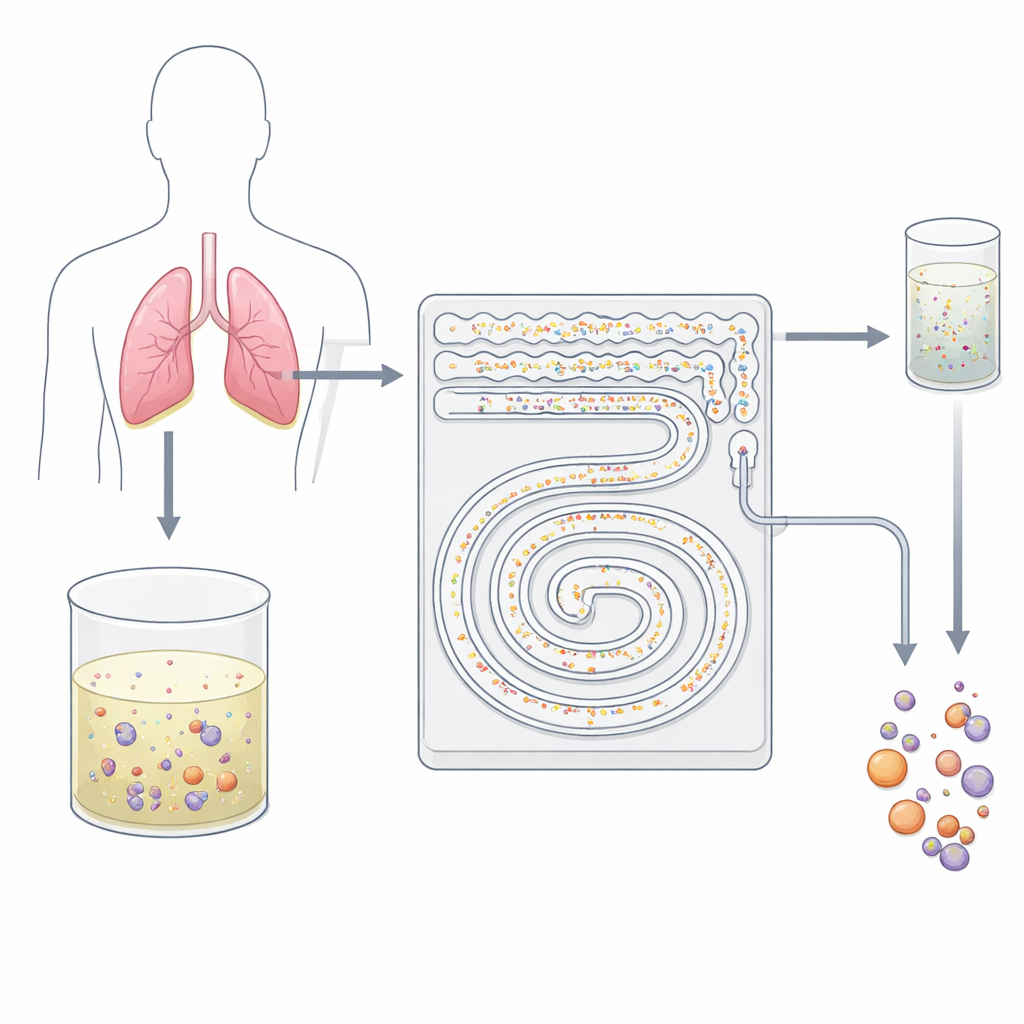
Een zachte celzeef op een chip
De onderzoekers ontwierpen een handpalmgroot plastic apparaat met microscopisch kleine kanalen die fungeren als een slimme, tweestaps filter. In plaats van kleverige antilichamen of ruwe zeefmethoden te gebruiken, vertrouwt de chip op het gedrag van cellen in snel stromende vloeistof. Als vloeistof door gebogen microkanalen stroomt, duwen onzichtbare krachten deeltjes van verschillende grootte in verschillende stroomlijnen. Het team maakt gebruik van dit effect, algemeen bekend als inertiële microfluidica, om kleine achtergrondbloedcellen te scheiden van grotere tumorcellen en hun clusters zonder ze aan te raken of te labelen. Omdat alles in een continue, gesloten stroming gebeurt, kan het apparaat tientallen milliliters vloeistof in slechts enkele minuten verwerken—iets wat traditionele cytologie op objectglaasjes niet gemakkelijk kan bereiken.
Eerste stap: de menigte opruimen
In de eerste fase van het apparaat wordt het pleuravocht—na het verwijderen van overtollig vocht en het opnieuw opsuspenderen van de cellen—door een reeks parallelle kronkelige kanalen gedreven. Hier drijft de draaiende, gebogen stroming kleine witte bloedcellen richting de kanaalwanden, terwijl grotere tumorcellen en clusters in het midden van de stroom blijven. De kleine cellen worden naar afvaluitgangen geleid, waardoor de achtergrond dramatisch wordt verdund. Deze hoogdoorvoerstap kan met ongeveer 8 milliliter per minuut draaien, wat betekent dat een typisch klinisch monster van 50 milliliter in ongeveer zes en een halve minuut kan worden verwerkt zonder te verstoppen. Wat uit deze eerste fase komt, is een veel schonere mengsel, verrijkt in potentiële maligniteiten en klaar voor fijnere scheiding.
Tweede stap: singles scheiden van clusters
Het gedeeltelijk verrijkte monster gaat vervolgens een schuine spiraalkanalen in die een herhalend patroon van nauwe en brede secties bevatten. In deze fase balanceren meerdere stromingskrachten verschillend voor objecten van verschillende grootte, waardoor ze zich in aparte banen nabij de binnen- of buitenwand van de spiraal sturen. Enkele tumorachtige cellen, die kleiner zijn, schikken zich op een laterale positie, terwijl grotere clusters naar een andere positie dichter bij de binnenwand migreren. Door uitgangen op de juiste plaatsen te zetten, verdeelt de chip deze stromen fysiek: één uitgang verzamelt voornamelijk losse tumorcellen, een andere verzamelt intacte clusters, en andere uitgangen verwijderen de resterende kleine cellen. Belangrijk is dat de clusters intact blijven en de schade en uiteenvallen vermijden die vaak worden gezien bij traditionele filtratiemethoden.
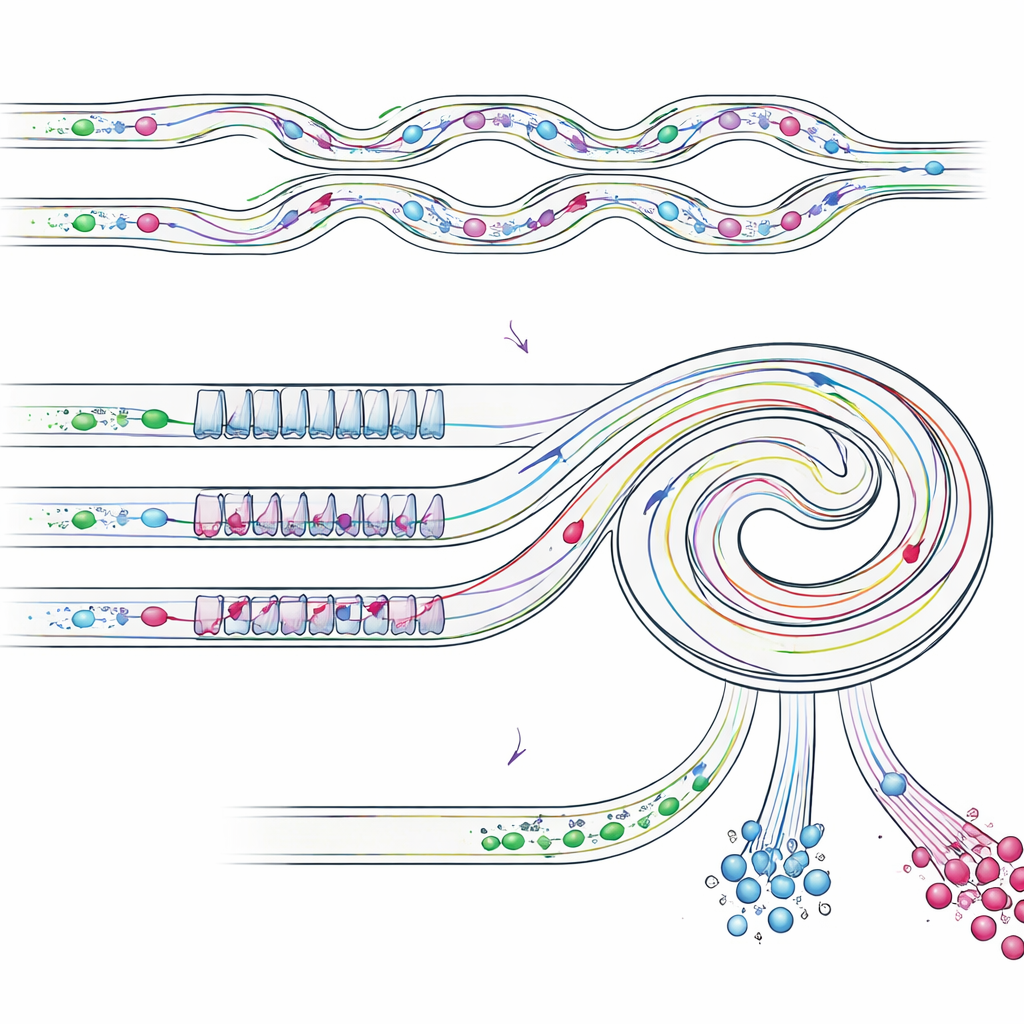
Het apparaat op de proef gesteld
Om te controleren hoe goed hun ontwerp werkte, gebruikte het team eerst kunststofparels van bekende groottes om bloedcellen, enkele tumorcellen en clusters na te bootsen. Ze toonden aan dat de cascadechip meer dan 87% van de ‘enkelcel’-parels en ongeveer 92% van de ‘cluster’-parels terugwon, terwijl de meeste kleinere ‘bloedcel’-parels werden verwijderd. Vervolgens gingen ze over op echte longkankercellen (A549-cellen) gemengd met witte bloedcellen. In deze tests herwon het apparaat ongeveer 82% van de kankercellen in totaal, met circa 76% zuiverheid in de verrijkte fractie en bijna 80% zuiverheid voor celclusters. Ten slotte verwerkten ze echte pleuravochtmonsters van drie longkankerpatiënten. Beginnend met vloeistof waarin tumorcellen en clusters minder dan 1% van alle cellen uitmaakten, produceerde de chip fracties waarin enkelvoudige maligne cellen ongeveer 68% van alle cellen bereikten en clusters ongeveer 35% van de cellen in een specifieke uitgangsstroom uitmaakten.
Wat dit voor patiënten zou kunnen betekenen
Door alleen gebruik te maken van vloeistofstroming en kanaalgeometrie kan dit apparaat snel en voorzichtig zowel enkele tumorcellen als intacte clusters uit grote volumes patiëntmateriaal halen zonder chemische labels of complexe instrumenten. De verrijkte cellen blijven geschikt voor standaardtests zoals immunofluorescentiekleuring en microscopie, en passen soepel in bestaande ziekenhuiswerkstromen. Hoewel de huidige studie een klein aantal patiënten betrof en grotere onderzoeken nodig zijn om de impact op diagnose en prognose te bewijzen, toont het werk een krachtig concept: een snelle, labelvrije “celconcentrator” die zowel het aantal als de geclusterde staat van tumorcellen in pleuravocht onthult. Op de lange termijn zouden zulke hulpmiddelen de beoordeling van maligniteit kunnen verscherpen, gepersonaliseerde behandelingskeuzes kunnen sturen en een duidelijker venster kunnen bieden op hoe kankers metastaseren.
Bronvermelding: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Trefwoorden: liquid biopsy, microfluidische celscheiding, tumorcellenclusters, pleuravocht, kankerdetectie