Clear Sky Science · nl
Ontwerp van een geautomatiseerd micro-injectiesysteem voor celpartijen op basis van magnetische pincetten voor zebravisembryo's
Waarom kleine vis eitjes ertoe doen
Voordat nieuwe geneesmiddelen of gentherapieën bij mensen worden getest, proberen onderzoekers ze vaak eerst uit op kleine, snelgroeiende dieren. Zebravisembryo's zijn populair omdat ze doorzichtig zijn en zich snel ontwikkelen, waardoor onderzoekers organen in realtime kunnen volgen. Om hun genen te veranderen of medicijnen toe te dienen, moeten wetenschappers elk delicaat eitje echter met een microscopische naald injecteren — een taak die meestal traag, vermoeiend en sterk afhankelijk van menselijke vaardigheid is. Dit artikel presenteert een nieuw robotsysteem dat batches zebravisembryo's automatisch kan injecteren, sneller, voorzichtiger en betrouwbaarder dan een mens, waarmee grotere en consistenter uitgevoerde experimenten mogelijk worden.
Een nieuwe manier om kwetsbare cellen te behandelen
Traditionele micro-injectie vereist een getrainde operator die een glazen naald onder een microscoop stuurt, elk embryo vindt, het in de juiste oriëntatie draait en doorboort zonder vitale structuren te beschadigen. Dat is extra lastig omdat embryo's zachte sferen zijn met belangrijke regio's die vermeden moeten worden om ze levend te houden. Bestaande robotsystemen hebben het vervoer en doorboren gedeeltelijk geautomatiseerd, maar ze kunnen meestal niet regelen hoe elk embryo in drie dimensies roteert. Daardoor kan de naald in een risicovolle hoek binnendringen, wat de overlevingskans verlaagt en het aantal betrouwbaar bewerkbare embryo's beperkt. Het team achter deze studie heeft een volledig geïntegreerd platform ontwikkeld dat embryo's soepel kan transporteren, roteren, injecteren en vrijgeven, zonder constante lenswissels of handmatige aanpassingen.
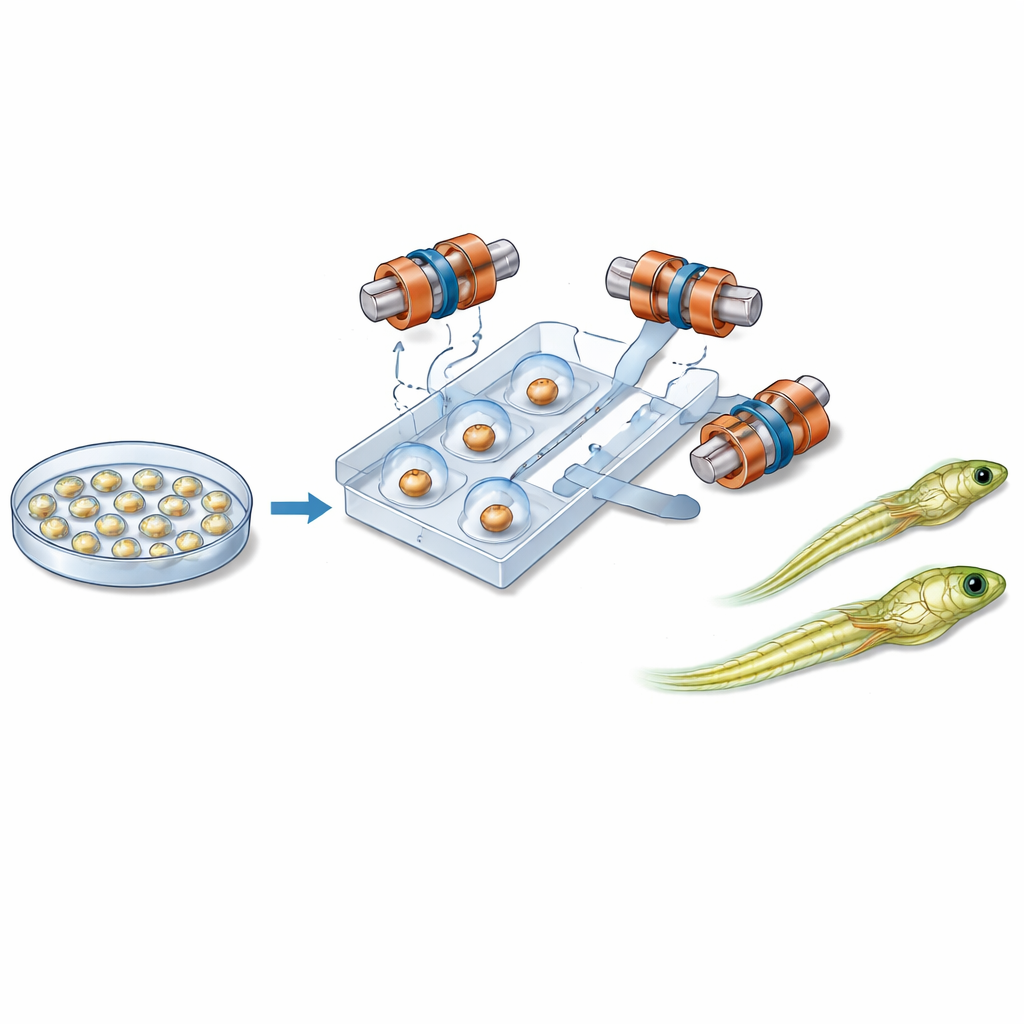
Magneten, microkanalen en zachte controle
Het hart van het nieuwe systeem is een handpalmgroot plastic chipje met smalle kanalen die individuele embryo's langs een vaste route leiden. Dicht bij elk embryo bevindt zich een klein magnetisch bolletje. Rond de chip genereren zes zorgvuldig gepositioneerde spoelen een uniform magnetisch veld in drie dimensies. Door de richting van dit veld in de tijd te variëren, laat het systeem het bolletje roteren. Dankzij wrijving tussen het bolletje en het oppervlak van het embryo draait de hele cel mee, als twee in elkaar grijpele tandwielen. Daardoor kan de robot het embryo kantelen uit het beeldvlak of in het vlak draaien totdat de gevoelige regio veilig gepositioneerd is ten opzichte van de naderende naald. Vloeistof en zachte luchtdruk verplaatsen en fixeren embryo's, terwijl een afzonderlijke module de injectienaald en de kleine stroom genetisch materiaal regelt.
Duidelijk zien in een klein zichtveld
Om deze precieze choreografie mogelijk te maken, ontwierpen de onderzoekers ook een geavanceerd computervisiestelsel, het microscopic manipulation perception network. Het analyseert beelden van een microscoopcamera in realtime om elk embryo te lokaliseren, de fijne naaldpunt te detecteren en de twee tegenoverliggende “polen” van het ei te onderscheiden waar belangrijke ontwikkelingsstructuren liggen. Het netwerk gebruikt moderne deep-learningtechnieken — zoals dubbele feature-extractiepaden, attentiemodules die belangrijke details benadrukken, en multi-scale fusie van beeldinformatie — om om te gaan met de rommelige, zwak belichte wereld binnen een microfluidische chip. In tests op duizenden afbeeldingen detecteerde en segmenteerde het netwerk embryo-regio's met ongeveer 98–99% nauwkeurigheid, wat de betrouwbare terugkoppeling levert die nodig is om zowel magnetische rotatie als naaldplaatsing te sturen.
Aantonen dat het werkt in levende zebravissen
Het team vergeleek hun geautomatiseerde systeem met ervaren menselijke operators, elk met 100 zebravisembryo's. De robot voltooide de injecties in ongeveer 33,8 seconden per embryo, meer dan twee keer zo snel als handmatig werk, en prikte elke cel met succes. Ook oriënteerde hij elk embryo met een gemiddelde hoekfout van slechts 2,1 graden, ongeveer de helft van de fout van menselijke operators. Het belangrijkste: 88% van de robot-geïnjecteerde embryo's overleefde tot ze uitkwamen als larven, vergeleken met 66% na handmatige injectie. Onder een fluorescentiemicroscoop gloeiden de larven van het geautomatiseerde systeem groen, wat aangeeft dat het ingebracht genetisch materiaal werd opgenomen en tot expressie kwam zoals bedoeld. Door embryo's magnetisch te roteren in plaats van samen te knijpen met mechanische gereedschappen, minimaliseerde het systeem vervorming en schade terwijl het toch een hoge doorvoer behaalde.
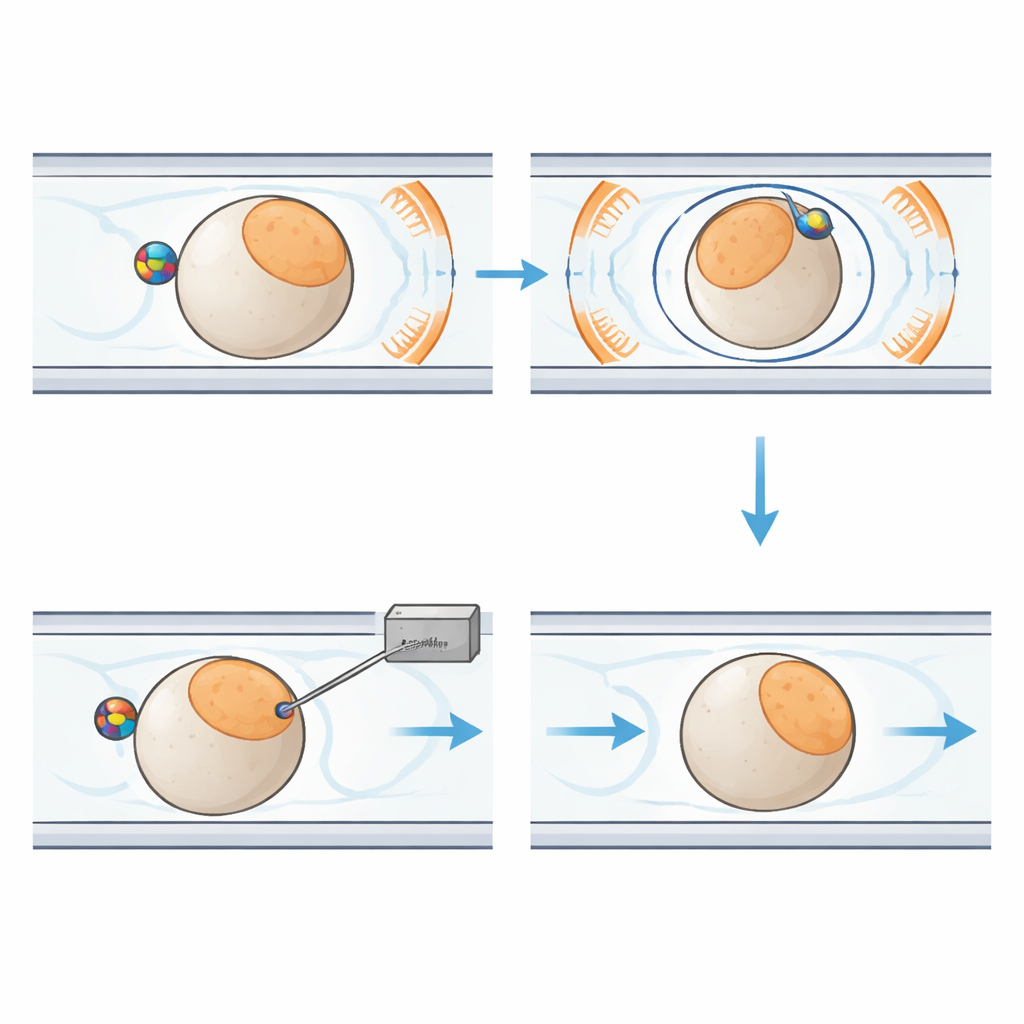
Wat dit betekent voor toekomstige studies
Simpel gezegd laat dit werk zien dat een zorgvuldig ontworpen combinatie van microkanalen, magnetische controle en slimme beeldanalyse kwetsbare visembryo's sneller en met betere overleving kan injecteren dan een bekwame persoon met traditionele gereedschappen. Omdat zebravissen een belangrijk model zijn voor het bestuderen van ontwikkeling, ziekte en medicijneffecten, kan een betrouwbare high-throughput injector grootschalige genetische screens en langdurige biologische studies versnellen die eerder werden beperkt door handmatig werk. Met geschikte ontwerpwijzigingen aan de chip en aansturingsinstellingen kan dezelfde strategie worden aangepast aan andere celtypen en kleine organismen, waardoor delicate cellulaire chirurgie verschuift van een ambacht geëxerceerd door enkele specialisten naar een geautomatiseerd, gestandaardiseerd proces.
Bronvermelding: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Trefwoorden: zebravisembryo's, micro-injectie, magnetische pincetten, microfluidica, robotische celmanipulatie