Clear Sky Science · nl
PEG-gepegeld Cu-gedoteerd WS2 hybride nanosheets voor doelgerichte multimodale kankertherapie
Waarom slimere kankerbehandelingen ertoe doen
Veel mensen met borstkanker krijgen nog steeds ingrijpende behandelingen die gezond weefsel kunnen beschadigen zonder de tumor volledig te stoppen. Deze studie beschrijft een nieuw soort nanoschaaltje, te klein om met het blote oog te zien, dat is ontworpen om door het lichaam te reizen, zich op borsttumoren te richten en ze gelijktijdig op meerdere manieren aan te pakken. Door warmte, chemie en een klassiek chemotherapeuticum in één doelgericht pakket te combineren, willen de onderzoekers de behandeling zowel krachtiger als vriendelijker voor de rest van het lichaam maken. 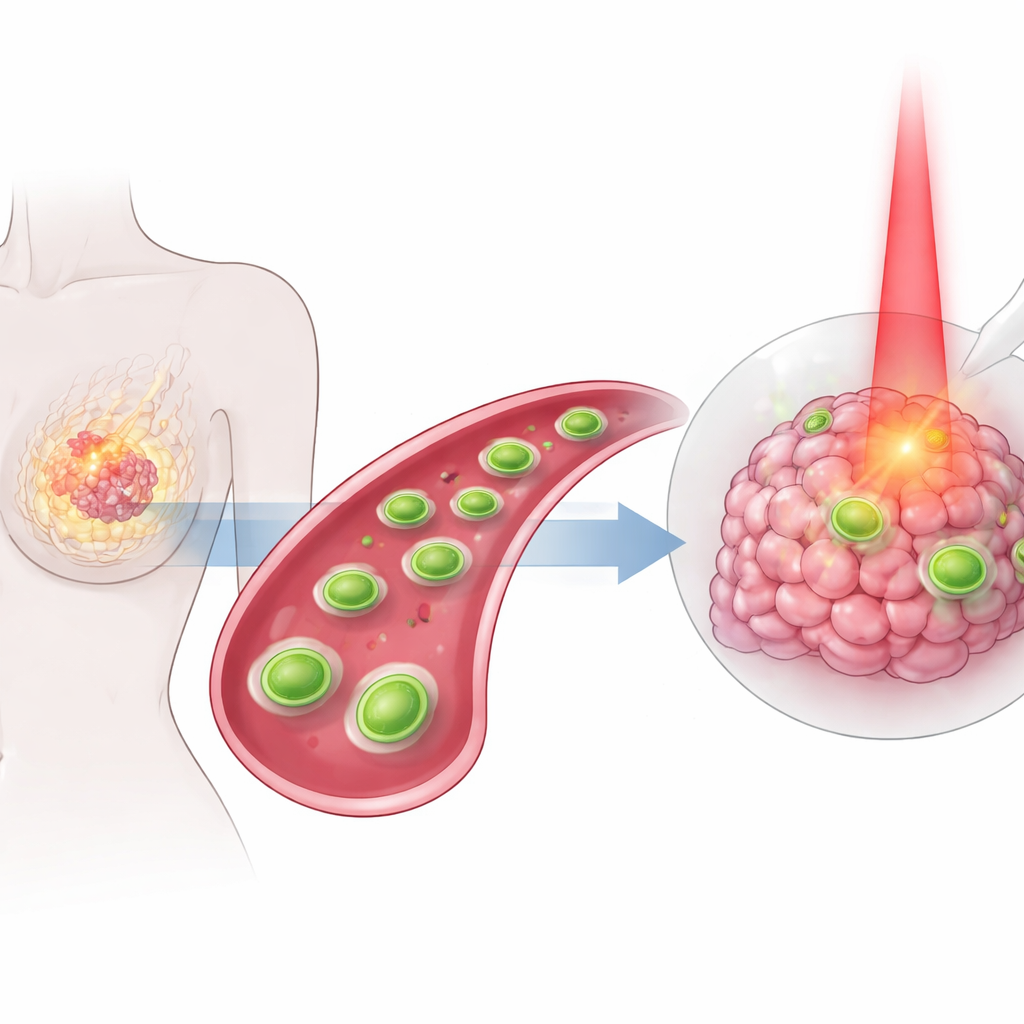
Kleine schilfers gebouwd om therapie te dragen en af te geven
De kern van de aanpak is een ultradun materiaal gemaakt van wolfraam en zwavel, gevormd als nanoschaaltjes. Deze schilfers absorberen van nature nabij-infrarood licht en zetten dat om in warmte. Het team maakte eerst deze schilfers en maakte vervolgens het oppervlak zorgvuldig ruw zodat ze andere nuttige ingrediënten konden vasthouden. Koperatomen werden in sterk verspreide vorm op de schilfers verankerd, en er werd een zachte, flexibele coating aangebracht die werkt als een moleculaire "regenjas" om de deeltjes goed in lichaamsvloeistoffen te laten disperseren en klontering te voorkomen. Ten slotte werd foliumzuur — een vitamine die veel tumorcellen gretig opnemen — als richtmechanisme aangehecht en werd het gebruikelijke chemotherapeuticum doxorubicine op het oppervlak geladen. Het eindresultaat is een klein, gelaagd platform dat in de bloedbaan kan circuleren, tumorcellen kan herkennen en een aanzienlijke lading behandeling kan vervoeren.
Hoe licht, chemie en medicijn samenwerken
Wanneer deze deeltjes eenmaal een tumor bereiken, gebeurt er tegelijk van alles. Als het tumorgebied wordt belicht met een zachte rode laser, verwarmen de wolfraam‑zwavel schilfers efficiënt en verhogen ze de lokale temperatuur genoeg om kankercellen te stressen en te beschadigen zonder de rest van het lichaam te oververhitten. Tegelijk reageren de koperatomen op de schilfers met natuurlijke peroxidemoleculen die in tumoren van nature in hogere concentraties aanwezig zijn. Deze reactie zet het peroxide om in zeer reactieve, kortlevende oxiderende soorten die van binnenuit schade aan cellulaire componenten toebrengen. Tumoren zijn daarnaast vaak iets zuurder dan gezond weefsel; in deze zuurdere omgeving, en onder verwarming door de laser, verzwakt de binding tussen het schilfermateriaal en doxorubicine, waardoor meer van het medicijn precies daar vrijkomt waar het nodig is. Deze drie effecten — warmte, chemische aanval en gerichte chemotherapie — zijn erop gericht elkaar te versterken. 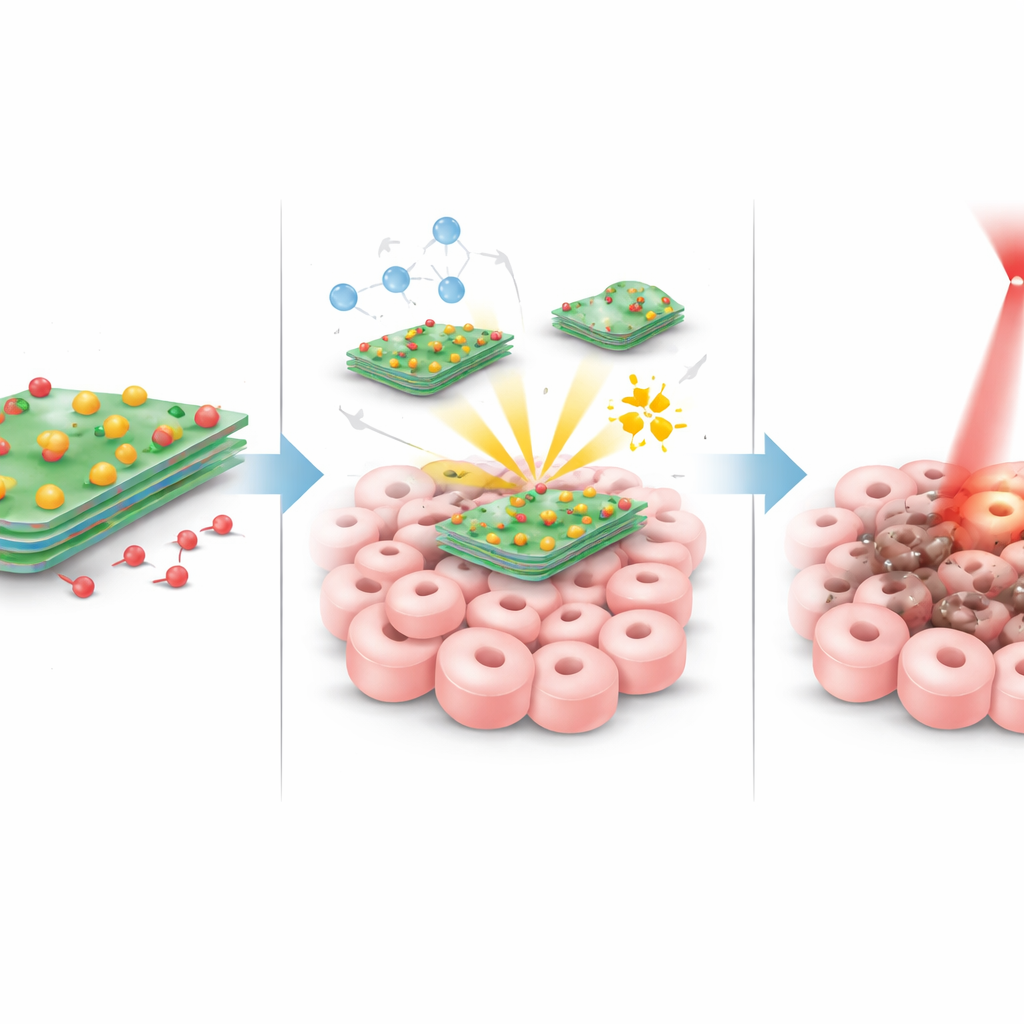
Bewijs uit cellen en bij muizen met tumoren
In laboratoriumschalen veroorzaakten de gecoate schilfers op zichzelf weinig schade aan normale cellen, wat wijst op een gunstige basisveiligheid. Maar wanneer ze waren geladen met doxorubicine en werden blootgesteld aan laserlicht in aanwezigheid van peroxide, veroorzaakten ze sterke celdood van borstkankercellen, veel meer dan bij enige afzonderlijke behandeling. De onderzoekers toonden ook aan dat de deeltjes een piek van reactieve oxiderende soorten in tumorcellen genereren, waarmee bevestigd wordt dat de koperchemie actief is. Bij muizen met borstkankertumoren stapelden deeltjes met de foliumzuurcoating veel sterker en langer op in tumorgweefsel dan niet‑gerichte deeltjes. Wanneer de muizen de volledige combinatie kregen — gerichte deeltjes plus belichting met rood licht — krimpten hun tumoren dramatisch, nam hun overlevingstijd toe en bleven hun lichaamsgewicht en orgaangezondheid grotendeels normaal, wat wijst op beperkte bijwerkingen vergeleken met standaard medicamenteuze behandeling.
Wat dit kan betekenen voor toekomstige kankerzorg
Gezamenlijk suggereren de bevindingen dat deze ontworpen schilfers werken als een multitool voor kankerbehandeling: ze zoeken tumoren op, verwarmen ze, vergiftigen ze van binnenuit via reactieve chemie en leveren een bewezen medicijn nauwkeuriger af, terwijl veel van de rest van het lichaam wordt gespaard. Het werk bevindt zich nog in de fase van dierstudies en er blijven belangrijke vragen over langetermijnveiligheid, afbraak en de beste manier om dergelijke deeltjes voor menselijk gebruik te produceren. De opzet laat echter zien hoe het combineren van meerdere bescheiden behandelingen in één slim pakket dat is afgestemd op de omgeving van de tumor een veel sterker totaal effect kan opleveren. Als vervolgonderzoek hun veiligheid en effectiviteit bevestigt, zouden dergelijke multifunctionele nanoplatforms kunnen bijdragen aan een meer gerichte, efficiëntere en minder belastende borstkankertherapie voor patiënten.
Bronvermelding: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Trefwoorden: borstkankertherapie, nanomedicijnen, fotothermische behandeling, gericht geneesmiddeltransport, chemodynamische therapie