Clear Sky Science · nl
Snel te vervaardigen en kosteneffectief enkel-laags microfluïdisch apparaat voor hoogdoorvoers driedimensionale hydrodynamische focussering
Waarom het verkleinen van microscopische stroompjes ertoe doet
De moderne geneeskunde is steeds meer afhankelijk van het één voor één bekijken van enorme aantallen individuele cellen, bijvoorbeeld om kankercellen in urine of bloed op te sporen. Om dit snel en goedkoop te doen, worden cellen vaak door haarfijne kanalen op microchips geleid, waar lasers of camera’s ze inspecteren. Maar om bij extreem hoge snelheden scherpe en betrouwbare beelden te krijgen, moet elke cel vrijwel exact door dezelfde kleine plek passeren. Dit artikel presenteert een nieuwe manier om zulke chips te bouwen zodat ze cellen strak in een smalle driedimensionale stroom kunnen dwingen, zelfs bij zeer hoge snelheden, met een apparaat dat sneller en goedkoper te produceren is dan de huidige standaardsystemen.
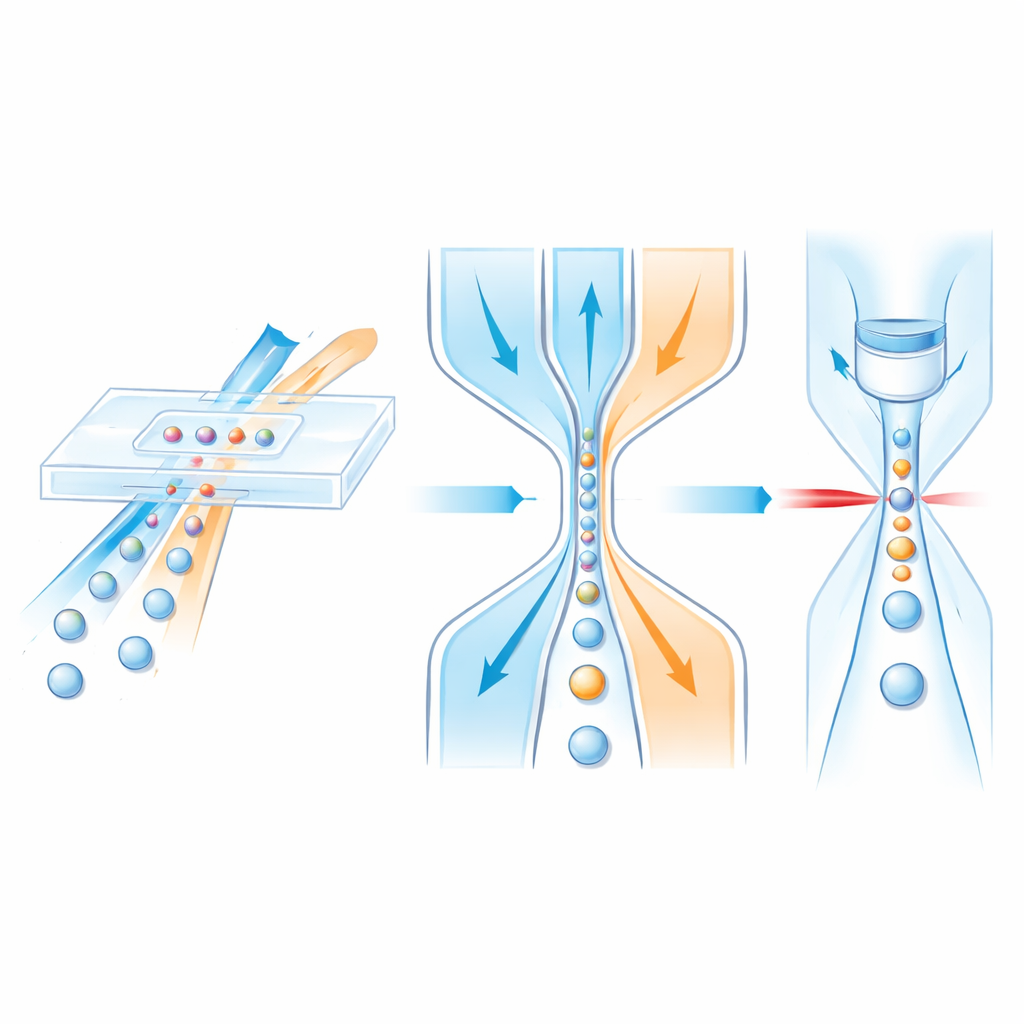
Cellen geleiden met stromende “rijstroken”
Binnen een microfluïdische chip reizen cellen in een centrale vloeistofstroom terwijl omliggende “sheath”-vloeistoffen werken als onzichtbare vangrails die het monster zachtjes naar het midden duwen. Vroegere ontwerpen konden cellen meestal alleen zijwaarts focussen, niet verticaal, of vertrouwden op complexe meerlaagse structuren die traag en kostbaar zijn om te vervaardigen. De auteurs ontwerpen in plaats daarvan een enkel-laagse kanaalstructuur die toch volledige driedimensionale controle bereikt. Eerst voegt het monster zich samen met een verticale sheath-stroom bij een schuin T-vormig kruispunt dat langs de lengte vernauwt. Vanwege de kanaalvorm en de traagheid van de vloeistoffen bij hogere snelheden wordt de monsterstroom naar de bovenste helft van het kanaal gedrukt. Vervolgens knijpen twee bijpassende zij-sheaths stroomafwaarts van links en rechts, waardoor het reeds opgetilde monster wordt samengeperst tot een smalle centrale filament die door een detectievenster loopt.
Betere chips bouwen in minuten, niet uren
De meeste onderzoeks-microfluïdische chips van tegenwoordig worden gemaakt van zacht siliconenrubber (PDMS) met behulp van softlithografie, een proces dat meerdere verwarmings- en uithardingsstappen vereist en een uur of langer per apparaat kan duren. PDMS is gemakkelijk te vormen maar buigt onder hoge druk, waardoor de kanalen uitzetten en de gefocusde stroom verspreidt. Het nieuwe apparaat gebruikt een hard plastic genaamd polyurethaanacrylaat (PUA), gepatterned via een “double transfer”-proces. Eerst wordt een herbruikbare PDMS-mal met verhoogde kanaalstructuren gegoten uit een silicium-master. Vloeibare PUA wordt vervolgens in deze mal gegoten, uitgehard onder ultraviolet licht en losgepeuterd om de kanaallaag te vormen. Een aparte, vlakke PUA-gecoate glazen slide dient als basis. De twee PUA-oppervlakken worden uitgelijnd, tegen elkaar gedrukt en gebonden met een korte aanvullende UV-belichting. Omdat elke uithardingsstap slechts enkele seconden duurt en geen langdurig bakken vereist is, kan een complete chip in ongeveer vijf minuten geproduceerd worden, ruwweg tien keer sneller dan traditionele methoden.
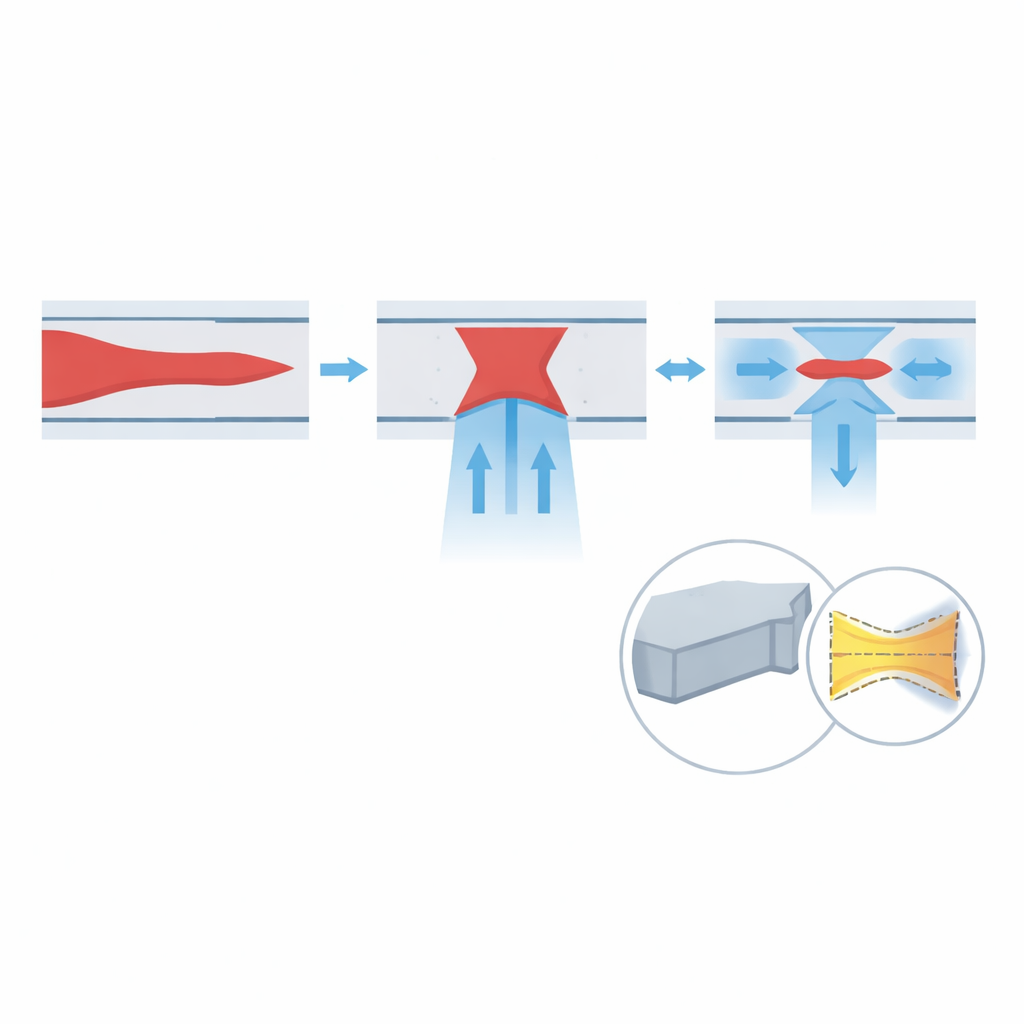
Stroom testen en vervorming beteugelen
Om te begrijpen hoe goed het ontwerp werkt, combineert het team computersimulaties met experimenten. Eerst simuleren ze hoe het variëren van de stroomsnelheden van de monster- en sheath-stromen de vorm van de gefocusde kern beïnvloedt. De resultaten tonen aan dat het verhogen van zowel de verticale als de zij-sheathstromen helpt om het monster in hoogte en breedte te vernauwen, en dat hogere totale snelheden (hogere Reynolds-getal) de focus verder verbeteren. Vervolgens simuleren ze hoe de kanaalwanden vervormen wanneer ze gemaakt zijn van zacht PDMS versus stijf PUA. Onder realistische hogesnelheidscondities bollen PDMS-wanden meer dan honderd micrometer uit, genoeg om de stroom dusdanig te vervormen dat het monster splitst en naar de hoeken afdwaalt. Daarentegen vervormt PUA met minder dan honderd nanometer — feitelijk rigide op deze schaal — zodat de gefocusde stroom gecentreerd en strak blijft, zelfs bij hoge druk.
Werkelijke cellen zien bij extreme snelheden
Naast gekleurde kleurstoftests evalueren de auteurs het apparaat met optische time-stretch (OTS) microscopie, een techniek die ultrafaste laserpulsen omzet in snelle lijnscans, waardoor miljoenen lijnbeelden per seconde mogelijk zijn. Ze sturen behandelde urinemonsters van blaaskankerpatiënten door de chip bij toenemende stroomsnelheden, terwijl OTS tweedimensionale beelden van elke passerende cel vastlegt. Omdat het optische systeem een zeer dun focale regio heeft, verschijnt elke cel die omhoog of omlaag afwijkt wazig, wat een directe maat geeft voor verticale focussering. Over snelheden van 3,3 tot 16,7 meter per seconde stijgt het aandeel scherp gefocusde beelden en bereikt 98,4% bij de hoogste geteste snelheid. Laterale focussering wordt beoordeeld door te meten hoe ver celcentra afwijken van het midden van het kanaal; deze afwijking neemt af met de snelheid, wat overeenkomt met ongeveer 95,0% laterale focussefficiëntie bij 16,7 meter per seconde.
Wat dit betekent voor toekomstige celanalyse
In eenvoudige bewoordingen tonen de onderzoekers aan dat een eenvoudige, enkel-laagse kunststofchip cellen betrouwbaar kan samenbrengen in een nauwe, goed gecontroleerde stroom in alle richtingen, zelfs onder de veeleisende omstandigheden die nodig zijn voor ultrahoge snelheid imaging. Door een vervormingsbestendig materiaal te combineren met een slimme opstelling van sheath-stromen, vermijden ze de mechanische beperkingen van zachte siliconenapparaten en verkorten ze de fabricagetijd dramatisch. Dit maakt het eenvoudiger om veel identieke chips te produceren voor klinisch en industrieel gebruik en om grootschalige, hoogdoorvoerse tests op echte patiëntmonsters uit te voeren. Als gevolg daarvan biedt de technologie een praktische route naar snellere, preciezere cel-screeningtools die nuttig kunnen zijn voor diagnostiek, kanker-monitoring en andere toepassingen die afhankelijk zijn van het nauwkeurig bekijken van grote aantallen individuele cellen.
Bronvermelding: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Trefwoorden: microfluïdische flowcytometrie, 3D hydrodynamische focussering, hoogdoorvoers single-cell analyse, polyurethaanacrylaat microfluïdische chips, optische time-stretch microscopie