Clear Sky Science · nl
Robotsysteem voor celtransport gebaseerd op modellering van micropipetweerstand
Minieme cellen verplaatsen zonder microscoop
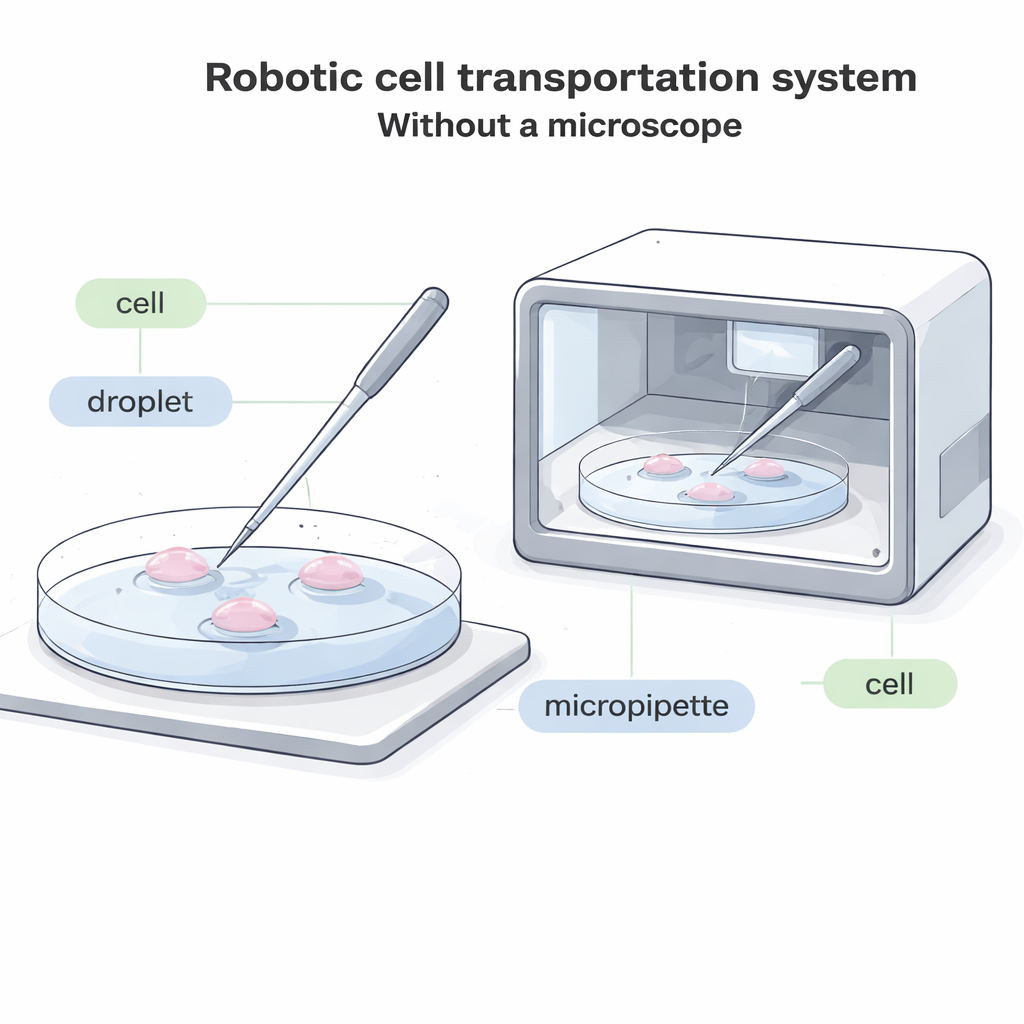
Moderne biologie hangt vaak af van een verrassend eenvoudige handeling: het oppakken van een enkele cel met een glazen buisje en die ergens anders plaatsen. Dit is essentieel voor vruchtbaarheidsbehandelingen, het invriezen van embryo’s, celgebaseerde therapieën en fundamenteel onderzoek. Toch vereist het tegenwoordig bijna altijd een omvangrijke microscoop en een hoogopgeleide menselijke operator die elke beweging nauwlettend volgt. Dit artikel beschrijft een nieuw robotsysteem dat individuele cellen tussen druppels vloeistof kan verplaatsen zonder enige microscopische waarneming, en daarmee de deur opent naar volledig afgesloten, geautomatiseerde ‘cell factories’ die sneller, goedkoper en met minder schade aan tere cellen kunnen werken.
Waarom celverplaatsing toe is aan vernieuwing
In huidige laboratoria kijkt een operator door een microscoop en gebruikt een dun glazen buisje, een micropipet genoemd, om de bodem van een schaaltje te raken, voorzichtig één cel op te zuigen, naar een nieuwe druppel te verplaatsen en die daar weer uit te drukken. Dit proces is traag, visueel belastend en moeilijk te automatiseren. In veel toekomstige systemen—zoals compacte, afgesloten apparaten die embryo’s of andere cellen in een behuizing laten groeien—is er simpelweg niet genoeg ruimte voor een traditionele microscoop. In andere gevallen zijn cellen gelabeld met fluorescerende kleurstoffen die vervagen of door licht beschadigd kunnen worden, zodat het minimaliseren van felle microscopische observatie belangrijk is. Bestaande ‘blinde’ systemen die niet op beelden vertrouwen werken alleen voor uitzonderlijk grote cellen, waardoor de meeste gangbare celtypen zonder goede geautomatiseerde oplossing blijven.
Een speciaal rietje met een ingebouwde stop
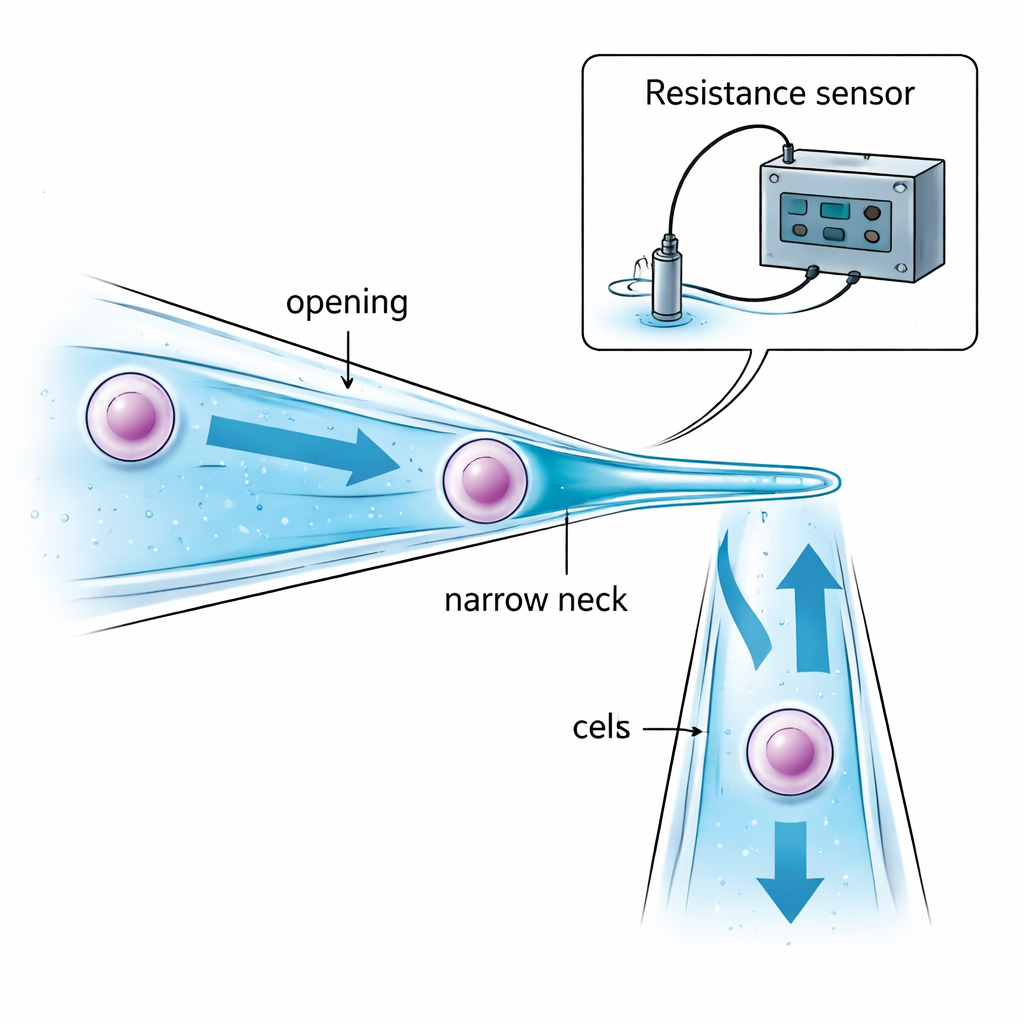
De auteurs pakken het probleem aan door de micropipet zelf opnieuw te ontwerpen. In plaats van een rechte glazen buis met overal dezelfde diameter, maken ze een micropipet met een smalle hals. De opening is iets groter dan de doelcel zodat de cel naar binnen kan worden getrokken. Dieper in vernauwt de buis geleidelijk tot een ‘hals’ die kleiner is dan de cel. Wanneer zuigkracht de cel naar deze vernauwing trekt, wordt de cel tegengehouden en vastgehouden in de buis—in plaats van te bungelen aan de punt en blootgesteld te worden aan olie of lucht tussen druppels. Zorgvuldige keuze van de openingsgrootte, de halsdiameter en de afstand daartussen zorgt ervoor dat de cel veilig wordt gevangen zonder te sterk te worden samengedrukt, en dat er slechts een kleine hoeveelheid vloeistof van de ene naar de andere druppel wordt meegenomen, wat verontreiniging vermindert.
Niet kijken maar luisteren naar elektrische signalen
Zonder microscoop moet de robot toch drie dingen weten: wanneer de glazen punt dicht genoeg bij de bodem van het schaaltje is, wanneer de cel succesvol bij de hals is gevangen, en wanneer die volledig in de nieuwe druppel is losgelaten. Het team lost dit op door zeer kleine veranderingen in elektrische weerstand in de vloeistof binnenin en rond de micropipet te monitoren. Terwijl de schuine pipet de bodem nadert, wordt de vloeistofspouw kleiner en stijgt de elektrische weerstand op een voorspelbare manier, wat een veilige landing aangeeft vlak voordat contact plaatsvindt. Als een cel de smalle hals blokkeert, wordt het elektrische pad door de vloeistof vernauwd en springt de weerstand plotseling omhoog; wanneer de cel wordt uitgedrukt, daalt de weerstand even scherp. Wiskundige modellen van deze ‘spouw-’, ‘aspiratie-’ en ‘injectie-’weerstanden stellen een computer in staat deze signalen in realtime te interpreteren en te beslissen wanneer zuigkracht of druk te stoppen, geheel zonder visuele feedback.
De robot aan een praktijktest onderwerpen
Om te onderzoeken of deze aanpak in de praktijk werkt, bouwden de onderzoekers een volledige robotopstelling die bewegingsregeling, drukregeling, weerstandsmeting en een hostcomputer combineert. Ze testten het systeem op kleine kankercellen bekend als HeLa-cellen (ongeveer 10 micrometer) en veel grotere varkenseicellen (ongeveer 150 micrometer). Het systeem kon betrouwbaar landen, vangen en loslaten detecteren puur aan de hand van weerstandssignalen over een breed scala aan pipetmaten. In directe vergelijkingen verplaatste de robot HeLa-cellen met een succeskans van 90 procent—beter dan een eerdere op beeld gebaseerde automatische methode—en transporteerde hij varkenseieren met een succeskans van 95 procent, hoger dan een standaard microscopische aanpak. De bedieningstijden per cel waren vergelijkbaar met, of sneller dan, door mensen bestuurde methoden, voornamelijk omdat de smalle hals de noodzaak van herhaalde fijnregeling van de zuigkracht om de cel te positioneren wegneemt.
Cellen levend houden en opschalen
Elke robotassistent in het biologie-labo moet voorkomen dat hij de cellen beschadigt die hij hanteert. Na transport door het nieuwe systeem werden zowel HeLa-cellen als varkenseicellen gedurende een dag gekweekt en gekleurd met een kleurstof die alleen in levende cellen oplicht. De overlevingspercentages voor de nieuwe methode kwamen overeen met, of benaderden dicht, die van traditionele onder microscoop geleide transfers en van onaangeroerde controlegroepen, wat aangeeft dat de zachte mechanische druk bij de smalle hals de levensvatbaarheid van cellen niet merkbaar vermindert wanneer de drempels correct zijn ingesteld. Vooruitkijkend suggereren de auteurs dat dezelfde op weerstand gebaseerde sensoring en drukregeling in compacte microfluïdische chips kunnen worden ingebouwd. Dat zou veel kanalen parallel laten werken, waardoor hoogdoorvoersystemen voor volledig afgesloten celhantering mogelijk worden—geschikt voor geautomatiseerde voortplantingsgeneeskunde, celtherapieën en langetermijneenheden voor celcultuur waar microscopen moeilijk te gebruiken zijn.
Wat dit betekent voor toekomstig celwerk
Voor niet-specialisten is de hoofdboodschap dat het verplaatsen van enkele cellen niet langer afhankelijk hoeft te zijn van een persoon die door een microscoop kijkt. Door een glazen buis zorgvuldig vorm te geven en te ‘luisteren’ naar hoe elektriciteit door de omringende vloeistof stroomt, kan een robot voelen wanneer hij geland is, een cel heeft gegrepen en loslaat—alles in het donker en in krappe ruimtes. Dit maakt het veel praktischer om gesloten, zelfstandig werkende kweeksystemen te ontwerpen die fragiele monsters beschermen, klinische workflows vereenvoudigen en laboratoriumkwaliteitscelmanipulatie dichter bij geautomatiseerde, fabrieksachtige bedrijfsvoering brengen.
Bronvermelding: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Trefwoorden: celmanipulatie, micropipet, robotica, microfluïdica, automatisering