Clear Sky Science · nl
Strategieën om cellulaire ruimtelijke organisatie te beheersen in microfysiologische systemen
Het bouwen van mini-weefsels in het laboratorium
Onze organen functioneren zo goed omdat hun cellen niet willekeurig verspreid zijn—ze zijn zorgvuldig in de ruimte gerangschikt. Dit artikel onderzoekt hoe wetenschappers leren die ingewikkelde ordening te reproduceren in “organen-op-chips” en andere miniatuur in het laboratorium gekweekte weefsels. Door te sturen waar verschillende cellen zich bevinden en hoe ze op elkaar reageren, kunnen onderzoekers realistischer modellen van hart, hersenen, darm, bloedvaten en zelfs mens–microbioom-ecosystemen bouwen. Deze geavanceerde systemen beloven veiligere medicijntests, minder dierproeven en betere instrumenten om ziekten te bestuderen en gepersonaliseerde behandelingen te ontwikkelen.
Waarom de positie van cellen ertoe doet
In het lichaam leeft elke cel in een specifieke buurt met zijn eigen mix van ondersteunende structuren, chemische signalen en fysieke krachten. Een levercel dicht bij een bloedvat ervaart heel andere prikkels dan een cel diep in het orgaan. Deze verschillen in locatie helpen bepalen hoe cellen groeien, wat ze differentiëren en hoe ze reageren op letsel of medicijnen. Wanneer wetenschappers cellen op platte plastic schalen kweken, gaat dat ruimtelijke “gesprek” grotendeels verloren en gedragen cellen zich vaak onnatuurlijk. Het artikel betoogt dat het nabootsen van realistische ruimtelijke organisatie geen optionele verbetering is, maar een basisvereiste als gekweekte weefsels echte organen willen nabootsen.
Twee hoofdmanieren om cellen te rangschikken
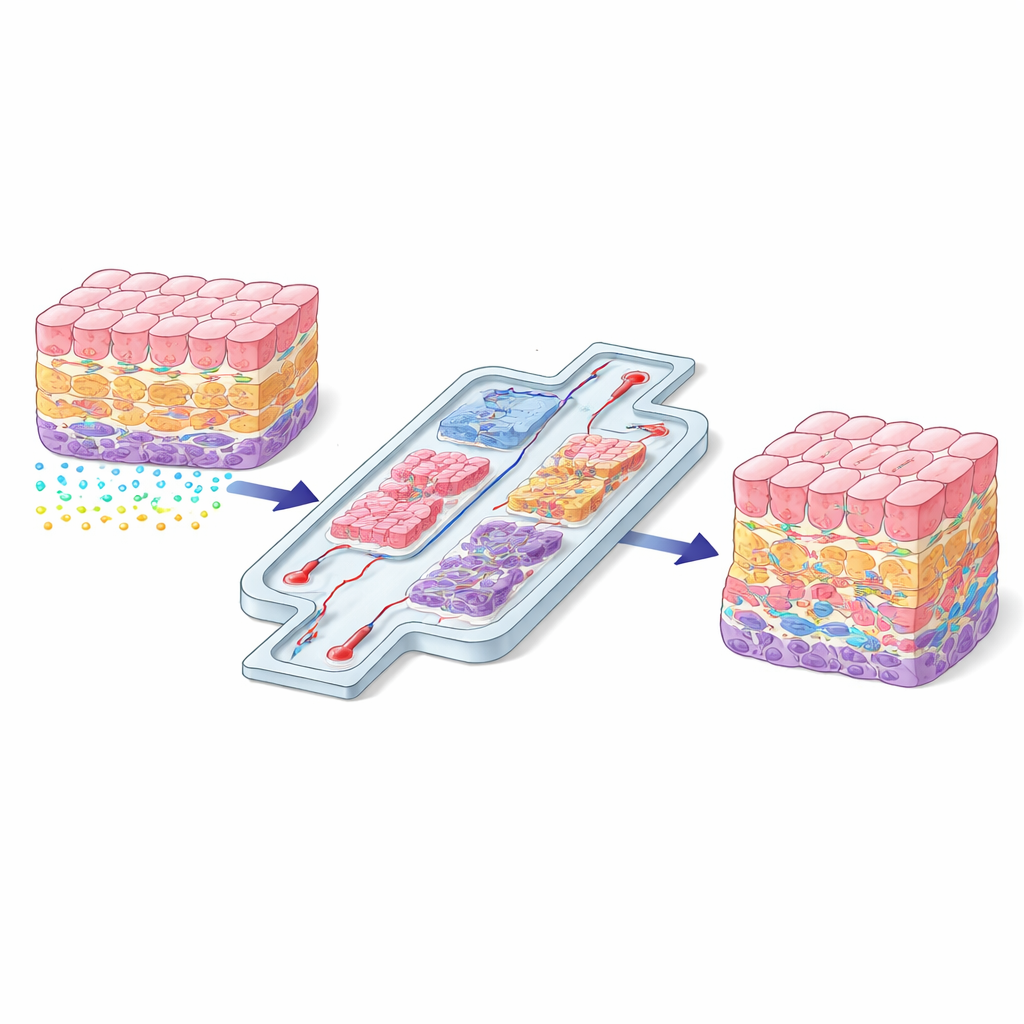
De auteurs delen de huidige strategieën in twee brede groepen: directe en indirecte controle. Directe methoden plaatsen cellen of compartimenten fysiek precies waar ze moeten zijn. Voorbeelden zijn 3D-bioprinten, dat lagen van cellen en zachte gels neerlegt als een biologische 3D-printer; microfluïdische chips die weefsels in verbonden kamers en kanalen vormen; en fysieke opvangmethoden die cellen in positie sturen met licht, geluid, magneten of elektrische velden. Deze benaderingen blinken uit wanneer precieze geometrie cruciaal is—zoals bij het nabootsen van een bloed–hersenbarrière, een gelaagde vaatwand of het stromingspad van darm naar lever.
Cellen hun omgeving laten lezen
Indirecte methoden hervormen in plaats daarvan de omgeving en laten de cellen de rest doen. Hier stemmen wetenschappers het “landschap” af dat cellen waarnemen: de samenstelling van de omringende gel, de stijfheid en textuur van oppervlakken en gradaties van opgeloste stoffen zoals groeifactoren of medicijnen. Zorgvuldig gerangschikte ondersteunende moleculen kunnen bepaalde celtypen doen neerslaan in specifieke regio’s. Slimme hydrogels die verzachten of signalen afgeven wanneer cellen ze remodelleren, stimuleren zelfgeorganiseerde structuren zoals bloedvatnetwerken of darmachtige crypten en villi. Microfluïdische apparaten kunnen stabiele chemische gradiënten genereren die stamcellen langs een kanaal verschillende identiteiten laten aannemen, of die kankercellen en immuuncellen naar aparte zones doen migreren, waardoor zichtbaar wordt hoe ziekten zich verspreiden.
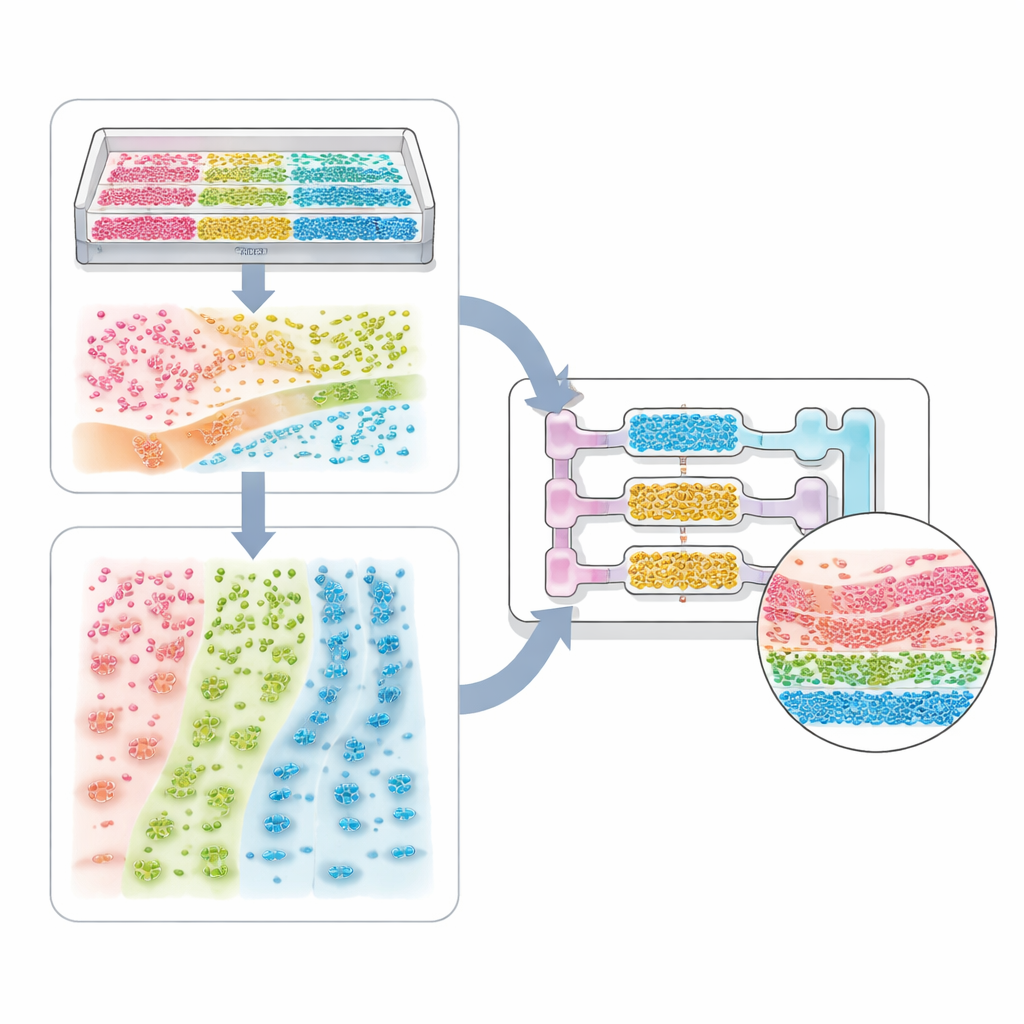
Van enkelcel-systemen tot lichaamsbrede modellen
De review loopt een spectrum van toepassingen door. Aan de eenvoudigste kant staan systemen met één celtype, waarbij geëtste groeven of stijfheidsgradiënten hartcellen synchroon kunnen laten samentrekken of zenuwcellen uitgelijnde vezels laten vormen. Meer complexe weefselmodellen mengen meerdere celtypen—zoals tumorcellen, ondersteunende cellen en vaatcellen—to make sferoïden en organoïden met interne kernen en schillen. Microkanaalchips en bioprinten voegen vervolgens grenzen en stroming toe, waarmee longblaasjes, nierfilters, leverzones en multi-orgaancircuits gereconstrueerd kunnen worden die volgen hoe een medicijn wordt opgenomen, omgezet en uitgescheiden. Dezelfde ideeën gelden voor gastheer–microbioom-systemen, waarbij de ruimtelijke ordening van bacteriën langs de darmwand of door een slijmlaag bepaalt of ze ons beschermen of ziekte veroorzaken.
Controleren of patronen echt zijn
Omdat deze systemen steeds complexer worden, hebben wetenschappers betrouwbare methoden nodig om te bevestigen dat cellen op de juiste plek terechtkomen en zich gedragen zoals bedoeld. Het artikel benadrukt beeldvormingstechnieken die levende cellen kunnen volgen terwijl ze bewegen en veranderen in de tijd, evenals geavanceerde kleuring en sequencing-technieken die in kaart brengen welke genen, eiwitten en metabolieten op elke locatie aanwezig zijn. Sensoren ingebed in chips kunnen zuurstof, nutriënten, zuren en mechanische krachten volgen, en zo lokale omstandigheden koppelen aan celreacties. Samen helpen deze instrumenten onderzoekers verifiëren dat een ontwerp niet alleen visueel overtuigend is maar functioneel trouw aan echt weefsel.
Waar dit werk naartoe gaat
De auteurs concluderen dat de krachtigste systemen directe en indirecte strategieën zullen combineren: chips en bioprinters gebruiken om de algemene lay-out vast te leggen, en daarbovenop afstelbare gels, texturen en gradiënten leggen die weefsels laten rijpen en remodelleren in de tijd. Ze noemen ook praktische uitdagingen—zoals opschaling van fabricage, het verminderen van variabiliteit tussen laboratoria en het adresseren van ethische vragen rond complexe menselijke weefselmodellen. Toch is de boodschap helder: het beheersen van ruimtelijke organisatie is de sleutel om microfysiologische systemen betrouwbare vervangers van menselijke organen te maken, en opent nieuwe mogelijkheden om ontwikkeling te bestuderen, therapieën te testen en geneeskunde op maat te maken voor individuele patiënten.
Bronvermelding: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Trefwoorden: orgaan-op-een-chip, cellulaire ruimtelijke organisatie, 3D-bioprinten, microfluïdische weefselmodellen, microfysiologische systemen