Clear Sky Science · nl
One-pot CRISPR-gebaseerd point-of-care platform voor snelle, specifieke en gevoelige detectie van HPV 16 zonder voorafgaande amplificatie
Waarom het opsporen van één virustype echt belangrijk is
Baarmoederhalskanker wordt vaak in verband gebracht met infectie door humaan papillomavirus (HPV), maar niet alle HPV‑typen geven hetzelfde risico. Artsen hebben daarom testen nodig die deze zeer vergelijkbare virussen betrouwbaar van elkaar kunnen onderscheiden, met name het hoogrisicotype dat HPV16 heet. De uitdaging is dat hedendaagse genetische tests soms nauwe verwantschappen kunnen verwisselen, wat leidt tot valse alarmen of gemiste gevallen. Deze studie introduceert een nieuwe testmethode die zowel de nauwkeurigheid als de praktische toepasbaarheid sterk verbetert, met als doel nauwkeurige HPV‑subtypering naar klinieken en point‑of‑care locaties te brengen.
Een slimme moleculaire slot-en-sleutel
De onderzoekers bouwden een eenbuistest die ze CASTSA noemen en die twee krachtige concepten combineert: de precisie van CRISPR, een gen‑gerichte methode afgeleid van bacteriën, en het signaalversterkende vermogen van PCR, de standaardmethode voor het kopiëren van DNA. In CASTSA wordt een CRISPR‑eiwit genaamd Cas12a door een kort RNA “sleuteltje” naar de HPV16‑genetische sequentie geleid. Wanneer het de exacte match vindt plus een nabijgelegen kort patroon dat het vereist, knipt Cas12a het virale DNA op een voorspelbare plek. Deze knip creëert een kenmerkend los uiteinde op één streng DNA dat dienstdoet als uniek startpunt voor amplificatie. Andere HPV‑typen, zelfs met zeer vergelijkbare sequenties, worden óf niet geknipt óf genereren niet het juiste startpunt, zodat zij niet worden geamplificeerd.
Een klein knipje omzetten in een sterk signaal
Om die CRISPR‑knip om te zetten in een detecteerbaar signaal ontwierp het team een speciaal DNA‑primer dat een terminal‑specifieke primer wordt genoemd. Deze primer hecht zich alleen correct aan de streng die door de Cas12a‑knip is geproduceerd, vouwt zich vervolgens terug als een haarspeld en helpt bij het opbouwen van een stabiel sjabloon voor PCR. Aansluitend hechten extra “universele” primersequenties zich en drijven ze een conventionele realtime PCR‑reactie aan. Cruciaal is dat amplificatie alleen plaatsvindt als Cas12a eerst zijn werk heeft gedaan en als de primer correct vouwt, waardoor er twee controlelagen ontstaan. Deze architectuur vermindert sterk de kans dat deels overeenkomend, niet‑doel‑DNA per ongeluk wordt geamplificeerd, en pakt een veelvoorkomend zwak punt aan van eerdere CRISPR‑gebaseerde tests die een afzonderlijke pre‑amplificatiestap gebruikten.
Alles in één buis, met minder fouten
Een belangrijk praktisch voordeel is dat CRISPR‑knippen en PCR‑amplificatie samen in dezelfde afgesloten buis plaatsvinden, waardoor het openen van buizen tussen stappen wordt vermeden — een belangrijke bron van contaminatie in veel laboratoriumwerkstromen. De auteurs stemden de reactiebestemmingen zorgvuldig af, met name de magnesiumconcentraties, zodat zowel Cas12a als het DNA‑kopieerenzym goed functioneren zonder spuriueuze reacties te stimuleren. Ze toonden aan dat hun one‑pot‑opstelling HPV16 betrouwbaar kan onderscheiden van verschillende andere hoogrisicotypen, waaronder HPV18, 33, 45 en 52, ook al delen deze virussen sterk geconserveerde genetische regio’s. Vergeleken met standaard realtime PCR alleen, of met CRISPR‑tests die eerst DNA amplificeren en daarna CRISPR‑detectie uitvoeren, leverde CASTSA veel minder misleidende signalen van off‑target HPV‑typen.
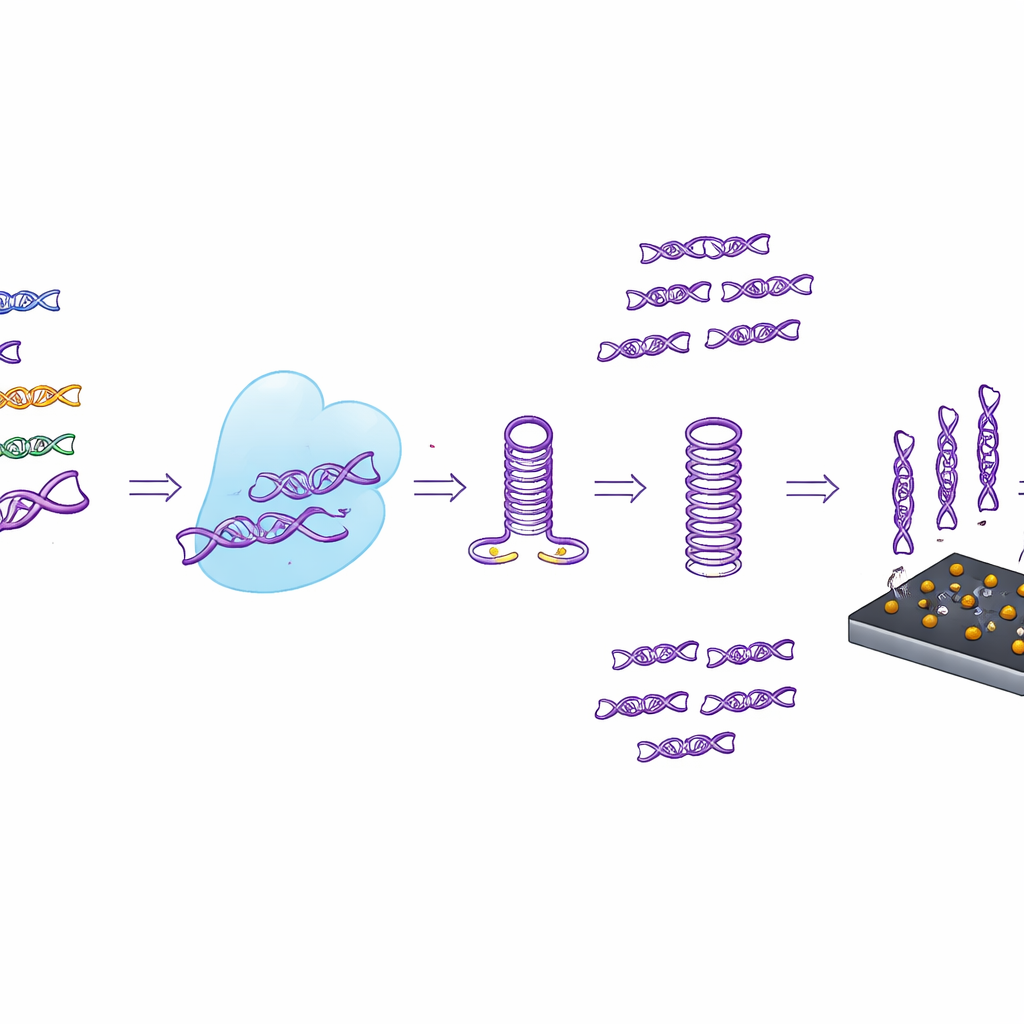
Van reageerbuis naar draagbare sensor
In plaats van uitsluitend te vertrouwen op fluorescentieaflezingen koppelden de onderzoekers CASTSA ook aan een compacte elektrochemische sensor gemaakt van laser‑geïnduceerd grafeen. Dit poreuze, zeer geleidende koolstofoppervlak is versierd met goudnanodeeltjes die vangstrengen dragen die uitsluitend ontworpen zijn om de CASTSA‑amplificatieproducten van HPV16 te binden. Wanneer deze producten vasthechten, verandert de elektrische stroom door de sensor op een meetbare manier. Door gebruik te maken van een vierelektrodenarray — drie meetpunten en één ingebouwde achtergrondcontrole — kan het apparaat ruis door niet‑specifieke hechting wegsubtraheren. In proeven detecteerde dit geïntegreerde systeem zo weinig als 18 kopieën van het HPV16‑doel per reactie, waarmee het de gevoeligheid van alleen fluorescente detectie overtrof en uitstekende reproduceerbaarheid behield.
Hoe dit HPV‑testen kan veranderen
Om te zien hoe de methode in de praktijk werkt, testte het team 20 klinische monsters waarvan bekend was dat ze HPV16 bevatten en 10 monsters van gezonde donoren. CASTSA, zowel in de fluorescentievorm als wanneer gekoppeld aan de grafeen‑gebaseerde sensor, kwam volledig overeen met standaard ziekenhuis‑PCR‑tests. Tegelijkertijd liet het een superieure capaciteit zien om andere hoogrisicotypen te negeren die vaak verwarring veroorzaken. Voor patiënten zou dit kunnen betekenen dat er minder onduidelijke resultaten zijn en dat er zekerder besluiten kunnen worden genomen over vervolgonderzoek en behandeling. Breder gezien biedt de CASTSA‑strategie — eerst CRISPR‑herkenning, daarna amplificatie, alles in één afgesloten buis — een blauwdruk voor zeer specifieke genetische tests met lage contaminatiekans die kan worden aangepast aan vele pathogenen en mutaties, vooral in situaties die snelle, betrouwbare antwoorden vereisen.
Bronvermelding: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Trefwoorden: Detectie van HPV16, CRISPR-diagnostiek, PCR-gebaseerde tests, elektrochemische biosensor, point-of-care assay