Clear Sky Science · nl
Interferometrische Image Scanning Microscopy voor label-vrije beeldvorming met 120 nm laterale resolutie in levende cellen
Levende cellen zien zonder extra kleurstoffen
De moderne biologie leunt vaak op fluorescerende labels om de verborgen architectuur binnen onze cellen zichtbaar te maken. Maar die labels kunnen cellen belasten, hun gedrag veranderen en zijn soms helemaal niet toepasbaar bij kwetsbare of lastig te manipuleren monsters. Dit artikel beschrijft een nieuwe manier om het leven in levende cellen gedetailleerd te observeren—zonder toevoeging van kleurstoffen of genetische tags—wat zachtere, langduriger en natuurlijker waarnemingen belooft van hoe cellen echt functioneren.
Cellen bekijken via hoe ze licht verstrooien
De methode bouwt voort op een familie technieken die niet op fluorescentie vertrouwen, maar in plaats daarvan meten hoe kleine structuren licht verstrooien. Een dergelijke techniek, interferometrische verstrooiingsmicroscopie (iSCAT), mengt licht dat verstrooid wordt door een nanoschaal object met een referentieweerkaatsing van een glasoppervlak. Het resulterende interferentiepatroon is buitengewoon gevoelig voor zeer kleine deeltjes zoals eiwitten, virussen of blaasjes. iSCAT werkte eerder het beste op eenvoudige, schone monsters zoals geïsoleerde deeltjes op glas. Toepassing diep in levende cellen is echter lastig geweest omdat cellen dicht en rommelig zijn: veel overlappende verstrooiingsgebeurtenissen produceren een korrelig achtergrondpatroon dat fijne details verbergt.
Twee ideeën combineren voor scherper, zachter beeld
Om deze beperkingen te overwinnen combineerden de auteurs iSCAT met een krachtige beeldvormingsstrategie genaamd image scanning microscopy (ISM). Bij ISM wordt het monster punt voor punt gescand met een gefocusseerde bundel, en in plaats van één enkele detector registreert een array van detectorpixel vele lichtelijk verschoven aanzichten van elk punt. Door deze aanzichten slim opnieuw uit te lijnen en te combineren, kan het uiteindelijke beeld verscherpt worden zonder kostbare fotonen weg te gooien. De nieuwe techniek—interferometrische image scanning microscopy, of iISM—past dit idee toe op de complexere, fasesensitieve signalen van interferometrische verstrooiing. De microscoop gebruikt een blauwe laser, speciale optiek om de lichtpolarizatie symmetrisch te maken, en een gevoelige camera om zowel verstrooid als gereflecteerd licht voor elke scanpositie vast te leggen. Een op maat gemaakte computationele workflow herverdeelt vervolgens de pixelinformatie op een manier die het golfkarakter van het signaal respecteert, wat beelden oplevert met circa 120 nanometer laterale resolutie, ongeveer twee keer fijner dan standaard diffractielimiterende optiek.
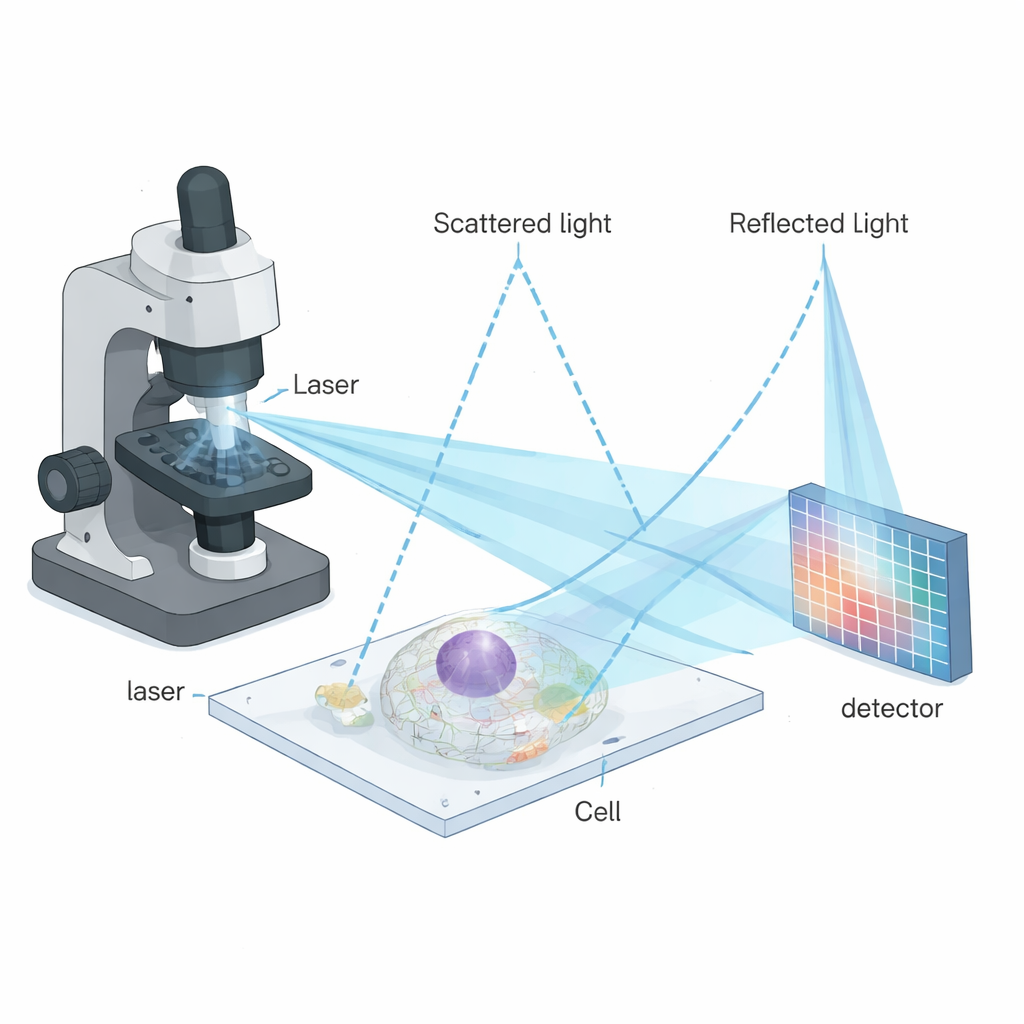
Slimme algoritmes zetten ruisachtige patronen om in heldere beelden
Aangezien interferometrische signalen zowel helderheids- als fase-informatie dragen, schieten de gebruikelijke verwerkingsmethoden uit de fluorescentiebeeldvorming tekort. De auteurs ontwierpen een adaptieve pixel-hertoewijzingsprocedure (APR) afgestemd op coherent licht. Eerst transformeren ze elk klein interferometrisch patroon in een "radiale variantie"-kaart die centra van symmetrie benadrukt zonder zich druk te maken over of het signaal positief of negatief is. Deze stap zet ingewikkelde interferentieringpatronen effectief om in beelden die zich meer gedragen als conventionele intensiteitsafbeeldingen. Daarna bepalen ze met open-source software hoeveel elk detectorpixelbeeld ten opzichte van het centrum verschoven is en schuiven ze deze weer terug voordat ze optellen. Deze verfijnde uitlijning concentreert het nuttige signaal terwijl de ruis gemiddeld wordt verlaagd, waardoor de contrast-op-ruisverhouding ongeveer een factor vier verbetert vergeleken met een streng gepinholede confocale iSCAT-afbeelding, bij hetzelfde lichtniveau.
Organellen en cytoskeletten in actie volgen
Met deze technische verbeteringen richtte het team zich op levende COS-7 cellen om te testen hoe iISM in de praktijk presteert. Bij zeer lage belichtingskracht—ongeveer tien keer lager per gefocusseerd punt dan conventionele confocale microscopen doorgaans gebruiken—konnen ze belangrijke organellen duidelijk onderscheiden: het endoplasmatisch reticulum, mitochondriën, blaasjes, het actine-cytoskelet, plasmamembraan en dunne voorste randen die lamellipodia worden genoemd. Omdat het interferometrische contrast sterk afhankelijk is van verticale positie, konden vergelijkbare organellen positief of negatief contrast vertonen, wat subtiele hoogteverschillen van slechts enkele honderden nanometers onthulde. Door tijdreeksopnamen vast te leggen, volgden ze blaasjes die bewogen en endoplasmatische reticulumtubuli die zich over meerdere minuten herconfigureerden, zonder duidelijke fotobeschadiging en zonder aanwijzingen dat de beeldvorming zelf het gedrag van de cellen verstoorde.
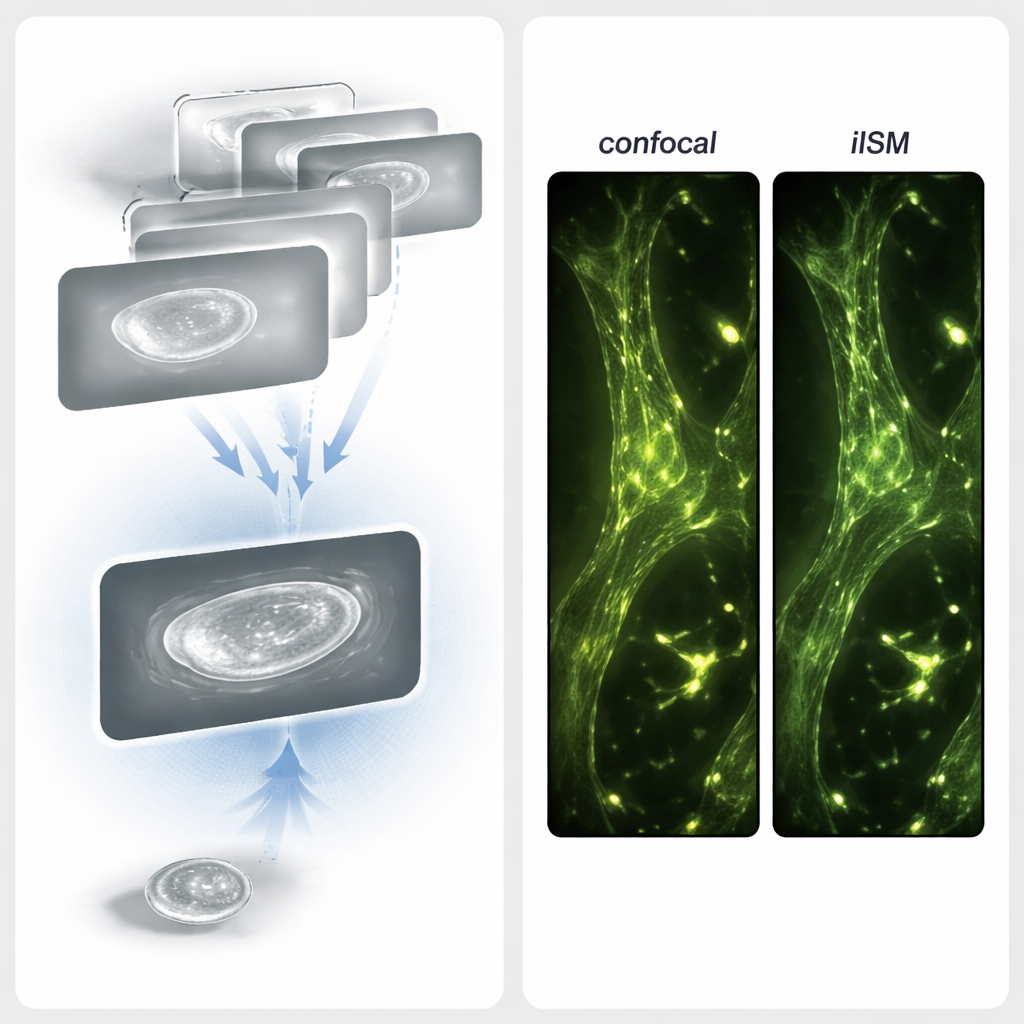
Label-vrije beelden vergelijken met fluorescerende kaarten
Om te controleren of de label-vrije beelden werkelijk overeenkomen met echte cellulaire structuren, voerden de onderzoekers ook gecombineerde iISM- en fluorescentie-ISM-metingen uit in gefixeerde cellen. Ze kleurden het actine-cytoskelet met een rood fluorescerend kleurstof en namen supergeresolveerde fluorescentiebeelden op naast label-vrije iISM-beelden van hetzelfde gebied. Wanneer ze de twee over elkaar legden, kwamen heldere actinefilamenten in het fluorescentiekanaal goed overeen met filamentachtige kenmerken in de iISM-beelden. In sommige regio's onthulde iISM zelfs aanvullende verstrooiingsdetails—zoals variaties langs filamenten of nabijgelegen onbeplakte structuren zoals focale adhesies—die in het fluorescentiekanaal onzichtbaar waren. Samen tonen deze resultaten aan dat iISM zowel bekende structuren kan bevestigen als extra informatie kan ontsluiten over onbeplakte omgevingen.
Een nieuw venster op cellen, met minder verstoring
Voor niet-specialisten is de belangrijkste boodschap dat iISM een manier biedt om fijne details binnen levende cellen te zien zonder ze kunstmatig te laten oplichten. Het combineert de gevoeligheid van interferometrische verstrooiing met het verscherpende vermogen van image scanning, en bereikt ongeveer 120-nanometer resolutie terwijl het veel minder licht gebruikt dan veel bestaande microscopen. Omdat het is opgebouwd uit componenten die al gebruikelijk zijn in geavanceerde confocale systemen, kan het in principe aan commerciële instrumenten worden toegevoegd. In de toekomst zou iISM kunnen worden gecombineerd met traditionele fluorescentie, snelle detectoren of zelfs machine-learning "virtuele kleuringen" om infecties, vrachtaanvoer of herordening van het cytoskelet in cellen te volgen onder omstandigheden die dichter bij hun natuurlijke, onaangetaste toestand liggen.
Bronvermelding: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Trefwoorden: label-vrije beeldvorming, levende-cel microscopie, interferometrische verstrooiing, superresolutie, cellulaire organellen