Clear Sky Science · nl
Synthetische lethale werking van MCL-1-remming en CAR-T-therapie bij agressief B-cellymfoom
Waarom dit belangrijk is voor kankerbehandeling
Agressieve B‑cellymfomen zijn snelgroeiende bloedkankers die vaak terugkeren na behandeling. Zelfs krachtige nieuwe benaderingen zoals CAR‑T-celtherapie, waarbij de eigen immuuncellen van een patiënt worden geherprogrammeerd om kanker aan te vallen, falen na verloop van tijd bij grofweg de helft van de patiënten. Deze studie onderzoekt een manier om die zwakte om te zetten in een kracht: het gebruik van een geneesmiddel dat zich richt op een belangrijk overlevingsproteïne in lymfomacellen om tumoren zowel te doden als de overgebleven cellen makkelijker te maken voor CAR‑T-cellen om af te maken.
Het probleem van hardnekkige lymfomacellen
Agressieve B‑cellymfomen worden vaak gedreven door overmatige activiteit van een gen dat MYC heet, dat cellen aanzet tot snelle deling en hen ook helpt te verbergen voor het immuunsysteem. Standaardbehandelingen en zelfs CAR‑T-therapie kunnen kleine eilandjes van lymfomacellen achterlaten die tolerant zijn voor geneesmiddelen en later herval veroorzaken. Deze “persisterende” en resistente cellen leven in een tumoromgeving vol onderdrukkende immuuncellen die doder‑T-cellen op afstand houden. De auteurs vroegen zich af of het blokkeren van MCL‑1, een eiwit waarop lymfomacellen vertrouwen om te voorkomen dat ze zichzelf vernietigen, een verborgen zwakte in dit systeem zou kunnen blootleggen.
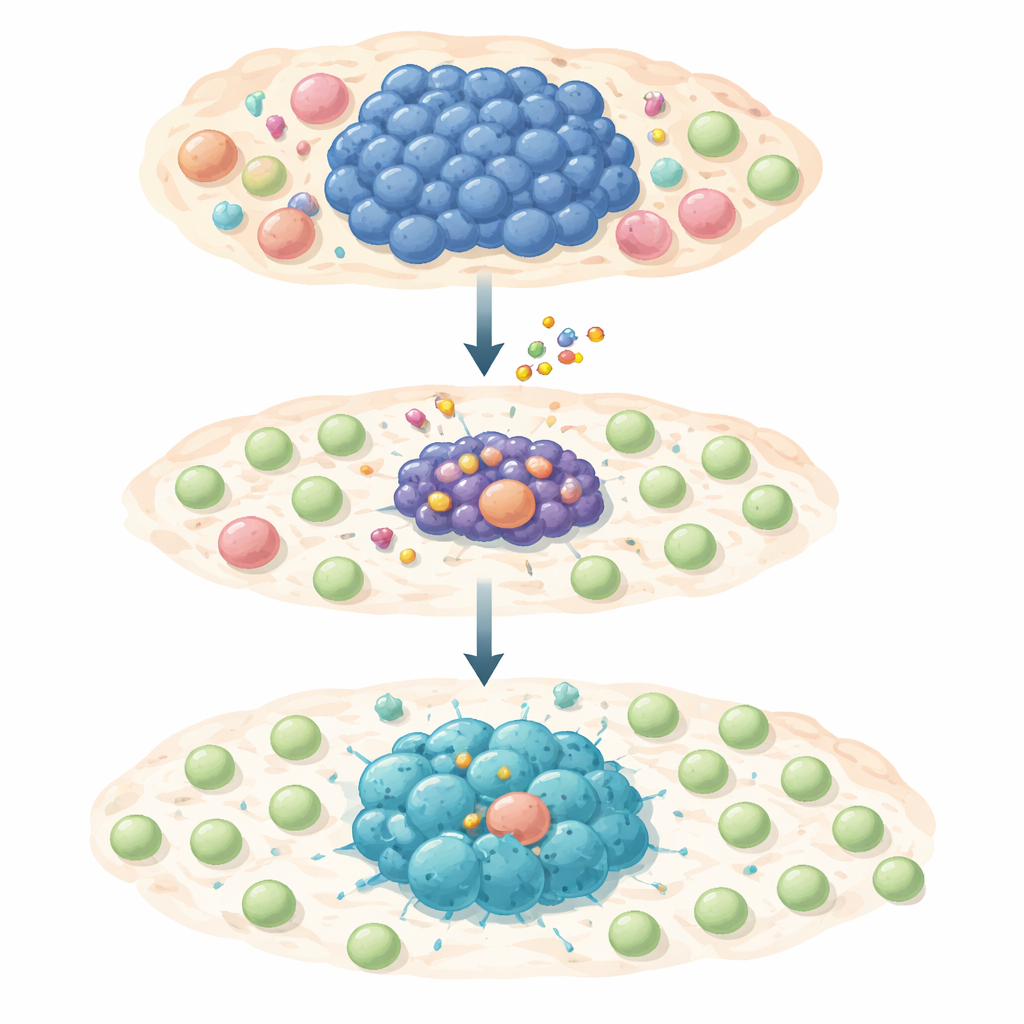
Een tweeledige aanval op tumorovertleving en verberging
Het team testte een selectief MCL‑1-remmend middel, S63845, in een grote reeks menselijke lymfomacellijnen die afhankelijk zijn van MYC. De meeste van deze kankercellen waren zeer gevoelig voor het middel en ondergingen geprogrammeerde celdood wanneer MCL‑1 werd geblokkeerd. Een klein deel overleefde echter kortdurende of langdurige blootstelling en werd geneesmiddeletolerant of volledig resistent. Toen de onderzoekers deze overlevenden in detail bestudeerden, ontdekten ze dat de MYC-activiteit werd verminderd terwijl een ander molecuul, STAT1, en het daarmee samenhangende interferon‑alarmpad werden aangezet. Deze verschuiving zette genen aan die ontstekingssignalen en chemokinen produceren — moleculaire “fakkels” die T‑cellen naar het tumorgebied kunnen lokken.
Het immuunmicroklimaat heractiveren
Om te zien hoe dit zich in een levend organisme uitpakt, behandelden de auteurs muizen met MYC‑gedreven lymfomen met een lage dosis van de MCL‑1-remmer. Het middel verkleinde de tumorlading terwijl normale B‑cellen werden gespaard, maar het effect ging verder dan louter verkleining van de massa. Behandelde tumoren toonden meer CD4‑ en CD8‑T‑cellen, minder uitgeputte T‑cellen, minder regulerende T‑cellen en minder onderdrukkende myeloïde cellen, allemaal tekenen van een immuunvriendelijker omgeving. Enkelcel-RNA‑sequencing van tumor- en omliggende cellen bevestigde dat resterende lymfomacellen verminderde MYC‑niveaus, verhoogde STAT1-activiteit en sterkere interferon- en ontstekingssignalen toonden, terwijl het omliggende weefsel werd herbevolkt met actieve T‑ en natural‑killercellen in plaats van onderdrukkende cellen.
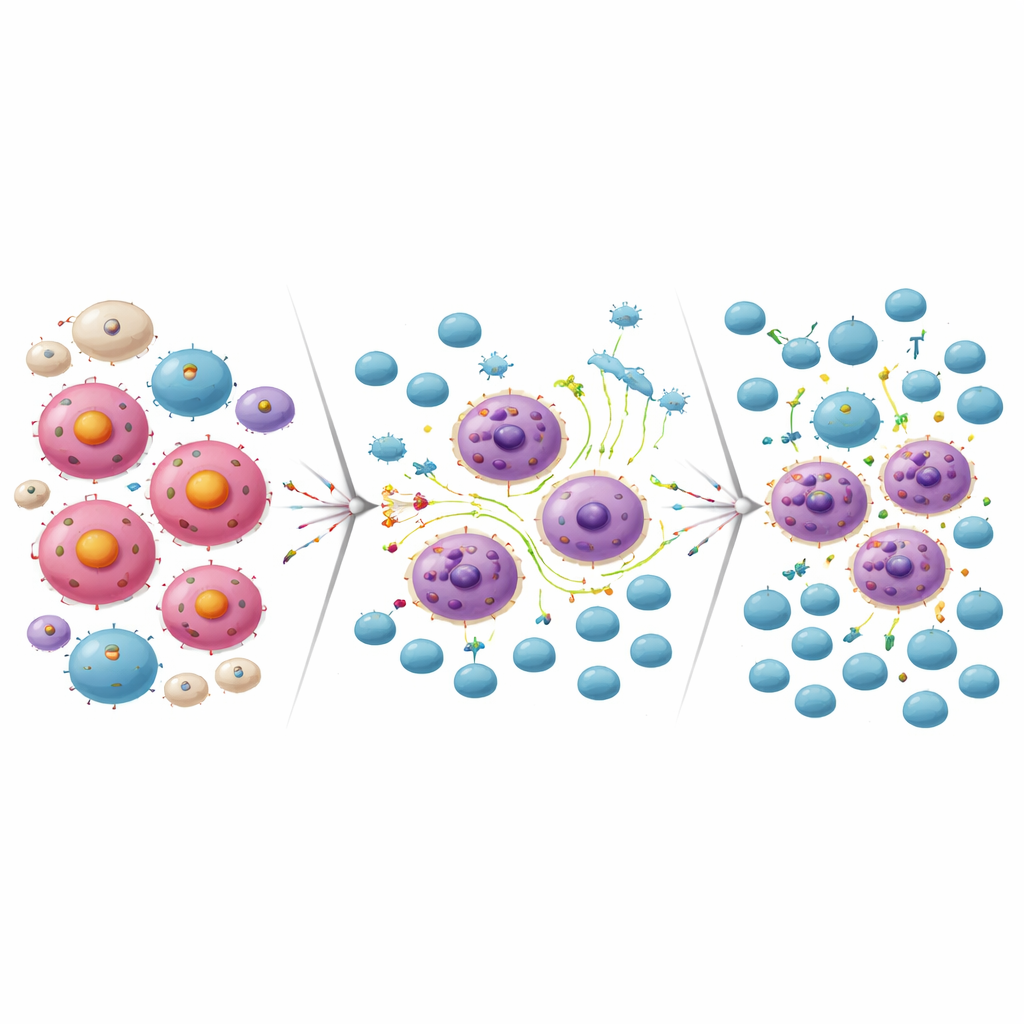
Weerstand omzetten in een opening voor CAR‑T‑cellen
Dezelfde ontstekingsachtige herprogrammering die sommige lymfomacellen hielp om MCL‑1-blokkade te overleven, maakte ze ook gevoeliger voor immuunaanval. In het lab doodden CD19‑gerichte CAR‑T‑cellen efficiënt lymfomacellen die resistent waren geworden tegen het MCL‑1‑middel. Omgekeerd waren lymfomacellen die resistent waren gemaakt tegen CD19 CAR‑T‑therapie zeer gevoelig voor de MCL‑1-remmer. Wanneer de onderzoekers een subletale dosis van het MCL‑1‑middel combineerden met CAR‑T‑cellen in celcultuur, gaven de twee behandelingen samen veel meer doding van lymfomacellen dan elk afzonderlijk. In muismodellen leidde het toedienen van de MCL‑1-remmer gevolgd door CD19 CAR‑T‑cellen tot bijna volledige tumoruitroeiing en een significant langere overleving vergeleken met enkelvoudige behandelingen.
Een één-twee klap met curatieve potentie
Simpel gezegd suggereert de studie een “één‑twee klap”-strategie. Eerst knijpt een MCL‑1‑blokkerend middel het merendeel van het lymfoom weg en dwingt het overgebleven kankercellen in een ontstoken, goed zichtbare staat die T‑cellen aantrekt en beschermende immuunbarrières wegneemt. Ten tweede benutten CD19 CAR‑T‑cellen deze nieuw blootgelegde zwakte om de resterende ziekte uit te roeien. Door zowel de interne overlevingsbedrading van de tumor als zijn beschermende omgeving aan te pakken, kan deze gecombineerde benadering recidieven verminderen en agressieve B‑cellymfomen dichter bij langdurige remissie brengen.
Bronvermelding: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Trefwoorden: B-cellymfoom, CAR-T-therapie, MCL-1-remming, tumormicro-omgeving, medicatieresistentie