Clear Sky Science · nl
Alnuctamab, een bivalent T-cel engager gericht op B-celrijpingsantigeen voor patiënten met terugkerend of refractair multipel myeloom: resultaten van een fase 1, eerste-in-mens-studie
Waarom dit nieuwe kankergeneesmiddel ertoe doet
Voor mensen met multipel myeloom, een bloedkanker die na behandeling vrijwel altijd terugkeert, kan elke nieuwe optie meer tijd en een betere levenskwaliteit betekenen. Deze studie onderzoekt een volgende‑generatie immuuntherapie genaamd alnuctamab, ontworpen om de eigen verdedigingscellen van het lichaam te helpen myeloomcellen opsporen en doden. Het onderzoek stelt een praktische vraag die zowel patiënten als artsen raakt: kan deze krachtige therapie als een eenvoudige onderhuidse injectie worden toegediend, met sterke antikankereffecten maar minder gevaarlijke bijwerkingen?
Een slimme manier om het immuunsysteem om te leiden
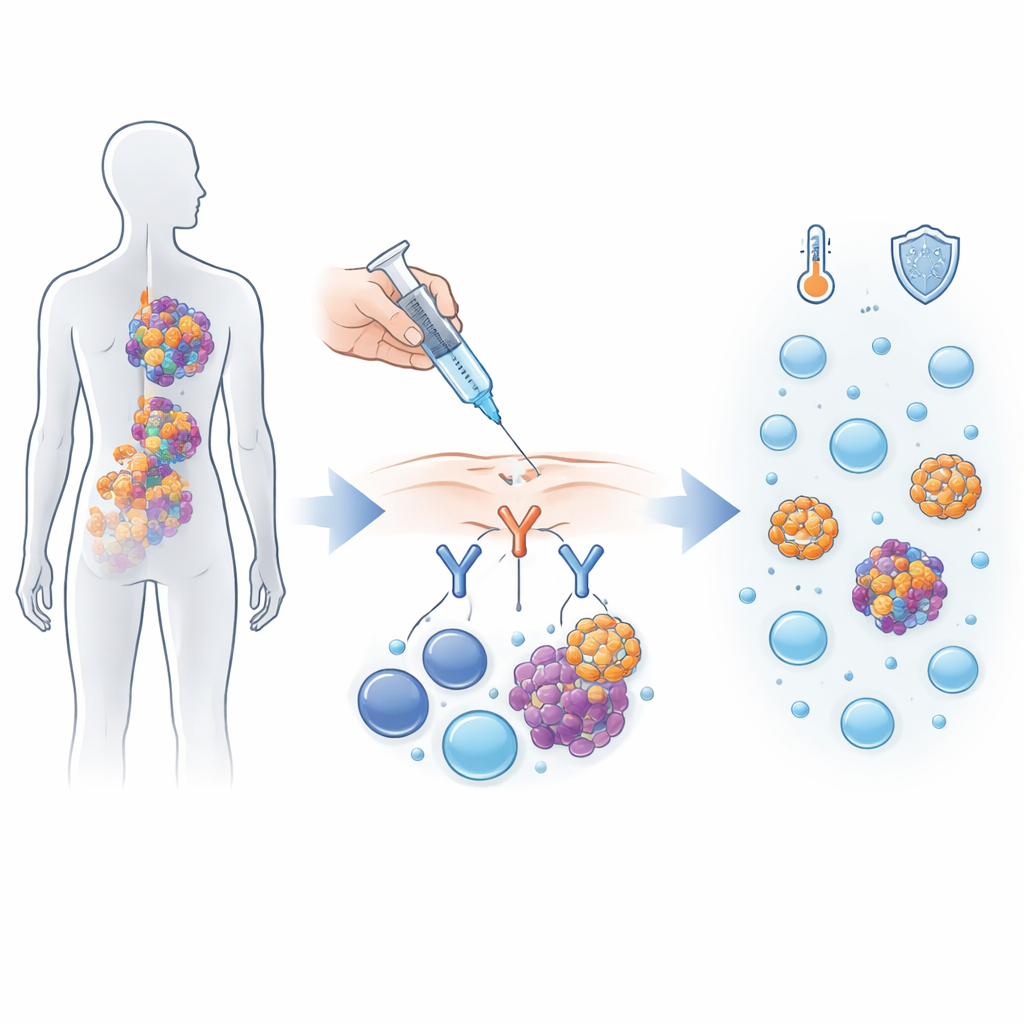
Alnuctamab behoort tot een nieuwe klasse geneesmiddelen die fungeren als moleculaire koppelaars tussen kankercellen en immuuncellen. Multipel myeloomcellen dragen een merker genaamd BCMA op hun oppervlak, terwijl de T‑cellen van het lichaam een andere merker, CD3, dragen. Alnuctamab is opgebouwd met twee “armen” die aan BCMA hechten en één arm die aan CD3 hecht, waardoor T‑cellen in nauw contact met myeloomcellen worden gebracht zodat ze die kunnen aanvallen. In deze eerste‑in‑mens‑trial kregen 165 mensen met myeloom dat was teruggekeerd na ten minste drie verschillende soorten behandeling alnuctamab, óf via intraveneuze toediening via een ader, óf via subcutane injectie onder de huid.
Van infuus naar injectie
In het begin werd het middel via de ader gegeven, maar deze aanpak veroorzaakte intensere immuunreacties, waaronder een levensbedreigende episode van een complicatie die cytokine release syndrome heet, waarbij het immuunsysteem plots grote hoeveelheden ontstekingssignalen afgeeft. Vanwege deze veiligheidszorgen en slechts bescheiden voordeel schakelde de studie over op onderhuidse dosering, die het middel geleidelijker vrijgeeft. Vijfennegentig patiënten werden op deze manier behandeld met een "step‑up" schema: kleine startdoses gevolgd door hogere streefdoses, waarbij de injectiefrequentie in de loop van de tijd langzaam werd verminderd van wekelijks tot eenmaal per vier weken als de behandeling werd voortgezet.
Hoe patiënten het deden en wat ze tegenkwamen
Onder alle patiënten die de onderhuidse injecties kregen, zagen ongeveer 59% dat hun kanker met ten minste de helft kromp, en bijna de helft werd "minimal residual disease negatief", wat betekent dat zeer gevoelige tests geen myeloomcellen meer in hun beenmerg konden vinden. Bij de aanbevolen dosis van 30 milligramen waren de reacties nog sterker: ongeveer 71% reageerde en meer dan de helft bereikte minimal residual disease‑negativiteit. Veel patiënten behielden de ziektecontrole bijna een jaar of langer, zelfs toen het doseringsschema minder intensief werd. Bijwerkingen kwamen vaak voor maar waren grotendeels beheersbaar. Koortsachtige immuunreacties traden op bij ongeveer drie van de vijf patiënten, maar alle waren mild of matig. Lage aantallen witte bloedcellen en infecties deden zich voor, wat zowel de kracht van het middel als de kwetsbaarheid van de patiënten weerspiegelt, maar ernstige infecties waren minder frequent dan gerapporteerd bij meerdere vergelijkbare middelen.
Waarom de injectieroute veiliger was
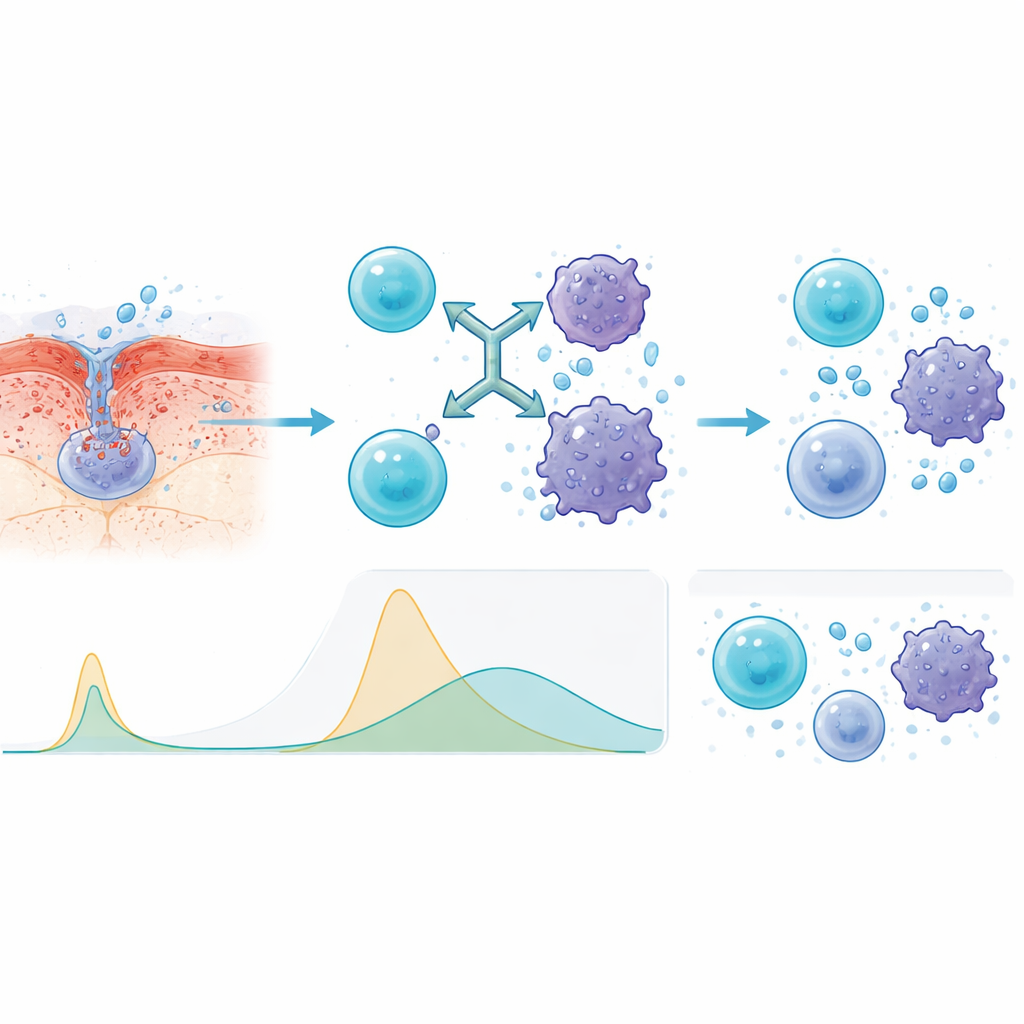
Om te begrijpen waarom de onderhuidse methode beter presteerde, maten de onderzoekers immuunsignaalmoleculen in het bloed. In vergelijking met infusie via een ader veroorzaakten injecties tragere, lagere pieken in belangrijke ontstekingssignalen zoals interleukines en tumornecrosefactor. Dit vlakker profiel betekent dat het immuunsysteem nog steeds tegen de kanker wordt geactiveerd, maar zonder dezelfde plotselinge uitbarsting die patiënten levensgevaarlijk ziek kan maken. Het team vond ook dat mensen wier bloed bij aanvang lagere niveaus van afgescheiden BCMA toonde — een teken van minder agressieve of minder gevorderde ziekte — geneigd waren beter te reageren en langer in remissie te blijven.
Wat dit betekent voor toekomstige myeloombehandeling
Hoewel het bedrijf sindsdien heeft besloten de ontwikkeling van alnuctamab om strategische redenen niet voort te zetten, zijn de lessen uit deze trial belangrijk. De studie toont aan dat een zorgvuldig ontworpen immuunengager als een eenvoudige injectie kan worden toegediend, op een schema dat in de loop van de tijd minder belastend wordt, en toch diepe en duurzame responsen oplevert bij veel mensen met moeilijk te behandelen myeloom. Het suggereert ook dat het stapsgewijs verhogen van de dosis en het vermijden van scherpe pieken in immuunactivatie ernstige reacties kan beperken zonder de antikankerwerking te verminderen. Deze inzichten zullen waarschijnlijk het ontwerp van toekomstige immuun-gebaseerde behandelingen sturen en bieden hoop dat meer patiënten met terugkerend myeloom effectieve therapieën kunnen krijgen die niet alleen krachtig, maar ook veiliger en makkelijker zijn om mee te leven.
Bronvermelding: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Trefwoorden: multipel myeloom, immunotherapie, bispecifiek antilichaam, BCMA, T-cel engager