Clear Sky Science · nl
Single-cell transcriptie-atlas onthult verschillende immuun-chondrocyt wisselwerkingsmechanismen bij temporomandibulaire gewrichtsartrose veroorzaakt door verschillende typen occlusale afwijkingen
Waarom je kaakgewricht ertoe doet
De kleine gewrichten voor je oren, de temporomandibulaire gewrichten (TMG), maken praten, kauwen, gapen en lachen mogelijk. Als ze artrose ontwikkelen, kunnen alledaagse bewegingen pijnlijk en moeilijk worden. Deze studie gebruikt geavanceerde single-cell genanalyse bij muizen om deze kaakgewrichten cel voor cel te onderzoeken en onthult hoe verschillende beetproblemen uiteenlopende vormen van schade veroorzaken — en hoe dat kan leiden tot preciezere behandelingen.
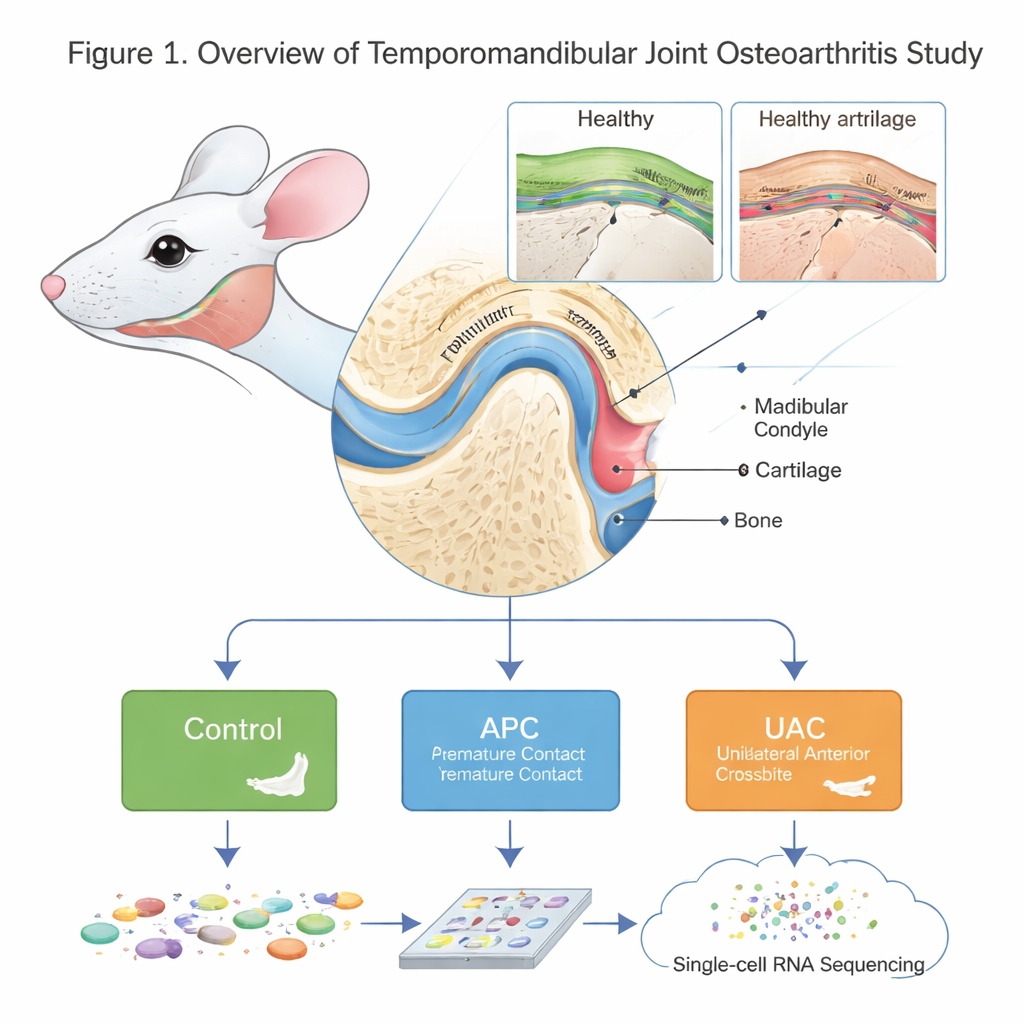
Nauwkeurig kijken naar een klein maar complex gewricht
Het TMG is geen eenvoudige scharnier. Het afgeronde uiteinde, de mandibulaire condylus, is bedekt met een speciaal type kraakbeen en wordt ondersteund door het onderliggende bot. Artrose in dit gewricht (TMJOA) veroorzaakt pijn, stijfheid en functieverlies, maar de microscopische en moleculaire oorzaken zijn moeilijk te ontrafelen geweest. De auteurs creëerden een gedetailleerde "cell atlas" van de muiscondylus in gezondheid en ziekte met behulp van single-cell RNA-sequencing, een techniek die uitleest welke genen actief zijn in duizenden individuele cellen. Ze vergeleken gezonde muizen met twee modellen van beetonevenwicht — anterior premature contact (APC), waarbij de voortanden te vroeg op elkaar komen, en unilateral anterior crossbite (UAC), waarbij één zijde van de voortanden verkeerd op elkaar komt — beide bekend om overbelasting van het kaakgewricht te veroorzaken.
Veel soorten kraakbeencellen, niet slechts één
Traditioneel is condylair kraakbeen beschreven in brede lagen — prolifereerende, rijpe en hypertrofische cellen. Deze studie laat zien dat de werkelijkheid veel gevarieerder is. Het team identificeerde meerdere chondrocyt-subtypen, elk met eigen genactiviteit en waarschijnlijke rol. Er waren progenitorcellen dicht bij het oppervlak die zich gedragen als een reparatiepool, fibrotische chondrocyten betrokken bij littekenachtig matrix en genezing, ontstekingsgeassocieerde chondrocyten die ontstekingssignalen produceren, mineralisatie-geassocieerde en hypertrofische chondrocyten die helpen kraakbeen in bot om te zetten, en herstelbevorderende cellen die stress en ontsteking dempen. In gezonde gewrichten liggen deze subtypen in een geordend ruimtelijk patroon en volgen ze een vloeiende ontwikkelings"traject" van progenitor naar meer rijpe toestanden.
Wanneer beetproblemen de cellulaire orde van het gewricht verstoren
Zowel APC- als UAC-modellen leidden tot dunner kraakbeen, oppervlakte-ruwheid en typische artroseachtige laesies in de condylus. Op cellulair niveau daalde het aandeel chondrocyten terwijl immuuncellen toenamen. Bij APC was er een toename van bepaalde mineraliserende en hypertrofische chondrocyten en een verstoring van de normale overgang van progenitor naar rijpe cellen. Bij UAC was er ook een toename van fibrotische en herstelbevorderende chondrocyten, wat wijst op een sterkere poging tot reparatie en remodellering. Microscopie bevestigde dat cellen hun geordende lagen verloren en compact en ongeorganiseerd werden in ziek kraakbeen, wat overeenkomt met de verstoorde ontwikkelingspaden afgeleid uit de genexpressiegegevens.
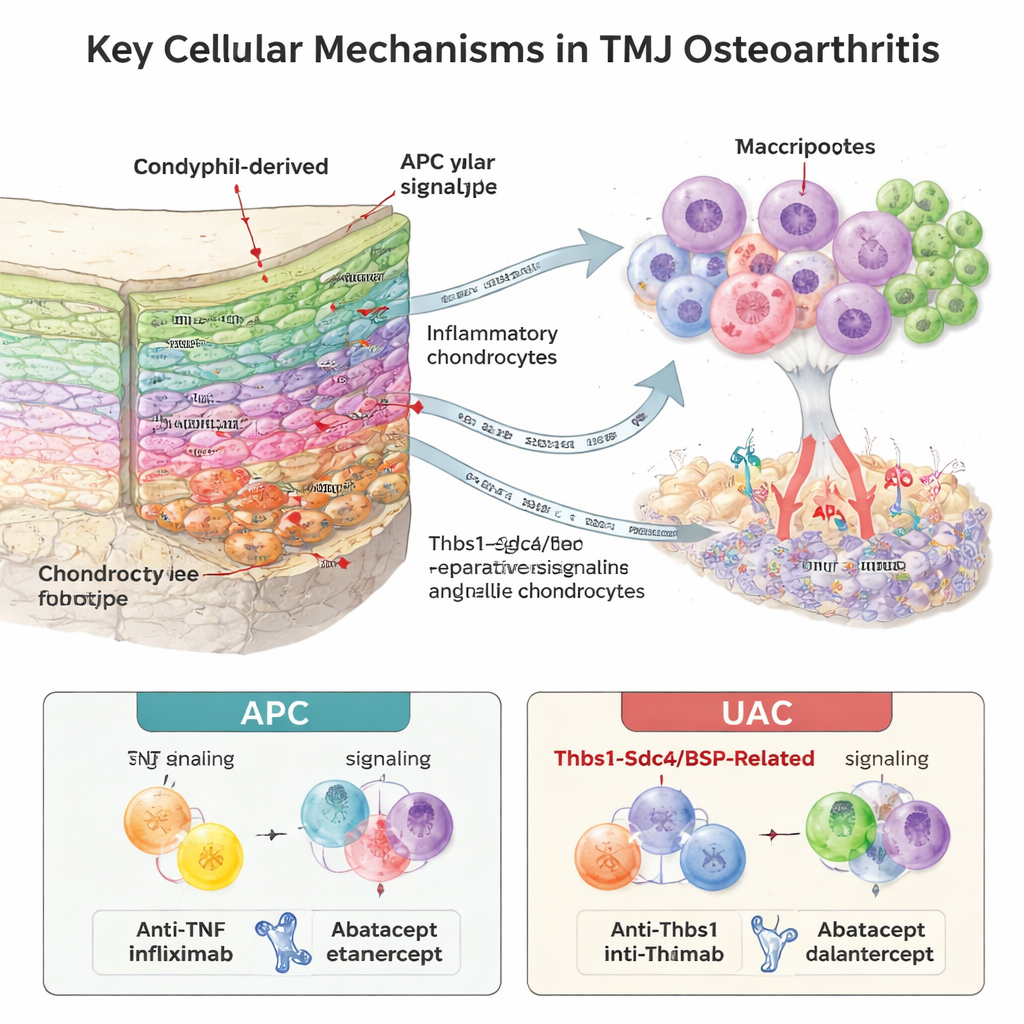
Immuuncellen, bloedvaten en kraakbeen communiceren met elkaar
Het ondersteunende bot en merg van de condylus herbergden een verrassend rijk immuun "micro-omgeving." De onderzoekers vonden negen immuunceltypes, met neutrofielen (een snel reagerende witte bloedcel) die sterk uitbreidden in zieke gewrichten, vooral een specifieke rijpingsfase. Door te analyseren welke signaalmoleculen en receptoren gezamenlijk werden uitgedrukt, concludeerden ze dat er intense "crosstalk" was tussen immuuncellen en chondrocyten. In het APC-model werden neutrofielen de belangrijkste bron van TNF-alpha, een krachtig ontstekingssignaal, dat sterke schadelijke boodschappen naar kraakbeencellen stuurde. In het UAC-model ontstond een ander patroon: bot- en kraakbeen-gerelateerde signalen met bot sialoproteïne (BSP) en het Thbs1–Sdc4-pad waren prominenter, en deze waren nauw verbonden met nieuwe bloedvatgroei aan de grens tussen kraakbeen en bot. Gebieden rijk aan BSP overlappen met markers van angiogenese, wat suggereert dat binnendringende vaten en aangetrokken immuuncellen gezamenlijk kraakbeenerosie aansturen.
Op maat gemaakte behandelingen voor verschillende gewrichtsbelastingen
Om te testen of deze verschillende signalen echt belangrijk zijn, behandelde het team muizen tijdens de ziekteontwikkeling met geneesmiddelen die specifieke paden blokkeren. Bij APC-geïnduceerde TMJOA beschermde het blokkeren van TNF-alpha met het geneesmiddel etanercept duidelijk het kraakbeen, terwijl een middel dat neutrofiel-aantrekkende receptoren remt (Navarixin) weinig verschil maakte. Daarentegen verlichtte Navarixin bij UAC-geïnduceerde TMJOA aanzienlijk de kraakbeenschade, in overeenstemming met een ziekteproces dat meer afhankelijk is van neutrofiel-gedreven vaatinnesteling en remodellering, terwijl etanercept een zwakker effect had. Deze bevindingen suggereren dat TMJ-artrose geen eenduidige ziekte is maar een verzameling verwante aandoeningen gevormd door de manier waarop het gewricht wordt belast, en dat effectieve therapieën mogelijk afgestemd moeten worden op de specifieke mechanische en cellulaire patronen die bij elke patiënt spelen.
Wat dit betekent voor mensen met kaakpijn
Voor iemand die worstelt met kaakknakken, pijn of beperkt openen benadrukt dit onderzoek twee kernideeën. Ten eerste wordt het kaakgewricht in stand gehouden door een diverse gemeenschap van kraakbeen- en immuuncellen die het weefsel kunnen beschermen of beschadigen, afhankelijk van hoe ze geactiveerd worden. Ten tweede kunnen verschillende beetproblemen deze gemeenschap in uiteenlopende schadelijke richtingen duwen — de ene meer gestuurd door klassieke ontsteking, de andere door abnormale bloedvatgroei en bot-kraakbeen remodellering. Op de lange termijn kan dit soort single-cell kaartlegging tandartsen en artsen helpen verder te gaan dan one-size-fits-all behandelingen, naar benaderingen die beetcorrectie combineren met gerichte medicijnen gekozen op basis van het specifieke patroon van gewrichtsschade van de patiënt.
Bronvermelding: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
Trefwoorden: temporomandibulair gewricht artrose, single-cell RNA-sequencing, chondrocyten, neutrofielen, occlusale afwijking