Clear Sky Science · nl
Implantatie wekt peri-implantaat osteogene potentie via Snx5-EGFR-as-gemedieerde mechanotransductie
Waarom het behoud van de kaak na tandverlies belangrijk is
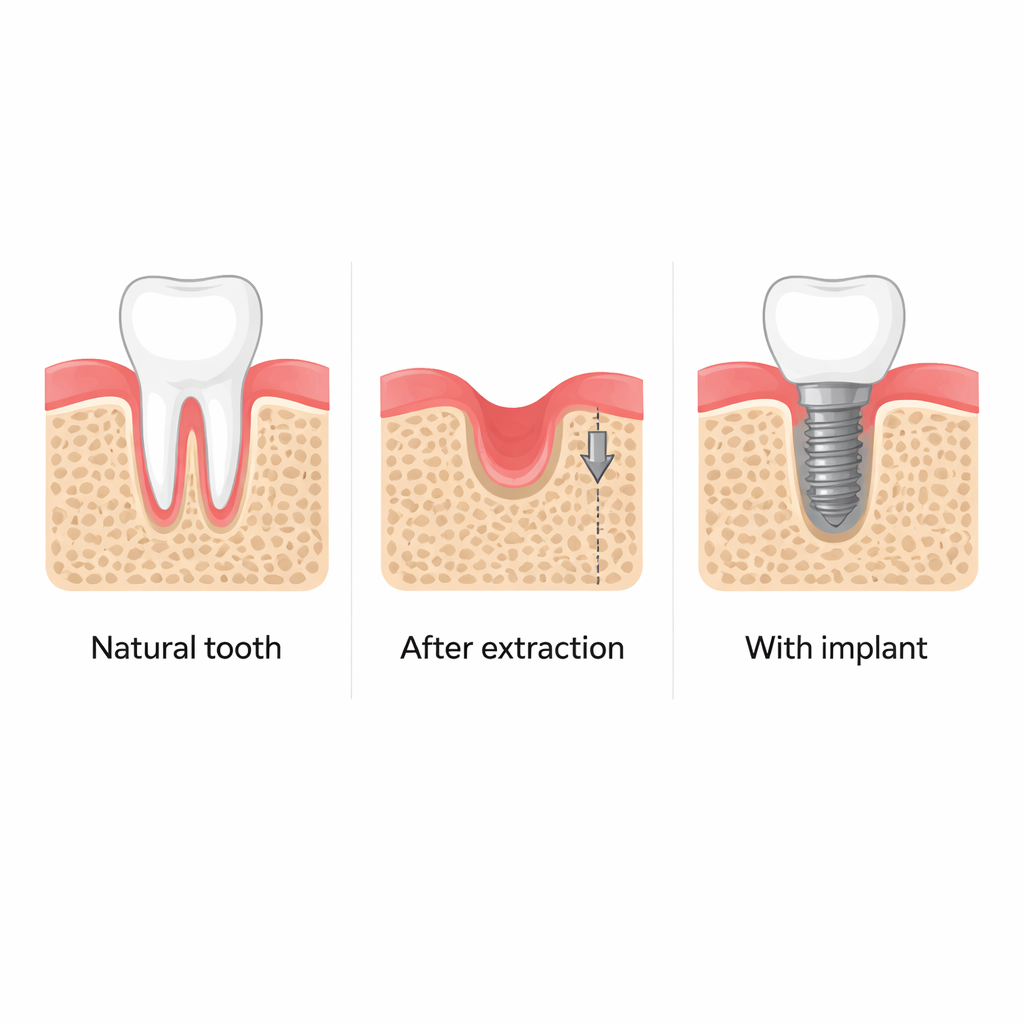
Wanneer een tand wordt getrokken, slinkt het omliggende kaakbot vaak, waardoor het later moeilijker wordt om stabiele tandimplantaten te plaatsen en het gezichtsvorm kan veranderen. Tandartsen merkten al langer dat het plaatsen van een implantaat in een vers extractiegat dit bot lijkt te behouden, zelfs voordat het implantaat wordt belast met kauwen. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe „wekt” het plaatsen van het implantaat zelf het herstelmechanisme van het bot en kunnen we dat proces benutten om kaakbotregeneratie te verbeteren?
Implantaten als stille botbeschermers
Klinische scans van patiënten en gedetailleerde experimenten in muizen bevestigen dat het plaatsen van een tandimplantaat kort na extractie helpt de hoogte en dikte van het omliggende kaakbot te behouden. Daarentegen verliezen extractieholtes die vanzelf genezen in enkele maanden aanzienlijk bot. Rond implantaten vonden de onderzoekers meer onrijpe botvormende cellen (osteoprogenitoren), wat erop wijst dat het weefsel naast de metalen staaf biologisch actiever is. Deze verhoogde activiteit lijkt niet te worden aangedreven door kauwkrachten, maar door de ongebruikelijke mechanische spanningen die ontstaan wanneer een strak implantaat in iets te kleine botruimte wordt geschroefd.
Een verborgen schakel binnen botstamcellen
Het team richtte zich op een speciale groep beenmergstamcellen gemarkeerd door een eiwit genaamd LepR, dat bekendstaat als belangrijke leverancier van nieuw bot bij volwassenen. Door genactiviteit in deze cellen te vergelijken tussen normaal bot, bot naast implantaten en cellen die in het laboratorium mechanisch werden belast, identificeerden ze één molecuul: sorting nexin 5 (Snx5), waarvan de niveaus consequent daalden bij aanwezigheid van mechanische signalen. In gebieden rond implantaten waren LepR-cellen met lage Snx5-niveaus vaker voorzien van markeringen van vroeg botopbouwende cellen, wat suggereert dat het terugschakelen van Snx5 deze stille stamcellen naar een actieve botopbouwende toestand helpt duwen.
Als de schakel kapot is, kan het bot krachten niet goed waarnemen
Om te onderzoeken wat Snx5 daadwerkelijk doet, gebruikten de onderzoekers muizen en stamcellen zonder dit eiwit. Zonder Snx5 toonden de stamcellen een sterke aangeboren neiging om bot te vormen, zelfs zonder extra stimulatie. Maar wanneer de wetenschappers mechanische rek toepasten—dat de spanningen nabij een implantaat nabootst—verhoogden normale cellen hun botvormende activiteit aanzienlijk, terwijl Snx5‑deficiënte cellen nauwelijks reageerden. In levende muizen veroorzaakten implantaten bij normale dieren duidelijke nieuwe botgroei rond de titaniumstaaf. Daarentegen kregen muizen zonder Snx5 geen extra botvorming na implantatie, wat aantoont dat Snx5 cruciaal is om mechanische signalen om te zetten in aanvullende botreparatie en niet zozeer voor de basale botvorming zelf.
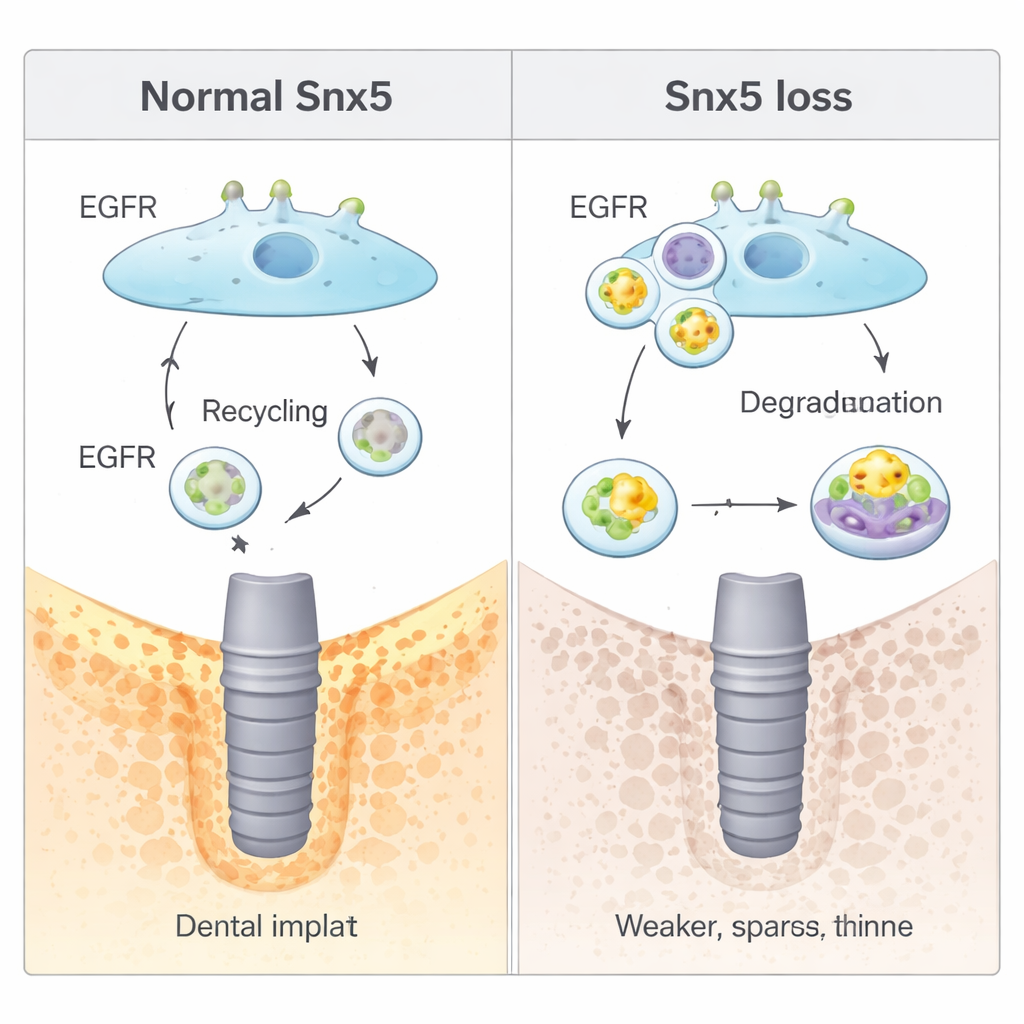
Hoe een recyclingroute botsignalen reguleert
De studie onthulde vervolgens hoe Snx5 op moleculair niveau werkt. Veel groeisignalen reizen via receptoren aan het celoppervlak die voortdurend worden geïnternaliseerd en vervolgens ofwel worden gerecycled of afgebroken. Snx5 behoort tot een familie van „sorterende” eiwitten die dit verkeer begeleiden. Hier bleek Snx5 het epidermale groeifactorreceptor (EGFR)—een belangrijke regelaar van celgroei en botdifferentiatie—terug naar het celmembraan te leiden nadat het was geïnternaliseerd. Wanneer Snx5 ontbrak, werd meer EGFR naar de „spijsverterings”compartimenten van de cel (lysosomen) geleid en afgebroken. Dit verminderde EGFR-signaal onverwacht de basale botvorming versterkt, maar liet de cellen minder goed hun gedrag aanpassen wanneer mechanische krachten veranderden. Geneesmiddelen die EGFR kunstmatig activeerden dempten de extra botvorming die zonder Snx5 werd gezien, terwijl middelen die lysosomale afbraak blokkeerden EGFR‑signalen herstelden en opnieuw de botopbouw verminderden.
Wat dit betekent voor toekomstige implantaatpatiënten
Voor leken suggereert deze bevinding dat de kaak een ingebouwd systeem bevat dat de subtiele duw- en trekkrachten kan waarnemen die ontstaan wanneer een implantaat wordt geplaatst en dit kan vertalen naar extra botgroei. Snx5 werkt als een verkeersleider die een belangrijke groeireceptor, EGFR, op het juiste niveau laat circuleren zodat botstamcellen die mechanische fluisteringen kunnen „horen” en erop reageren. Wanneer deze verkeersleider is veranderd, kan bot gemakkelijker bij rust vormen maar verliest het zijn fijn afgestemde reactie op krachten. Inzicht in deze Snx5–EGFR-as opent de deur naar nieuwe behandelingen—geneesmiddelen of oppervlaktecoatings op implantaten—die de mechanische gevoeligheid van het bot kunnen aanpassen, waardoor kaakbeenderen beter behouden blijven en het succes van implantaten in uitdagende klinische situaties kan verbeteren.
Bronvermelding: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Trefwoorden: tandimplantaten, kaakbeenregeneratie, mechanotransductie, botstamcellen, EGFR-signaalgeving