Clear Sky Science · nl
DNA- en RNA-gebaseerde ampliconsequencing van gekoppelde supragingivale en dentine-laesieplaque bij kinderen met ernstige vroegkinderlijke cariës
Waarom diepe tandbederf bij peuters ertoe doet
Tandbederf bij zeer jonge kinderen is veel meer dan een cosmetisch probleem. Ernstige vroegkinderlijke cariës (S-ECC) kan melktanden vernietigen, hevige pijn veroorzaken, slaap en eten verstoren en zelfs behandeling onder algemene anesthesie noodzakelijk maken. Deze studie stelt een eenvoudige maar cruciale vraag: welke microben zijn niet alleen aanwezig, maar beschadigen actief de tanden van kinderen diep in de cariëslaesies, en hoe verschillen zij van de microben op het tandoppervlak?
Voorbij de gebruikelijke verdachten kijken
Decennialang kreeg één hoofdschuldige, Streptococcus mutans, de meeste schuld voor cariës. Tandartsen en wetenschappers weten nu echter dat tandbederf wordt aangedreven door hele bacteriegemeenschappen die suikers verteren en zuren produceren. Bij S-ECC verspreidt de aantasting zich van het buitenste glazuur naar de zachtere binnenste dentine‑laag en holt de tand als het ware van binnenuit uit. Het team achter deze studie richtte zich op die diepe schadezone bij kinderen onder de zes jaar en vergeleek de bacteriën in het dentine van sterk aangetaste tanden met de bacteriën op het nabijgelegen tandoppervlak, de supragingivale plaque.
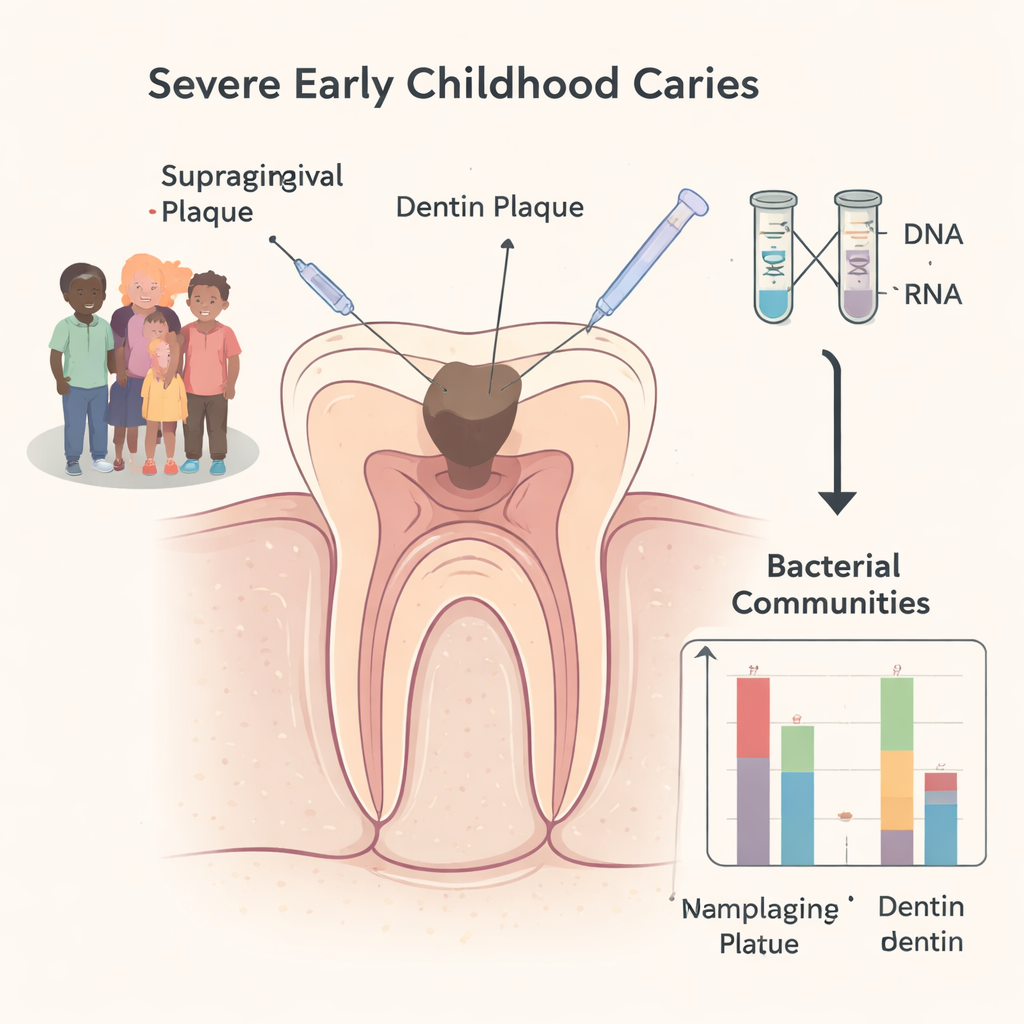
Monstername: kleine patiënten, laag voor laag
De onderzoekers werkten met 13 kinderen die meerdere extracties voor S-ECC onder algemene anesthesie nodig hadden. Van elk kind verzamelden zij twee monsters van dezelfde tand: plaque van het buitenoppervlak en plaque die uit het diepe dentine werd geschraapt nadat de tand was verwijderd. Vervolgens gebruikten ze moderne genetische technieken om fragmenten van een bacterieel merker-gen, het 16S rRNA-gen, te lezen in twee vormen. De ene vorm kwam van DNA, wat onthult welke soorten aanwezig zijn, levend of dood. De andere kwam van RNA, dat snel afbreekt en alleen door actieve cellen wordt geproduceerd, en biedt daarmee inzicht in welke bacteriën op dat moment actief en metabolisch “aan” zijn.
Een eenvoudiger maar meedogenlozere diepe-tandomgeving
Toen het team de oppervlakte- en diepe-dentinegemeenschappen vergeleek, vonden ze dat de diepe laesies minder soorten bacteriën herbergden maar meer op elkaar leken van kind tot kind. Met andere woorden: naarmate de aantasting naar binnen vordert, wordt de gemeenschap minder divers en uniformer, waarbij een smallere groep taaie microben de overhand krijgt. Deze overlevenden zijn goed aangepast aan het leven in een donkere, beschutte, zuurstofarme ruimte die wordt overstroomd door zuur door constante suikerafbraak. De oppervlakteplaque daarentegen bevatte een rijkere, gevarieerdere mix van soorten en verschilde meer tussen kinderen, wat de wisselende condities in de mond weerspiegelt.
Welke bacteriën richten daadwerkelijk de schade aan?
Door RNA en DNA te vergelijken konden de onderzoekers bacteriën onderscheiden die slechts aanwezig waren van degenen die bijzonder actief waren. Verschillende bekende cariës-geassocieerde groepen, waaronder Streptococcus en Prevotella, waren verrijkt in diep dentine, maar hun RNA-niveaus suggereerden daar slechts matige activiteit. Daarentegen toonden bacteriën uit de Lactobacillus-groep—en in het bijzonder Lactobacillus casei—zowel hogere abundantie als een opvallend hoge RNA‑op‑DNA‑verhouding in het dentine, wat wijst op sterke metabole activiteit. Een andere soort, Oribacterium sp. HMT-078, was ook consequent verrijkt en actiever in diepe laesies. Samen wijzen deze bevindingen op L. casei en dit type Oribacterium als sleutelspelers bij het creëren en in stand houden van extreem zure omstandigheden die dentine oplossen.
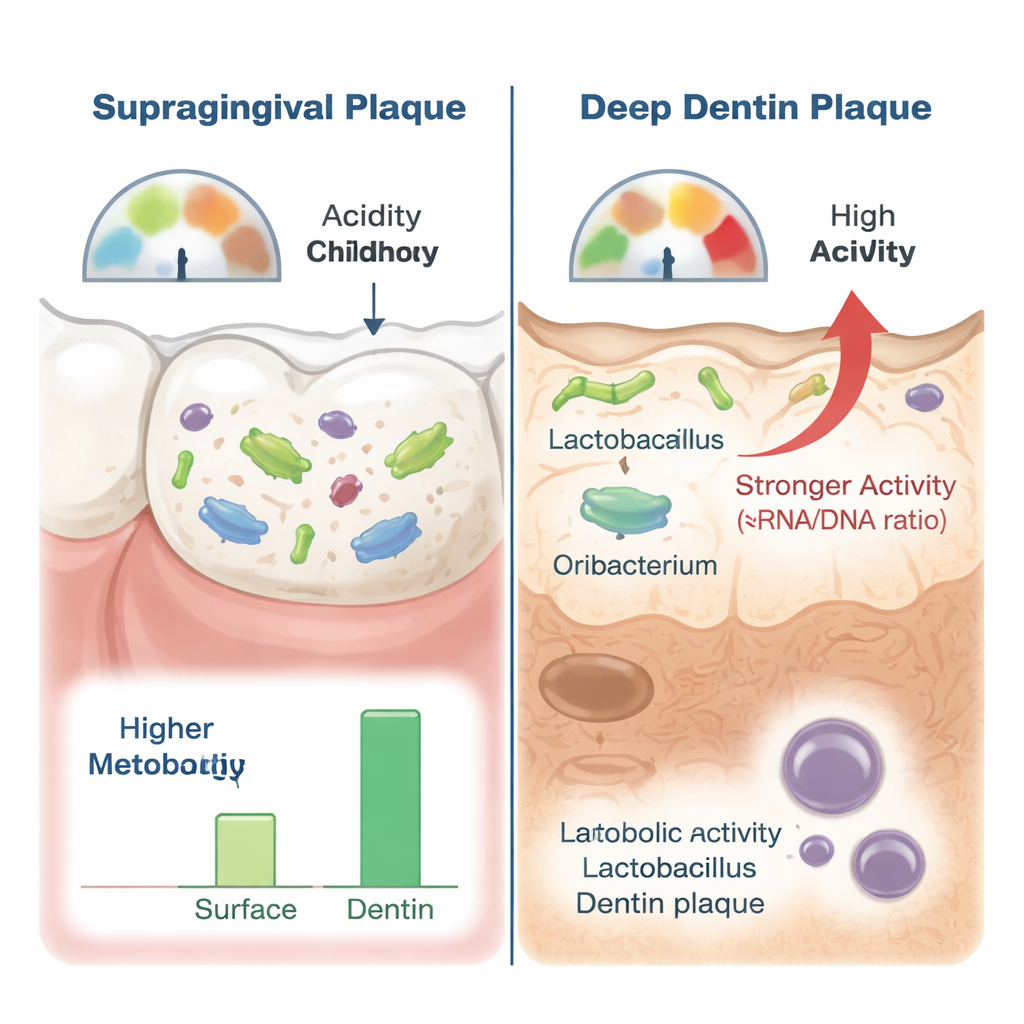
Wat dit betekent voor het beschermen van jonge tanden
Voor leken is de kernboodschap dat de ergste vormen van tandbederf bij peuters niet door willekeurige cariësbacteriën worden veroorzaakt, maar door een gespecialiseerde groep die diep in de tand onder zeer zure omstandigheden floreert. Lactobacillus casei en aanverwante soorten lijken bijzonder actieve daders te zijn, in samenwerking met andere zuurproducerende microben. Beter inzicht in welke bacteriën het meest actief zijn waar de tand afbreekt, kan toekomstige strategieën sturen—van gerichte preventie en voedingsadvies tot nieuwe behandelingen die deze diepe, zuurminnende gemeenschappen verstoren voordat ze de tanden van een kind vernietigen.
Bronvermelding: Naumann, A.A., Elmorr, E.M., Lamont, E.I. et al. DNA and RNA-based amplicon sequencing of paired supragingival and dentin lesion plaque in children with severe early childhood caries. Int J Oral Sci 18, 19 (2026). https://doi.org/10.1038/s41368-025-00421-4
Trefwoorden: vroegkinderlijke cariës, orale microbiota, dentineplaque, Lactobacillus casei, tandbederf bij kinderen