Clear Sky Science · nl
KDM6B/Pdk1-glycolysepad-gedreven ZEB2-lactylatie bevordert de vorming van cellulair cementum
Waarom het beschermen van wortels uitmaakt
Tandvleesaandoening, of parodontitis, is een van de belangrijkste oorzaken van tandverlies bij volwassenen. Naarmate de aandoening vordert, tast zij stilletjes de weefsels aan die tanden aan de kaak verankeren. Een van de belangrijkste daarvan is cementum, een dun, botachtig laagje dat het worteloppervlak bedekt en het mogelijk maakt dat de tand zich verankert aan het omringende ligament en bot. Zodra cementum verloren gaat, raken tanden losser en kunnen ze uiteindelijk uitvallen. Deze studie stelt een eenvoudige maar belangrijke vraag: kunnen we op moleculair niveau begrijpen hoe cementum wordt opgebouwd, zodat we het lichaam ooit kunnen helpen het te herbouwen en tanden levenslang op hun plaats te houden?
Van tandondersteunende cellen naar een therapeutisch doel
Cementum wordt aangemaakt door gespecialiseerde cellen die cementoblasten worden genoemd; zij zitten op het worteloppervlak en leggen nieuw mineraal af. Deze cellen gedragen zich veel als botvormende cellen, maar de signalen die bepalen wanneer en hoe ze cementum bouwen, waren tot nu toe slecht begrepen. De onderzoekers richtten zich op een molecuul genaamd KDM6B, een enzym dat chemische labels op DNA-verpakkingsproteïnen wijzigt en genen kan activeren. Door muizenpijlen van verschillende leeftijden en in het laboratorium gekweekte cementoblasten te bestuderen, vonden zij dat KDM6B-niveaus stijgen tijdens de actieve fase van cementumvorming en dalen wanneer de groei vertraagt. Wanneer ze KDM6B in cellen of in muizen blokkeerden, daalde de activiteit van cementoblasten en werd het ‘cellulaire’ deel van het cementum – het dikkere, levende deel nabij de wortelpunt – dunner, wat suggereert dat KDM6B een sleutelrol speelt bij gezonde cementumgroei.
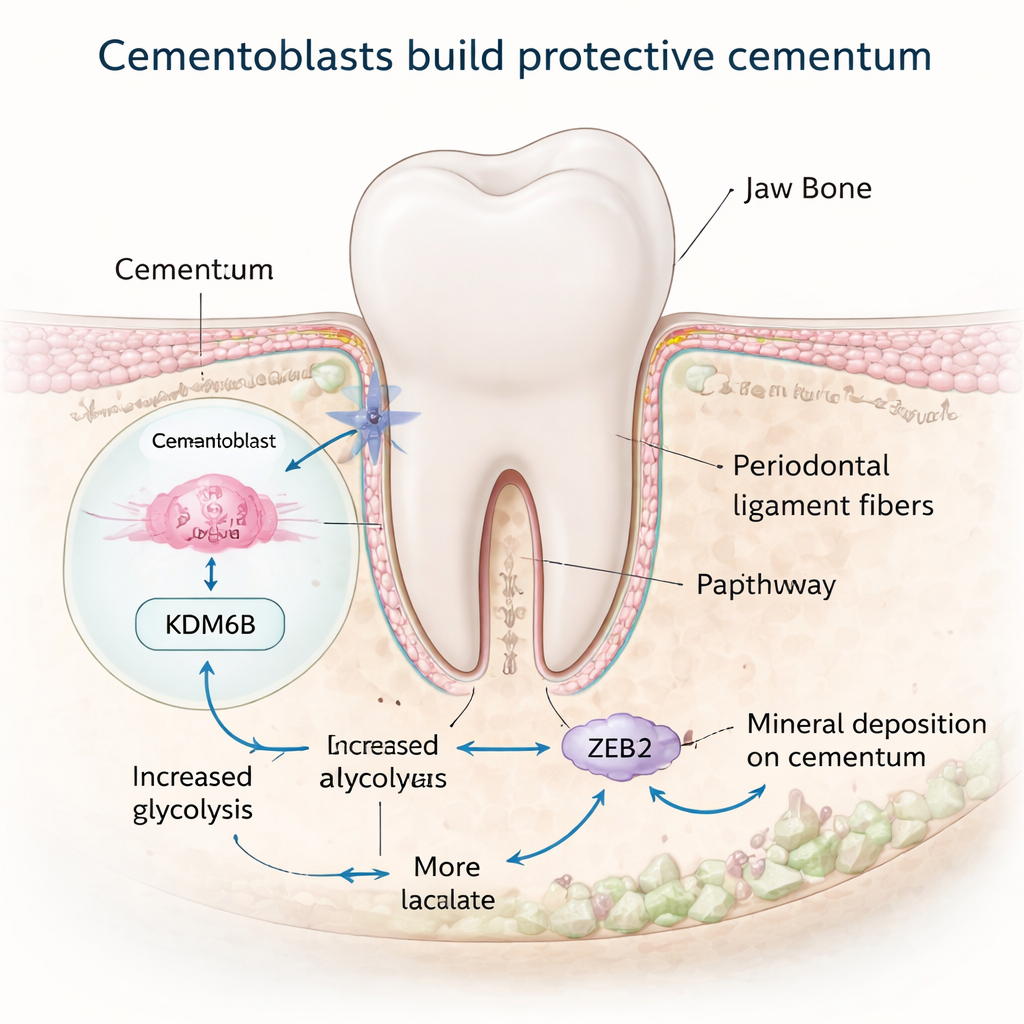
Metabole herprogrammering om mineraal te bouwen
Het opbouwen van gemineraliseerd weefsel kost veel energie, en veel cellen schakelen hun metabolisme naar een hogere versnelling tijdens dat proces. Het team ontdekte dat KDM6B cementoblasten helpt hun suikervoorziening anders te gebruiken. Normaal gesproken geven deze cellen de voorkeur aan een pad dat glycolyse heet, waarbij glucose snel wordt afgebroken en lactaat wordt geproduceerd. Wanneer KDM6B werd verminderd, werden genen die betrokken zijn bij glycolyse omlaaggebracht, terwijl genen die gekoppeld zijn aan langzamere, zuurstofafhankelijke energieproductie gemengd of verhoogd waren, en de cellen produceerden in totaal minder energie. Een centrale speler in deze verschuiving was het enzym PDK1. Met genomemapppingsinstrumenten toonden de onderzoekers aan dat KDM6B fysiek een remmend label verwijdert uit het DNA-gebied dat het Pdk1-gen reguleert, waardoor PDK1-niveaus kunnen stijgen. Het herstellen van PDK1 in KDM6B-deficiënte cellen bracht vele markers van mineralisatie terug, en onthulde zo een KDM6B–PDK1-metabool schakelmechanisme dat cementoblasten aandrijft.
Lactaat van afvalproduct naar nuttig signaal
Lactaat wordt vaak gezien als een afvalproduct van hardwerkende spieren, maar recent onderzoek laat zien dat het ook kan fungeren als signaal dat proteïnen modificeert. Hier zorgden hogere glycolyse, aangedreven door KDM6B en PDK1, voor een toename van lactaatproductie in cementoblasten. De onderzoekers volgden vervolgens een nieuwere vorm van eiwitmodificatie, lactylatie, waarbij lactaat-afgeleide labels aan specifieke eiwitplaatsen worden gehangen. Ze vonden dat lactylatieniveaus in cementoblasten stegen tijdens periodes van actieve cementumvorming en daalden in oudere muizen en in KDM6B-deficiënte cellen. Het toevoegen van eenvoudig natriumlactaat aan het systeem versterkte de lactylatie, heractiveerde mineralisatiegerelateerde genen en herstelde de vorming van mineraalknobbels zowel in gecultiveerde cellen als in een muismodel, zelfs wanneer KDM6B was geblokkeerd. Dit suggereert dat lactaat zelf kan helpen verzwakte cementumopbouw te herstellen.
Een moleculaire impuls voor een sleutelregulator van cementum
Het team vroeg zich vervolgens af welke eiwitten door lactaat werden "geadopteerd" op een manier die relevant was voor cementum. Ze richtten zich op ZEB2, een genregulerend eiwit dat al bekendstaat als bevorderlijk voor de mineralisatie door cementoblasten. Met eiwitmappingtechnieken identificeerden ze specifieke plaatsen op ZEB2 die lactylatie-merken dragen en toonden aan dat het wijzigen van één kritisch site het vermogen van de cel om mineralisatiegenen aan te zetten verzwakte. Verdere experimenten lieten zien dat de KDM6B–PDK1-route ZEB2-lactylatie versterkt en dat het bijvoegen van extra lactaat ZEB2’s activiteit kan herstellen wanneer PDK1 laag is. In wezen zijn metabolisme en genregulatie gekoppeld: suikerafbraak levert lactaat, dat vervolgens ZEB2 fijnafstemt om de programma’s voor cementumopbouw krachtig te houden.
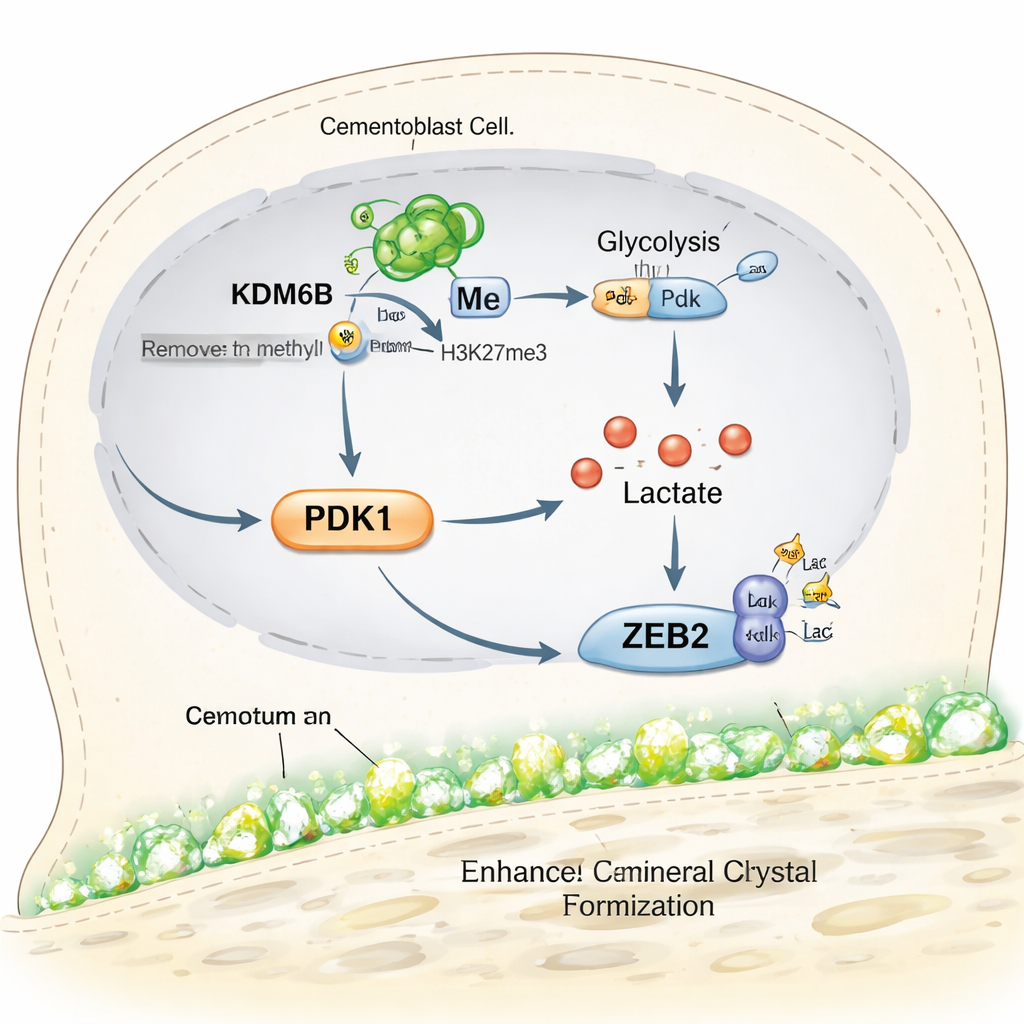
Wat dit betekent voor toekomstige tandbehoudende therapieën
Simpel gezegd onthult de studie een keten van gebeurtenissen binnen cementumvormende cellen: het enzym KDM6B maakt het Pdk1-gen toegankelijk, PDK1 stuurt cellen naar snelle suikerverwerking, dat metabolisme genereert lactaat, en lactaat stemt het ZEB2-eiwit chemisch bij om mineraalafzetting aan te sturen. Wanneer een stap in deze keten wordt geblokkeerd, stokt de cementumgroei, maar het zorgvuldig aanvullen van lactaat kan deze deels herstellen. Voor patiënten vertaalt dit werk zich nog niet direct naar een klinische behandeling, maar het wijst op nieuwe, precieze doelwitten voor geneesmiddelen of biomaterialen die zijn ontworpen om cementum te regenereren en tanden te stabiliseren bij gevorderde tandvleesziekte. Het suggereert ook dat vergelijkbare metabole "schakelaars" benut kunnen worden om botgenezing elders in het lichaam te stimuleren.
Bronvermelding: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Trefwoorden: cementumregeneratie, parodontitis, metabolisme van cementoblasten, histonendemethylase KDM6B, proteïnelactylatie