Clear Sky Science · nl
Reguleringsmechanismen voor de stabiliteit van het Snail-eiwit: ubiquitine–proteasoomsysteem en chaperonne-gemedieerde autofagie
Waarom de verspreiding van kanker afhangt van een kwetsbaar eiwit
Kanker wordt pas echt levensbedreigend wanneer cellen losraken van de oorspronkelijke tumor en naar verre organen migreren. Deze verspreiding, of metastase, hangt voor een deel af van een krachtig "master switch"-eiwit genaamd Snail, dat cellen helpt hun verbindingen te versoepelen en mobieler te worden. Dit artikel legt uit hoe onze cellen Snail doorgaans kort houden door het snel af te breken via twee hoofdafvalsysteem. Begrijpen hoe dit evenwicht werkt, biedt nieuwe aanknopingspunten om metastase te vertragen of te voorkomen.
Van strak verpakte cellen naar zwervende indringers
In gezonde weefsels vormen epitheelcellen ordelijke, baksteenachtige lagen die op hun plek blijven en stevig aan hun buren vastzitten. Om te ontsnappen ondergaat een tumorcel vaak een transformatie die epithelial–mesenchymal transition (EMT) wordt genoemd, waarbij ze haar nauwe contacten verliest en het vermogen krijgt te bewegen en te invaseren. Snail is een belangrijke aanjager van deze transformatie: wanneer het in de celkern aanwezig is, schakelt het genen uit die cel–cel-adhesie onderhouden en schakelt het genen aan die beweging en invasie bevorderen. Hoge niveaus van Snail worden in verband gebracht met agressieve vormen van kanker en slechte patiëntuitkomsten, dus cellen hebben mechanismen ontwikkeld om Snail schaars en kortlevend te houden onder normale omstandigheden.
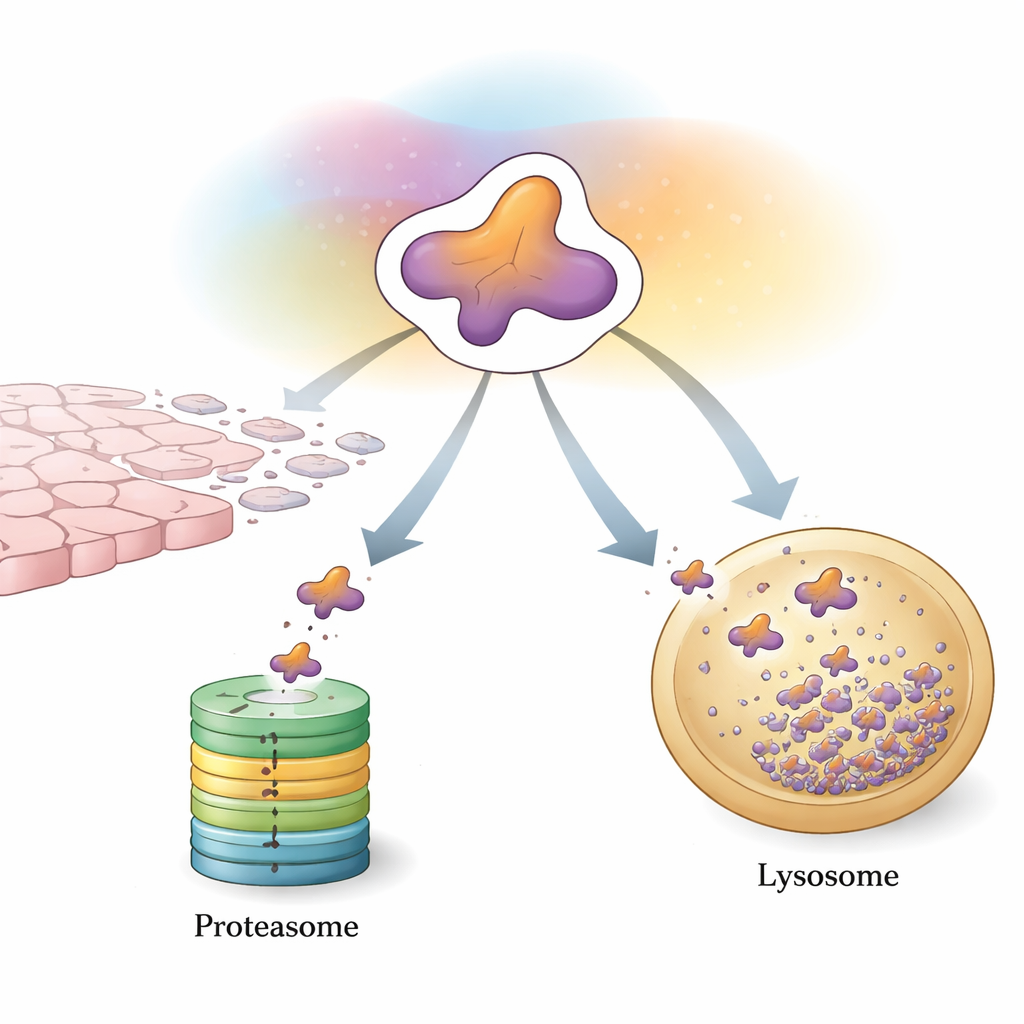
De eerste verdedigingslinie van de cel: markeren en versnipperen
Een belangrijke manier waarop cellen Snail beheersen, is via het ubiquitine–proteasoomsysteem, een markeer-en-versnippermachine voor ongewenste eiwitten. Gespecialiseerde enzymen hechten kleine "vlaggetjes" gemaakt van het eiwit ubiquitine aan Snail. Wanneer genoeg van deze vlaggen in een bepaald patroon zijn aangebracht, wordt Snail naar het proteasoom gestuurd, een tonvormig complex dat het in stukjes hakt. Een groot aantal hulp-eiwitten verfijnt dit proces. Sommige enzymen plaatsen ketens die afbraak bevorderen en Snail snel naar de versnipperaar sturen, wat helpt tumorgroei en -spreiding te beperken. Andere voegen juist ketens toe die Snail stabiliseren of indirect de genproductie verhogen, waardoor de balans doorslaat naar EMT en metastase. Chemische aanpassingen zoals fosforylering en acetylatie fungeren als extra schakelaars die bepalen welke helpers aan Snail kunnen binden en of het wordt vernietigd of gespaard.
De remmen losmaken: enzymen die Snail redden
Het verhaal eindigt niet bij het markeren van Snail voor afbraak. Een andere groep enzymen, de deubiquitinases, kan de ubiquitinevlaggen verwijderen en Snail zo redden van het proteasoom. Veel van deze enzymen zijn in kankers geactiveerd of versterkt, waardoor Snail ontkomt aan afbraak en in de kern blijft bestaan. Hun werking hangt sterk af van de cellulaire context: in sommige omstandigheden stabiliseren ze Snail direct, terwijl ze in andere beïnvloeden waar Snail zich in de cel bevindt of hoe het met partner-eiwitten interageert. Signalen uit kankergeassocieerde routes, zoals groeifactoren en stressreacties, voeden dit netwerk en bepalen of Snail snel wordt verwijderd of toegestaan wordt het EMT-programma te sturen.
Een tweede vangnet: selectieve aanlevering naar het recyclecentrum van de cel
Buiten het proteasoom vertrouwen cellen op autofagie, een verzameling routes die eiwitten naar zure compartimenten genaamd lysosomen transporteren voor afbraak. Deze review belicht een zeer selectieve vorm die bekendstaat als chaperonne-gemedieerde autofagie (CMA) als een tweede belangrijke route voor het beheersen van Snail. CMA herkent een korte sequentie binnen Snail en levert, met behulp van escort-eiwitten, cytoplasmatisch Snail aan lysosomen voor vernietiging. In minder agressieve borstkankercellen houdt dit systeem Snail grotendeels buiten de kern en vatbaar voor lysosomale verwijdering. In agressievere, triple-negatieve borstkankers hoopt Snail zich eerder in de kern op en omzeilt het CMA, waardoor zijn vermogen om EMT en metastase te activeren wordt versterkt.
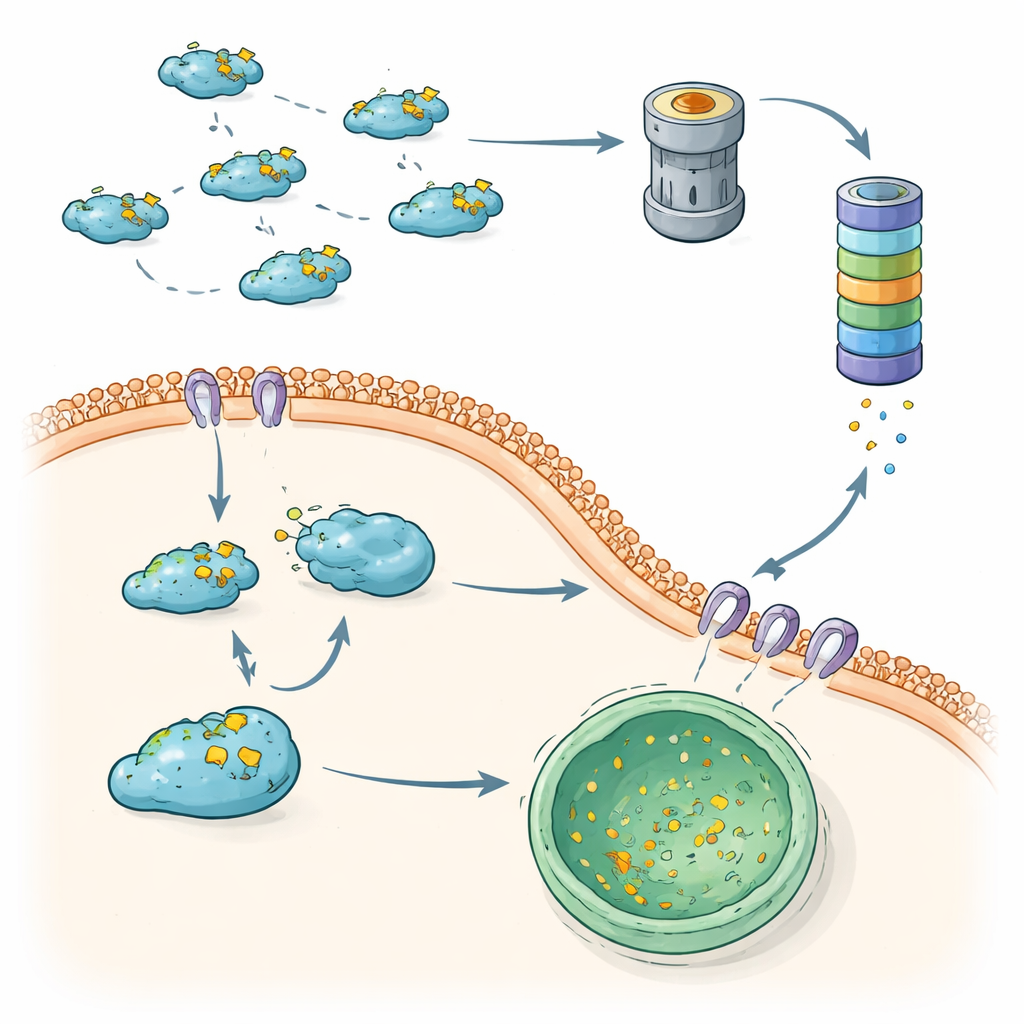
Wanneer kwaliteitscontrole faalt, wint metastase terrein
Samengenomen tonen deze bevindingen aan dat cellen twee complementaire "kwaliteitscontrole"-assen gebruiken om Snail te beperken: de ubiquitine–proteasoomroute en CMA-gebaseerde lysosomale afbraak. Wanneer beide goed functioneren, wordt Snail snel omgezet, wat EMT beperkt en helpt te voorkomen dat tumorcellen zich verspreiden. Wanneer een van beide assen verzwakt raakt — door veranderingen in markeerenzymen, deubiquitinases of CMA-componenten — wordt Snail stabieler, hoopt het zich op in de kern en bevordert het invasief gedrag sterk. Door deze onderling verbonden afbraakroutes in kaart te brengen, schetst het artikel nieuwe therapeutische mogelijkheden: geneesmiddelen die Snail-afbraak herstellen of versterken, of die Snail weer richting CMA- of proteasomale vernietiging sturen, zouden kunnen helpen het remsysteem op metastase weer in te schakelen zonder deze essentiële eiwitrecyclingsystemen volledig uit te schakelen.
Bronvermelding: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Trefwoorden: kankeruitzaaiing, epitheel–mesenchymale transitie, Snail-eiwit, eiwitafbraak, autofagie