Clear Sky Science · nl
Een transient receptor potential vanilloid 1-afhankelijk cornea–trigeminus neuro-inflammatoir circuit bevordert corneale neuropathie
Gevoelige ogen en aanhoudende pijn
Veel mensen met droge, geïrriteerde ogen zijn verbaasd dat hun ergste klachten niet voortkomen van het oppervlak van het oog zelf, maar van de zenuwen die irritatie en pijn waarnemen. Deze muizenstudie onthult een verborgen terugkoppellus tussen het oog en het sensorische centrum in de hersenen die helpt verklaren waarom oogpijn persistent kan worden en waarom het soms beide ogen treft, ook wanneer slechts één droog lijkt. Door een specifieke moleculaire poortwachter in deze lus aan te wijzen, wijst het werk op nieuwe manieren om pijnlijke ogen te kalmeren zonder alleen maar meer tranen toe te voegen.

Wanneer het alarmsysteem van het oog misfires
Het heldere voorraam van het oog, de cornea, is dichtbezette met zenuwuiteinden die constant vochtigheid, temperatuur en de chemische samenstelling van tranen controleren. Bij droge-oogaandoeningen nemen tranen af of worden ze te zout, en patiënten ontwikkelen vaak branderigheid, stekende pijn of zelfs invaliderende pijn. De auteurs concentreerden zich op een moleculair sensor op corneale pijnvezels genaamd TRPV1, vooral bekend als de receptor voor het chilipeper‑bestanddeel capsaïcine. Deze sensor is gevoelig voor warmte en voor signalen die vrijkomen bij weefselstress. Het team vroeg zich af of overactivatie van TRPV1 door droogte en schade niet alleen lokale irritatie maar ook diepere veranderingen in de zenuwen die het oog met de hersenen verbinden, zou kunnen aansturen.
Een zenuw–immuun circuit dat oog en hersenen verbindt
Met muismodellen waarin de traanproductie chirurgisch werd verminderd, toonden de onderzoekers aan dat droogte TRPV1-dragende zenuwvezels in de cornea sterk activeert. Dit veranderde op zijn beurt genactiviteit en immuunresponsen in het trigeminale ganglion, een zenuwknoop die de cellichamen van corneale sensorische neuronen herbergt. In normale muizen veroorzaakte droogte daar een golf van ontstekings- en immuungerelateerde genen en veranderde het de toestand van nabijgelegen macrophagen, immuuncellen die sensorische neuronen omringen. Tegelijkertijd vertoonden de droge ogen zelf geactiveerde immuuncellen aan het oppervlak, verminderde zenuwdichtheid en abnormale gevoeligheid: de cornea werd minder responsief voor mechanische aanraking en voor sommige chemische prikkels, maar juist reactiever voor TRPV1-stimulatie, wat suggereert dat deze specifieke sensor gesensitiseerd was geraakt.
Hoe één pijnlijk oog het andere kan beïnvloeden
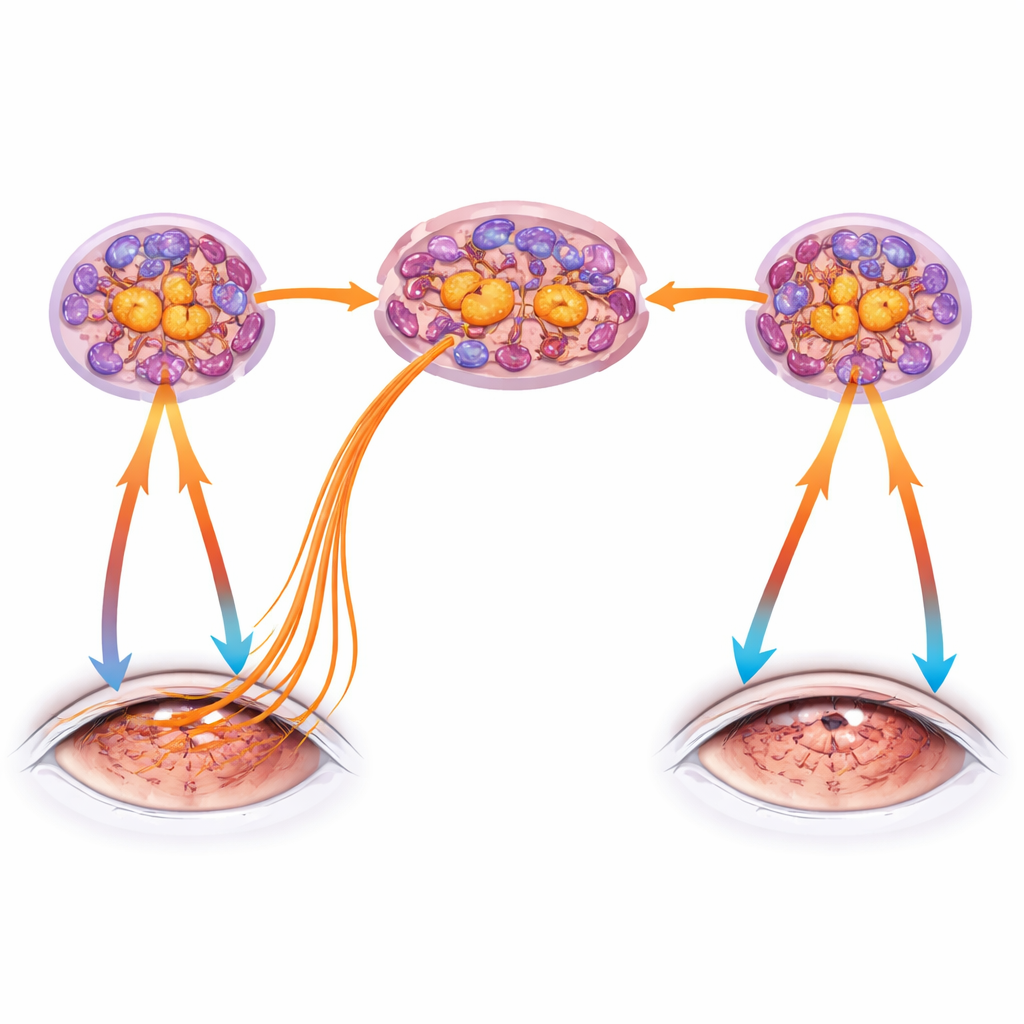
Om directe effecten van droogte te onderscheiden van verder weg ontstane zenuwsignalen, creëerde het team een “eenszijdig” droog oog door alleen de traanklier aan de rechterkant te verwijderen. Opvallend bleef het onbehandelde linkeroog normaal vochtig en behield het een gezonde oppervlaktebarrière, maar na verloop van tijd ontwikkelde het subtiele ontsteking en duidelijke tekenen van zenuwdisfunctie — verdunning van diepere zenuwvezels en veranderde gevoeligheid — die het beschadigde oog spiegelden maar erachteraan liepen. Deze contralaterale veranderingen waren afhankelijk van TRPV1: muizen die genetisch deze sensor misten, waren beschermd in zowel het droge als het onaangetaste oog. RNA-sequencing van trigeminale ganglia bevestigde dat unilaterale droogte ook aan de tegenovergestelde zijde een immuun- en ontstekingshandtekening opwekte, wat wijst op een cornea–trigeminus–cornea-circuit dat problemen van het ene oog naar het andere kan verspreiden.
Aantonen dat TRPV1 voldoende is om schade te veroorzaken
Droogte is complex en activeert vele paden, dus vroegen de auteurs vervolgens of TRPV1 op zichzelf dit circuit in gang kon zetten. Ze brachten capsaïcine topisch aan op de cornea van één oog, waarbij TRPV1 werd gestimuleerd zonder het oppervlak uit te drogen. Het behandelde oog vertoonde duidelijke degeneratie van corneale zenuwen en verminderde gevoeligheid, ook al bleef de epitheliale barrière intact. Opmerkelijk ontwikkelde het onbehandelde oog opnieuw mildere maar meetbare verliezen van zenuwuiteinden en veranderingen in gevoeligheid, wat bevestigt dat sterke activatie van TRPV1 in één cornea voldoende is om zenuwschade en functionele veranderingen in het tegenliggende oog te veroorzaken via het gedeelde trigeminusnetwerk. Muizen zonder T- en B-lymfocyten ontwikkelden alleen veranderingen in het behandelde oog, wat suggereert dat volledige bilaterale verspreiding zowel een adaptieve immuunrespons als zenuwactivatie vereist.
Een pijnbevorderende boodschapper en een mogelijke behandelrichting
De studie onderzocht ook substantie P, een neuropeptide dat vrijkomt uit gestimuleerde pijnvezels en weefsels verder kan ontsteken en TRPV1-activiteit kan versterken. Het blokkeren van substantie-P-receptoren met oogdruppels in het niet-droge oog van muizen met eenszijdige droge ogen schaadde het corneale oppervlak niet maar verminderde significant het verlies van tastgevoeligheid en de verhoogde respons op TRPV1-stimulatie. Het voorkwam echter niet volledig het structurele verlies van zenuwuiteinden, wat onderstreept dat meerdere factoren samenwerken om corneale zenuwen te beschadigen. Gezamenlijk schetsen de bevindingen een vicieuze cirkel: droogte en letsel activeren TRPV1 in corneale zenuwen, die gevaarsignalen naar het trigeminale ganglion sturen, immuuncellen daar rekruteren en herprogrammeren, en vervolgens pro-inflammatoire zenuwsignalen en neuropeptidevrijgave terug naar het oogoppervlak sturen, waardoor zenuwdegeneratie verergert en disfunctie tussen ogen zich verspreidt.
Wat dit betekent voor mensen met droge, pijnlijke ogen
Voor niet‑specialisten is de kernboodschap dat droge-oogaandoening niet slechts een lokaal probleem van ontbrekende tranen is. Het omvat een zichzelf versterkende zenuw–immuunlus die het oogoppervlak verbindt met sensorische centra in het hoofd en terug. TRPV1 bevindt zich aan het toegangspunt van deze lus en fungeert als een overgevoelig alarm dat, eenmaal geactiveerd, helpt ontsteking en zenuwschade in stand te houden, zelfs als de oorspronkelijke droogte bescheiden of eenzijdig is. Therapieën die de TRPV1-activiteit op corneale zenuwen terugschakelen, of die downstream boodschappers zoals substantie P onderbreken, zouden daarom meer kunnen doen dan een droog oppervlak verzachten — ze kunnen een dieper pijncircuit doorbreken en het verfijnde zenuwnetwerk beschermen dat onze ogen comfortabel en responsief houdt.
Bronvermelding: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Trefwoorden: droge ogen, corneale zenuwen, TRPV1, neuro-inflammatie, substantie P