Clear Sky Science · nl
Metabole wisselwerking tussen kankergeassocieerde fibroblasten, adipocyten en immuuncellen als drijver van een immunosuppressieve tumor-microomgeving
Waarom de buurt van de tumor ertoe doet
Kanker groeit niet geïsoleerd. Het leeft in een drukke omgeving van steuncellen, vetcellen en immuuncellen die voortdurend voedingsstoffen en chemische signalen uitwisselen. Dit artikel legt uit hoe de „metabolisme” van die omgeving — de manier waarop cellen brandstof gebruiken en delen — stilletjes het gevecht in het voordeel van de tumor en tegen het immuunsysteem kantelt. Inzicht in deze verborgen economie van suikers, vetten en aminozuren opent nieuwe wegen om immunotherapieën effectiever te maken en om het ondersteuningssysteem van de tumor af te snijden.
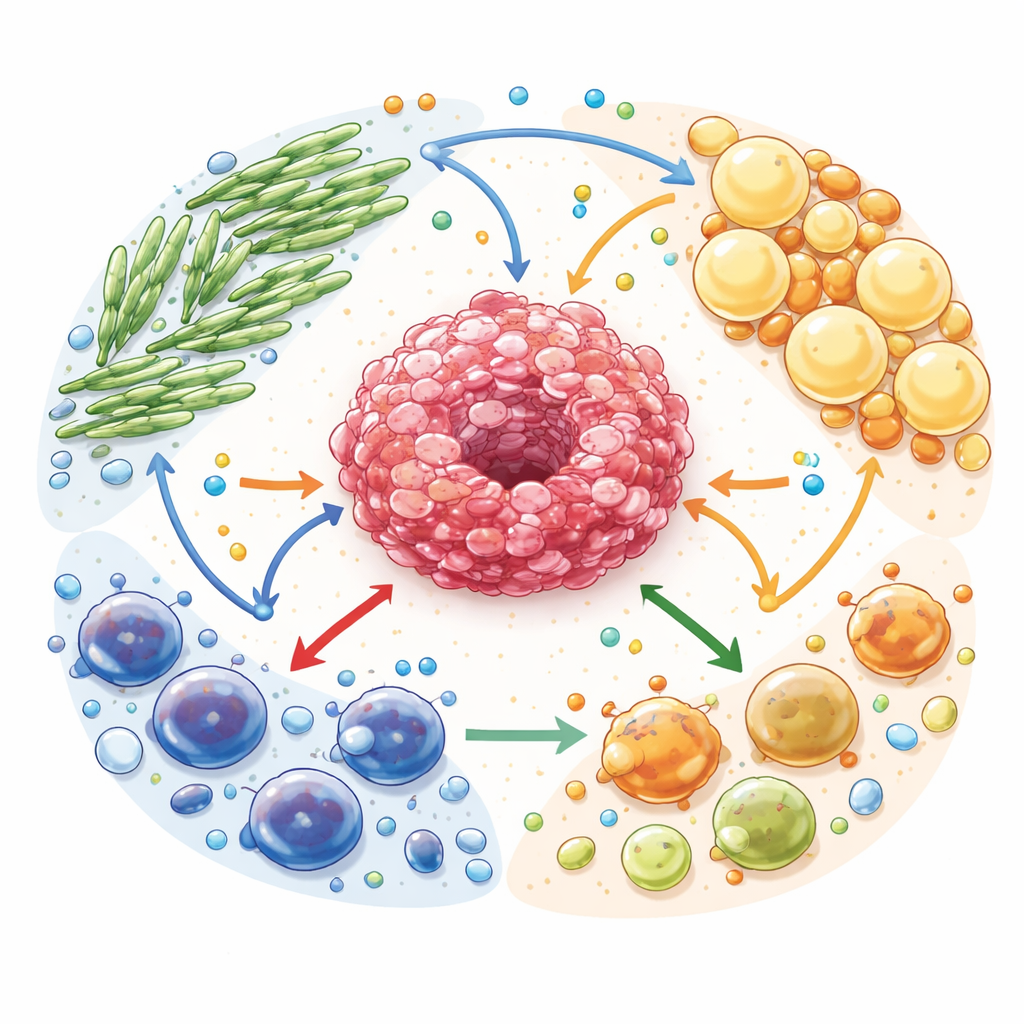
Brandstofdeling in een kankerecosysteem
De auteurs beschrijven de tumor-microomgeving als een complex ecosysteem. Kankercellen worden omringd door kankergeassocieerde fibroblasten (littekenachtige ondersteunende cellen), kankergeassocieerde adipocyten (herschakelde vetcellen) en vele typen immuuncellen. Al deze cellen concurreren om en wisselen brandstoffen uit zoals glucose, vetzuren en aminozuren. Maar deze handel is niet neutraal: ondersteunende cellen worden omgebouwd om hun eigen voorraden af te breken en energierijke moleculen uit te exporteren die kankercellen voeden. Tegelijkertijd hopen zich afvalachtige bijproducten op, waaronder lactaat en adenosine, die als krachtige signalen werken die beschermende immuuncellen verzwakken en cellen bevoordelen die de immuunaanval dempen.
Hoe vetcellen tumoren helpen en de verdediging belemmeren
De nabijgelegen vetkussens doen veel meer dan alleen calorieën opslaan. Onder invloed van tumorsignalen en lage zuurstof transformeren gewone vetcellen in kankergeassocieerde adipocyten. Ze krimpen hun vetdruppels, verhogen vetafbraak en stromen uit vrije vetzuren, ontstekingsmoleculen en kleine vesikels geladen met cargo. Kankercellen importeren deze vetten gulzig en verbranden ze in hun mitochondriën, waardoor ze een flexibele, langdurige energiebron krijgen die hen helpt stress te overleven, uit te zaaien en resistentie tegen behandeling te ontwikkelen. Immuuncellen in vetrijke gebieden hebben het minder goed: cytotoxische T‑cellen en natural killer‑cellen overladen zich met vetten, krijgen last van oxiderende stress en glijden in een “uitgeputte” toestand met verminderde capaciteit om tumorcellen te vernietigen. Ter vergelijking, regulerende T‑cellen en bepaalde myeloïde cellen groeien bij deze lipiden en worden onderdrukkender, wat de immuunresponsen verder dempt.
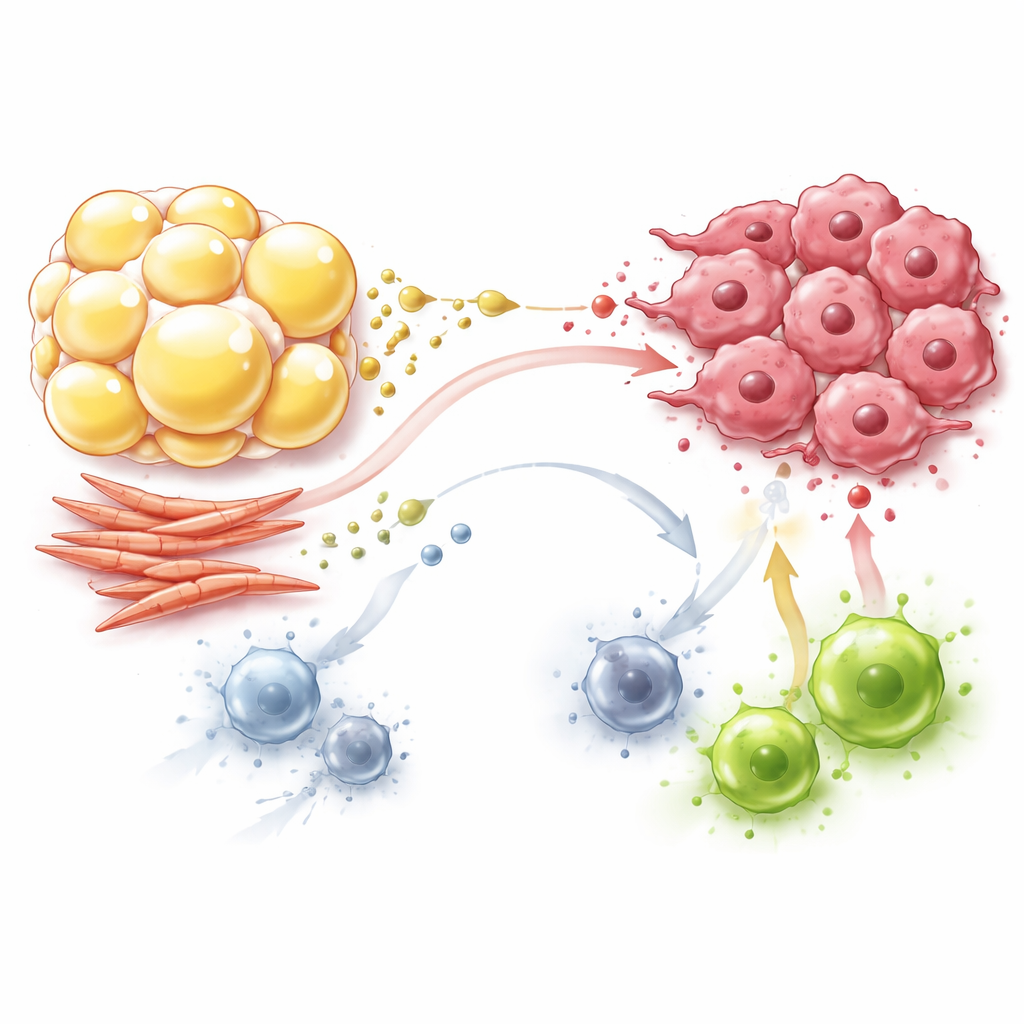
Fibroblasten: bouwers die ook het metabolisme herschakelen
Fibroblasten, lang bekend als de bouwers van littekenachtig weefsel rond tumoren, zijn ook actieve spelers in dit metabole drama. Kankergeassocieerde fibroblasten schakelen over op suikerhongerig gedrag en zetten grote hoeveelheden glucose om in lactaat en pyruvaat, zelfs wanneer er zuurstof beschikbaar is. Ze exporteren deze producten naar de omgeving, waar kankercellen ze hergebruiken als brandstof voor hun eigen energiecentrales, waardoor glucose vrijblijft voor groei. Fibroblasten maken en verhandelen ook aminozuren zoals glutamine, proline en asparagine, die zowel de structuur van de tumor als de groei onder nutriëntstress ondersteunen. Tegelijk consumeren fibroblasten sleutelvoedingsstoffen en laten lactaat vrij, waardoor effector T‑cellen die van glucose afhankelijk zijn worden verdrongen en macrofagen en T‑cellen naar tolerantere, minder agressieve toestanden worden geduwd.
Immuuncellen gevangen in een metabole val
Het immuunsysteem in tumoren wordt evenzeer gevormd door brandstofbeschikbaarheid als door antigenen. Cytotoxische T‑cellen en natural killer‑cellen, die snelle suikerverbranding nodig hebben om hun aanval te voeden, bevinden zich in een landschap dat is ontdaan van glucose en overspoeld met lactaat, vetten en andere onderdrukkende metabolieten. Hun motoren stokken, hun mitochondriën raken beschadigd en remmende „brakes” op hun oppervlak nemen toe. Ondertussen zijn regulerende T‑cellen en tumorgeassocieerde macrofagen goed aangepast aan deze harde omgeving. Zij geven de voorkeur aan vetverbranding en oxidatieve metabolisme, waardoor ze gedijen waar anderen falen. Ondersteund door fibroblasten en adipocyten versterken deze cellen een tolerante, wondgenezingsachtige staat die de tumor beschermt en de effectiviteit van checkpointremmers en andere immunotherapieën vermindert.
Het metabolisme als therapeutisch doelwit inzetten
De review belicht een groeiende gereedschapskist aan experimentele geneesmiddelen die bedoeld zijn om dit ondersteuningsnetwerk te verstoren zonder simpelweg delende cellen te vergiftigen. Sommige benaderingen zijn gericht op het blokkeren van vetvrijgave uit adipocyten of van vetopname en -verbranding in kankercellen. Andere richten zich op fibroblastgedreven routes die lactaat produceren, de matrix herevormen of suppressieve myeloïde cellen aantrekken. Door lactaatniveaus te verlagen, specifieke brandstoftransporters te blokkeren of lipidesensorische schakelaars binnen cellen te herprogrammeren, proberen deze strategieën de toegang tot glucose en de mitochondriale gezondheid van uitgeputte T‑ en natural killer‑cellen te herstellen. Het uiteindelijke doel is niet alleen de tumor uit te hongeren, maar ook de buurt te „heropvoeden” zodat immuuncellen de kankercellen weer kunnen zien, bereiken en effectief aanvallen.
Bronvermelding: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Trefwoorden: tumor microomgeving, kanker metabolisme, kankergeassocieerde fibroblasten, kankergeassocieerde adipocyten, tumor immunosuppressie