Clear Sky Science · nl
Tekort aan exocyst-complexcomponent Exoc5 verergert de vooruitgang van nierschade (fibrose)
Waarom littekenvorming in de nier belangrijk is
Chronische nierziekte treft honderden miljoenen mensen wereldwijd, en een belangrijke reden waarom ze voortschrijdt is fibrose—littekenweefsel dat langzaam het functionerende nierweefsel vervangt. Deze studie onderzoekt een minder bekend cellulair apparaat, het exocyst, en een van zijn onderdelen genaamd Exoc5, met een praktische vraag: helpt dit eiwit dat nieren schoon herstellen na een beschadiging, of drijft het ze richting littekenvorming en falen?
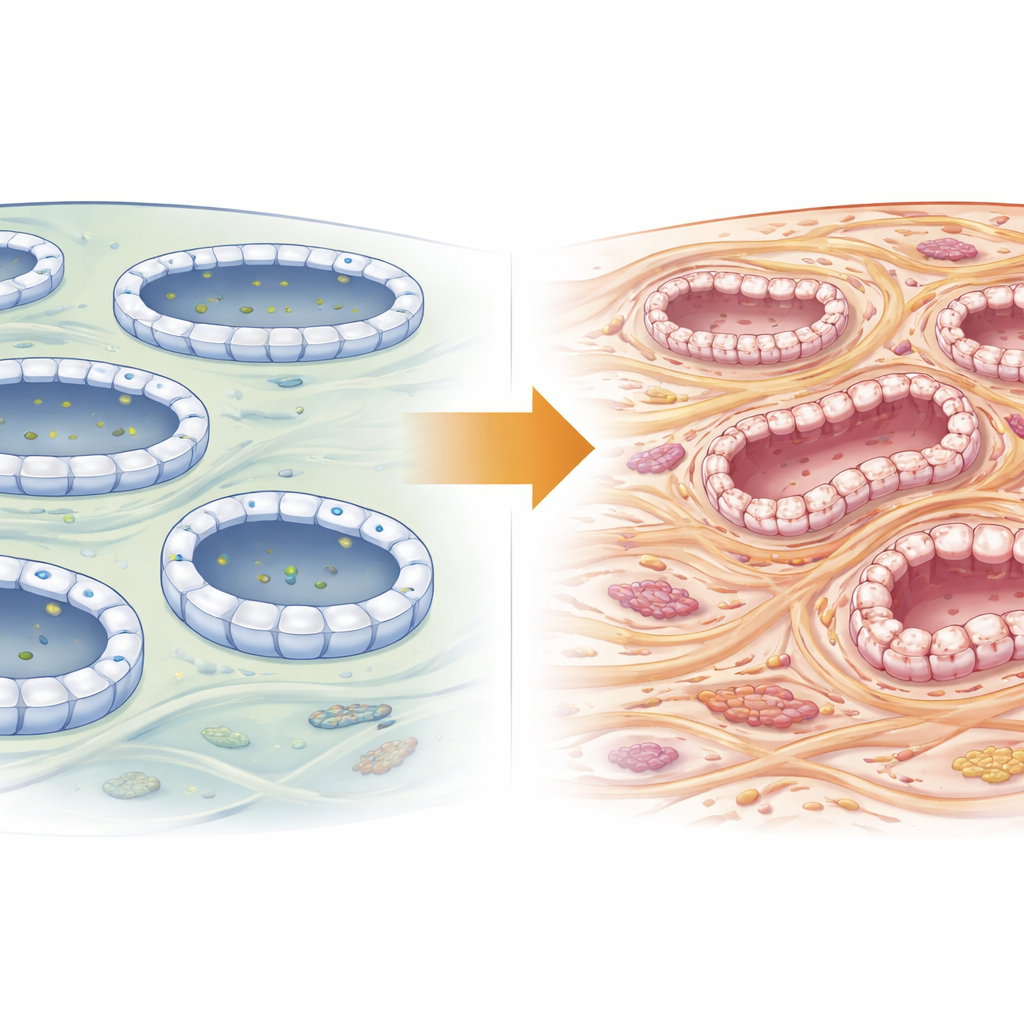
Een cellulaire logistieke hub in niertubuluscellen
Elke niertubuluscel is een druk logistiek centrum, voortdurend bezig met het verplaatsen van kleine, met cargo gevulde blaasje naar precieze plekken op het celoppervlak. Dit verkeer wordt georganiseerd door het exocyst, een acht-delige dockingcomplex. Exoc5 zit in het hart van dit apparaat en vormt de brug tussen cargo die van binnen de cel komt en de dockingsite in het buitenmembraan. Eerder werk toonde aan dat het verstoren van Exoc5 verschillende organen schaadt en dat het bijdraagt aan het behoud van de strakke, ordelijke structuur van niertubuluscellen. Omdat een verstoorde structuur een kenmerk is van fibrose, vermoedden de auteurs dat Exoc5 mogelijk stilletjes bepaalt of beschadigde nieren herstellen of littekenvorming ontwikkelen.
Het testen van de rol van Exoc5 in muizennieren
De onderzoekers maakten muizen waarbij Exoc5 alleen in proximale tubuluscellen was verwijderd—de segmenten die het meeste filtreren en reabsorberen. Tot hun verrassing groeiden deze muizen normaal en hadden ze bij normale omstandigheden een normale nierstructuur, transportereigenschappen en functie. Om een sterke, lokale beschadiging na te bootsen die vaak tot littekenvorming leidt, bond het team vervolgens één ureter dicht, een standaardprocedure die binnen een week drukopbouw, ontsteking en fibrose in de aangedane nier veroorzaakt. In zowel normale als Exoc5-deficiënte muizen verminderde deze obstructie de Exoc5-niveaus, maar de knockout-dieren ontwikkelden veel ernstiger tubulaire krimp, collageenophoping en binnendringen van ontstekingsgerelateerde cellen.
Van geordende buisjes naar migrerende cellen
Gezonde tubuluscellen zitten strak aan elkaar vast, met duidelijk gedefinieerde boven- en onderkanten. Tijdens fibrose ondergaan ze vaak een "epitheel-naar-mesenchym transitie" (EMT), een verschuiving van een verankerde, plaatachtige toestand naar een meer mobiele, vezelachtige toestand. De auteurs vonden dat na obstructie nieren zonder Exoc5 sterkere activatie van belangrijke EMT-stuurgenen vertoonden en hogere niveaus van eiwitten die typisch zijn voor migrerende, vezelproducerende cellen, samen met groter verlies van junctie-eiwitten die normaal de polariteit van tubuluscellen behouden. Ze zagen ook de terugkeer van Pax2, een ontwikkelingsregulator die normaal wordt uitgeschakeld zodra niertubuli volwassen zijn. Pax2 keerde sterker terug in Exoc5-deficiënte tubuli, met name in gestreste cellen die niet succesvol deelden, wat suggereert dat verlies van Exoc5 cellen naar een half-herstelde, gededifferentieerde staat duwt die vatbaar is voor littekenvorming.
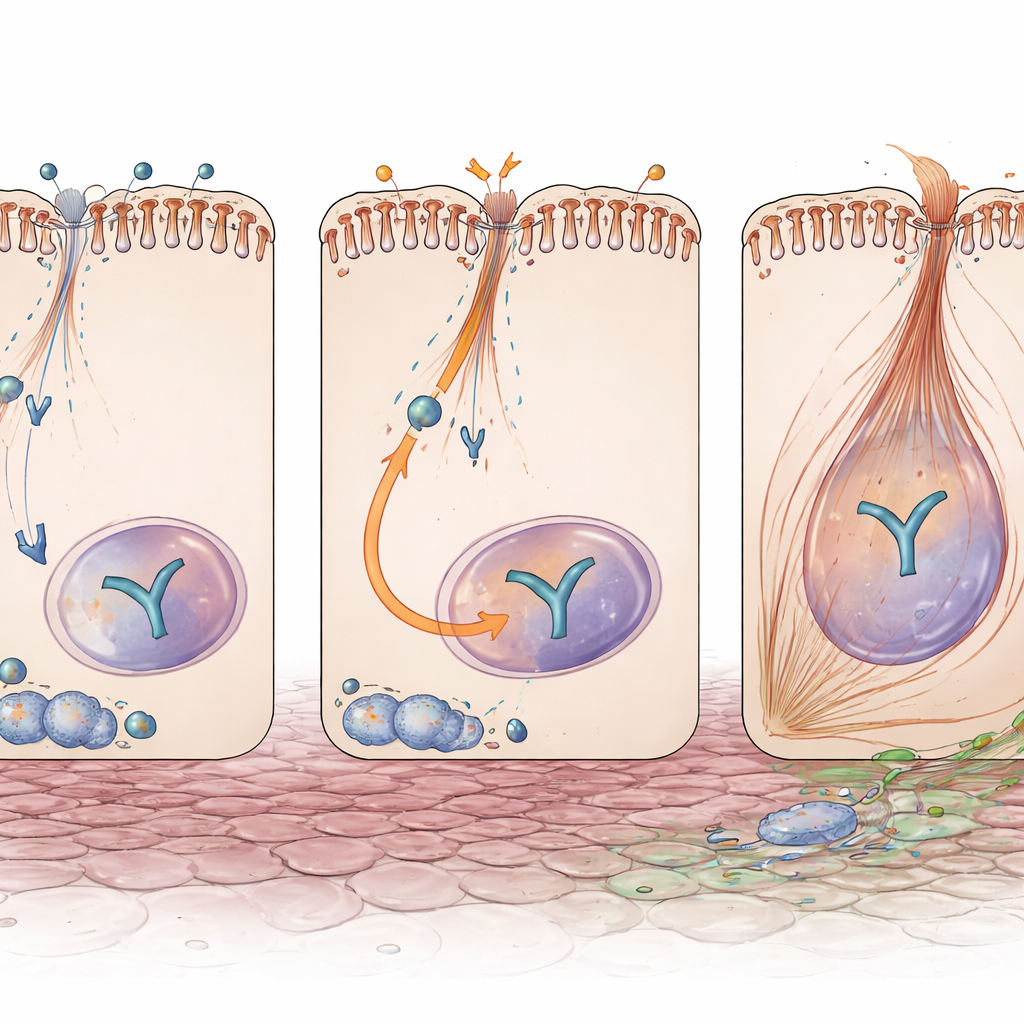
Een schakel die schade aan littekeningssignalen koppelt
Een andere centrale speler in fibrose is YAP, een signaalgevoelig eiwit dat naar de kern verhuist om genen voor groei en matrixproductie aan te zetten. Zelfs zonder verwonding hadden tubuli zonder Exoc5 hogere YAP-eiwitniveaus. Na obstructie was YAP sterker geactiveerd en geconcentreerd in celkernen in deze nieren, en waren de volgende producten—moleculen die bekend zijn als drijvers van fibrotische remodelering—verhoogd. Belangrijk is dat dit niet afkomstig was van extra YAP-genactiviteit, wat impliceert dat Exoc5 normaal YAP op eiwit- of traffickingniveau onderdrukt. In gekweekte menselijke niertubuluscellen leidde het verminderen van EXOC5 via RNA-interferentie tot een toename van YAP en Pax2, en zorgde het ervoor dat cellen sterker reageerden op het fibrotische signaal TGF-β, met grotere EMT-achtige veranderingen en meer cellen die contractiele vezels kregen die typisch zijn voor myofibroblasten.
Wat dit betekent voor toekomstige behandelingen
Samen genomen schetsen de bevindingen Exoc5 als een stille beschermer: onder stress helpt het tubuluscellen hun georganiseerde identiteit te behouden en houdt het pro-litteken signalen zoals YAP en Pax2 in toom. Wanneer Exoc5-niveaus dalen—hetzij door genetisch verlies, hetzij door beschadiging—verliezen tubuluscellen gemakkelijker hun polariteit, glijden ze in een ontwikkelingsachtige toestand en voeden ze het fibrotische proces. Omdat het verwijderen van Exoc5 in proximale tubuli gezonde nieren niet schaadde maar duidelijk de littekenvorming na beschadiging verergerde, wijzen de resultaten op Exoc5 en zijn signaalpartners als veelbelovende doelwitten voor therapieën die gericht zijn op het vertragen of omkeren van nierfibrose voordat die uitmondt in nierfalen.
Bronvermelding: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Trefwoorden: nierfibrose, Exoc5, epitheel-naar-mesenchym transitie, YAP-signaaltransductie, chronische nierziekte