Clear Sky Science · nl
Microglia-geassocieerde progressie van multiple sclerose: doelwitidentificatie en therapeutische interventie in menselijke in vitro-modellen
Waarom immuuncellen in de hersenen ertoe doen bij multiple sclerose
Multiple sclerose (MS) wordt vaak omschreven als een aandoening waarbij het immuunsysteem het brein en ruggenmerg aanvalt. Veel huidige geneesmiddelen verminderen acute aanvallen, of relapses, succesvol, maar ze stoppen de trage, stille achteruitgang die veel patiënten over jaren ervaren niet. Deze review legt uit hoe kleine immuuncellen die permanent in de hersenen wonen, microglia genoemd, die langetermijnachteruitgang kunnen aansturen — en hoe nieuwe in het laboratorium gekweekte menselijke hersenmodellen wetenschappers helpen behandelingen te vinden die progressie eindelijk kunnen vertragen of stoppen.
De verborgen motor van aanhoudende schade
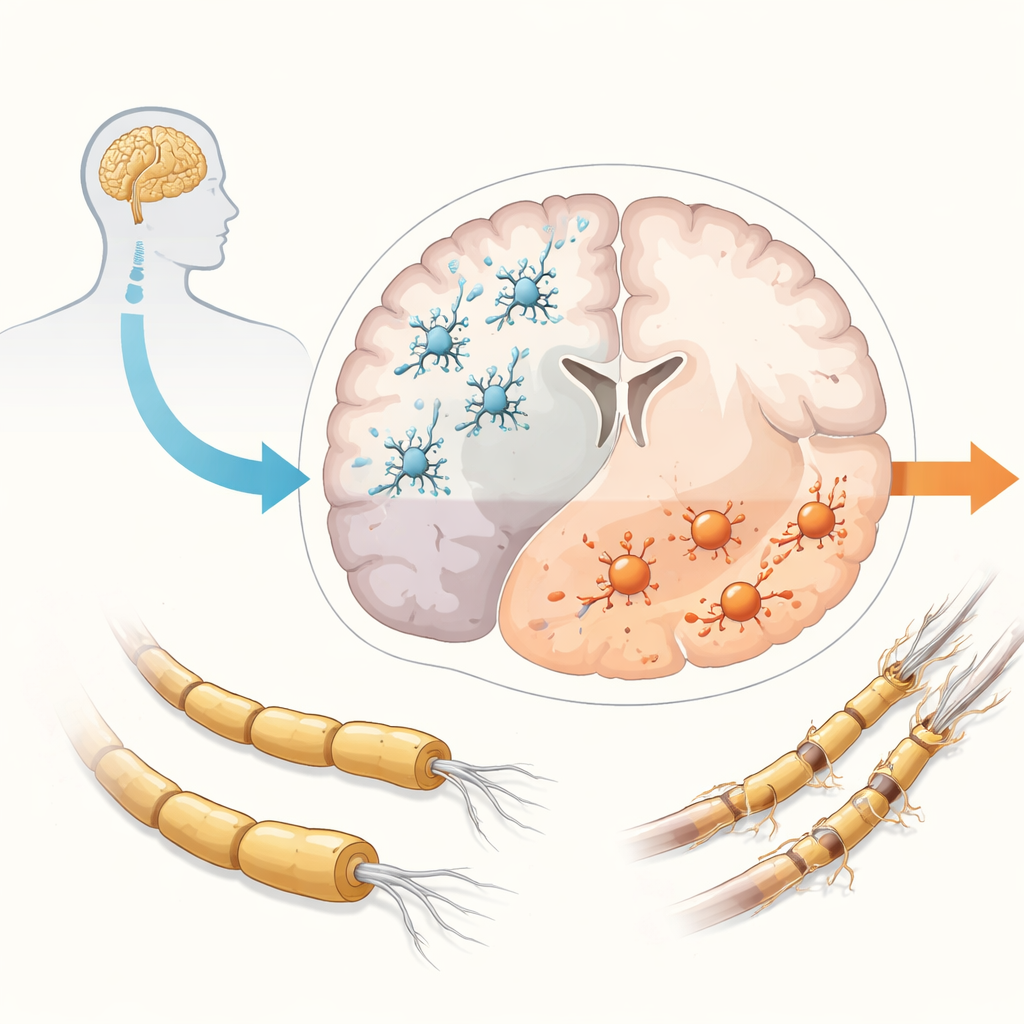
MS is traditioneel opgedeeld in relapsing- en progressieve vormen, maar bewijs toont nu dat progressie zeer vroeg begint bij vrijwel iedereen met de ziekte, zelfs wanneer ze nog alleen relapses lijken te hebben. Terwijl relapses worden aangedreven door immuuncellen die vanuit het bloed binnenkomen, lijkt progressie te worden gevoed door ontsteking die opgesloten raakt binnen de hersenen en het ruggenmerg. In deze afgesloten omgeving zijn microglia betrokken bij veel schadelijke processen: aanhoudende ontsteking, verlies van de isolerende myelinebekleding van zenuwvezels in zowel wit als grijs stof, ophoping van schadelijke zuurstofgerelateerde stoffen en falen van herstel. Het eindresultaat is het geleidelijke verlies van zenuwcellen en hun verbindingen. Microglia helpen normaal gesproken het brein gezond te houden door afval op te ruimen en zenuwcellen te ondersteunen, maar bij MS verschuiven ze vaak naar agressievere toestanden en verliezen ze sommige van hun beschermende rollen, waardoor ze hoofdverdachten zijn in het aandrijven van progressie.
Waarom traditionele diermodellen tekortschieten
Decennialang waren studies in muizen en andere dieren cruciaal voor het ontwikkelen van geneesmiddelen die relapses beperken, maar ze hebben grotendeels gefaald in het opleveren van therapieën die progressie stoppen. Een reden is dat diermodellen MS slechts gedeeltelijk nabootsen en de complexe, langdurige ontsteking die bij patiënten in de hersenen wordt gezien niet volledig reproduceren. Microglia van knaagdieren verschillen ook op belangrijke genen en reacties van menselijke microglia. Als gevolg daarvan werken behandelingen die veelbelovend lijken in dieren vaak niet bij mensen. Het tekort aan diermodellen die daadwerkelijk progressieve MS vangen heeft onderzoekers ertoe aangezet nieuwe op menselijke cellen gebaseerde systemen in het laboratorium te bouwen, waar ze microglia en andere hersencellen directer kunnen bestuderen.
Menselijke hersenmodellen in een schaaltje opbouwen
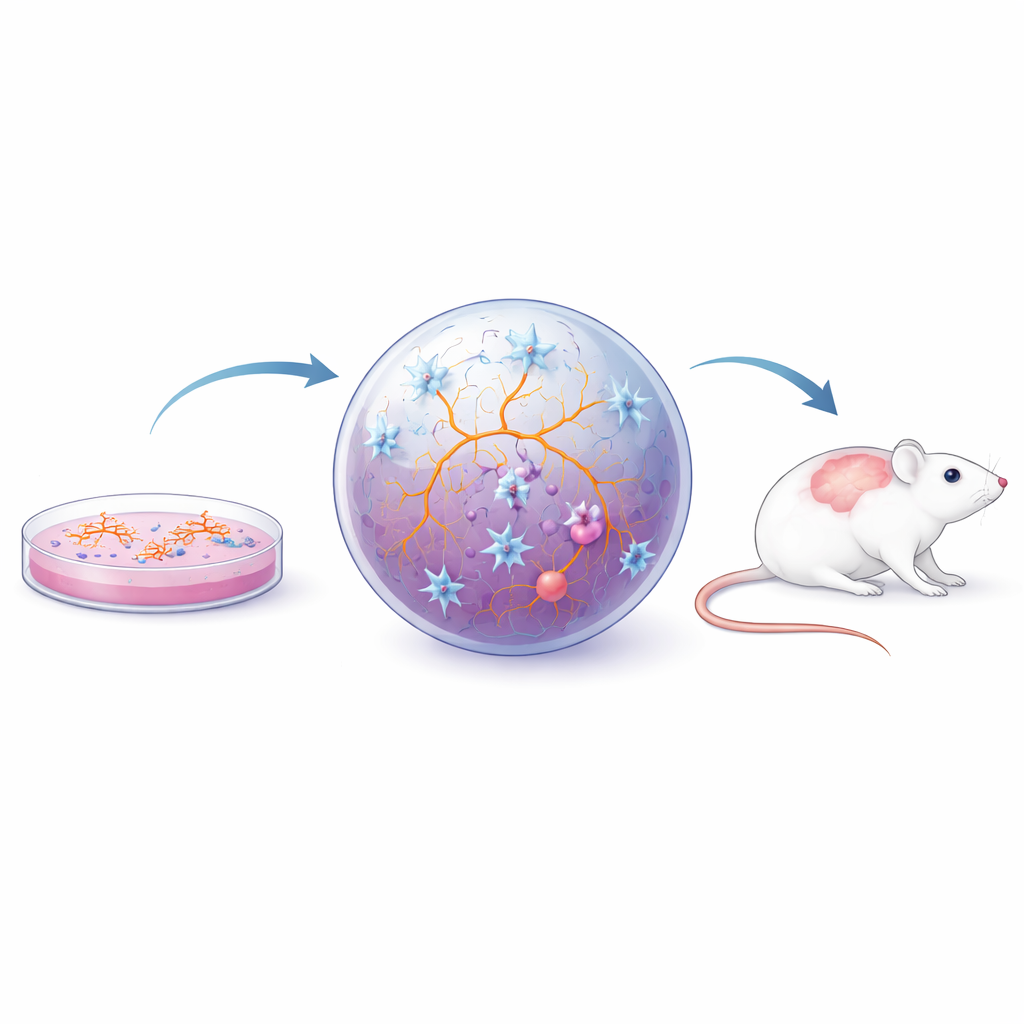
Wetenschappers gebruiken nu verschillende lagen aan laboratoriummodellen om menselijke microglia te bestuderen. Primaire cellen die rechtstreeks uit knaagdier- of menselijk hersenweefsel worden genomen behouden veel natuurlijke kenmerken maar zijn moeilijk te verkrijgen, veranderen snel buiten hun natuurlijke omgeving en zijn niet gemakkelijk op te schalen. Om deze obstakels te overwinnen, schakelen onderzoekers over op geïnduceerde pluripotente stamcellen (iPS) — volwassen cellen die teruggeprogrammeerd zijn naar een flexibele, stamcelachtige staat. Deze iPS-cellen kunnen worden gestuurd om microglia, neuronen of andere hersencellen te worden. In eenvoudige platte kweekomgevingen vangen iPS-afgeleide microglia veel kernmerken en kunnen ze in grote aantallen worden geproduceerd, wat gedetailleerde experimenten en geneesmiddenschermen mogelijk maakt. Ze kunnen zelfs worden gemaakt van individuele MS-patiënten, waardoor ingebouwde verschillen aan het licht komen zoals veranderde genactiviteit en verschillen in hoe deze cellen reageren op stress en afval opruimen.
Realistische hersenomgevingen toevoegen
Aangezien het gedrag van microglia sterk wordt gevormd door hun omgeving, zijn onderzoekers verder gegaan dan enkelvoudige cellagen naar realistischere opstellingen. In tweedimensionale coculturen groeien microglia samen met neuronen en ondersteunende cellen, wat hen helpt meer natuurlijke vormen en gedrag aan te nemen en wetenschappers in staat stelt te onderzoeken hoe celtypen elkaar beïnvloeden. Driedimensionale sferoïden en organoïden — kleine, zelf-organiserende stukken hersenachtig weefsel — gaan verder en bieden een zachte, drukke omgeving die meer lijkt op daadwerkelijk hersenweefsel. Wanneer microglia in deze structuren ingebed zijn, vertonen ze complexe vertakkingen, reageren ze op letsel, interageren ze met een bloed–hersenbarrière-achtige laag en reageren ze op inflammatoire signalen uit het ruggenmergvocht van mensen met MS. Dergelijke modellen zijn gebruikt om te bestuderen hoe chronische ontsteking een "moe maar ontstoken" toestand kan veroorzaken die cellulaire senescentie wordt genoemd in microglia en astrocyten, en hoe veranderingen in de vetstofwisseling van microglia myelinereparatie kunnen belemmeren. Parallel daaraan maakt transplantatie van menselijke iPS-afgeleide microglia of organoïden in muizenhersenen het mogelijk dat deze cellen verder rijpen binnen een levend netwerk en getest worden in gevestigde MS-achtige ziektemodellen.
Van laboratoriummodellen naar toekomstige behandelingen
Gezamenlijk vormen deze op menselijke cellen gebaseerde in vitro- en chimerische modellen een gereedschapskist om te ontrafelen hoe microglia bijdragen aan MS-progressie en om nieuwe therapieën te testen die schadelijke microgliaire activiteit willen kalmeren terwijl hun beschermende functies worden hersteld. Hoewel geen enkel model de menselijke hersenen volledig reproduceert, legt elk model verschillende stukjes van de puzzel vast, en samen overbruggen ze de kloof tussen eenvoudige celkweken en onvolmaakte diermodellen. Door inzichten uit deze systemen te combineren hopen onderzoekers precieze geneesmiddeldoelen te identificeren — zoals pathways die ontsteking, verouderingsachtige veranderingen en lipidenstofwisseling in microglia reguleren — die mogelijk kunnen worden vertaald naar behandelingen die de geleidelijke invaliditeit kenmerken van progressieve MS eindelijk vertragen of stoppen.
Bronvermelding: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Trefwoorden: progressie van multiple sclerose, microglia, geïnduceerde pluripotente stamcellen, hersenorganoïden, neuro-inflammatie