Clear Sky Science · nl
Een ESRP1/circPHGDH/miR-149/RAP1B-positieve terugkoppelingslus bevordert de kwaadaardige eigenschappen en glycolyse van prostaatkankercellen
Waarom dit onderzoek belangrijk is voor mannengesondheid
Prostaatkanker is een van de meest voorkomende vormen van kanker bij mannen, en veel tumoren worden uiteindelijk agressief en resistent tegen behandeling. Deze studie onthult een verborgen regelkring binnen prostaatkankercellen die hen helpt sneller te groeien, zich eenvoudiger te verspreiden en de manier waarop ze suiker verbranden voor energie te herprogrammeren. Door deze moleculaire lus in kaart te brengen wijzen de onderzoekers op nieuwe kwetsbare plekken die mogelijk gericht kunnen worden om de ziekte te vertragen of bestaande therapieën effectiever te maken.
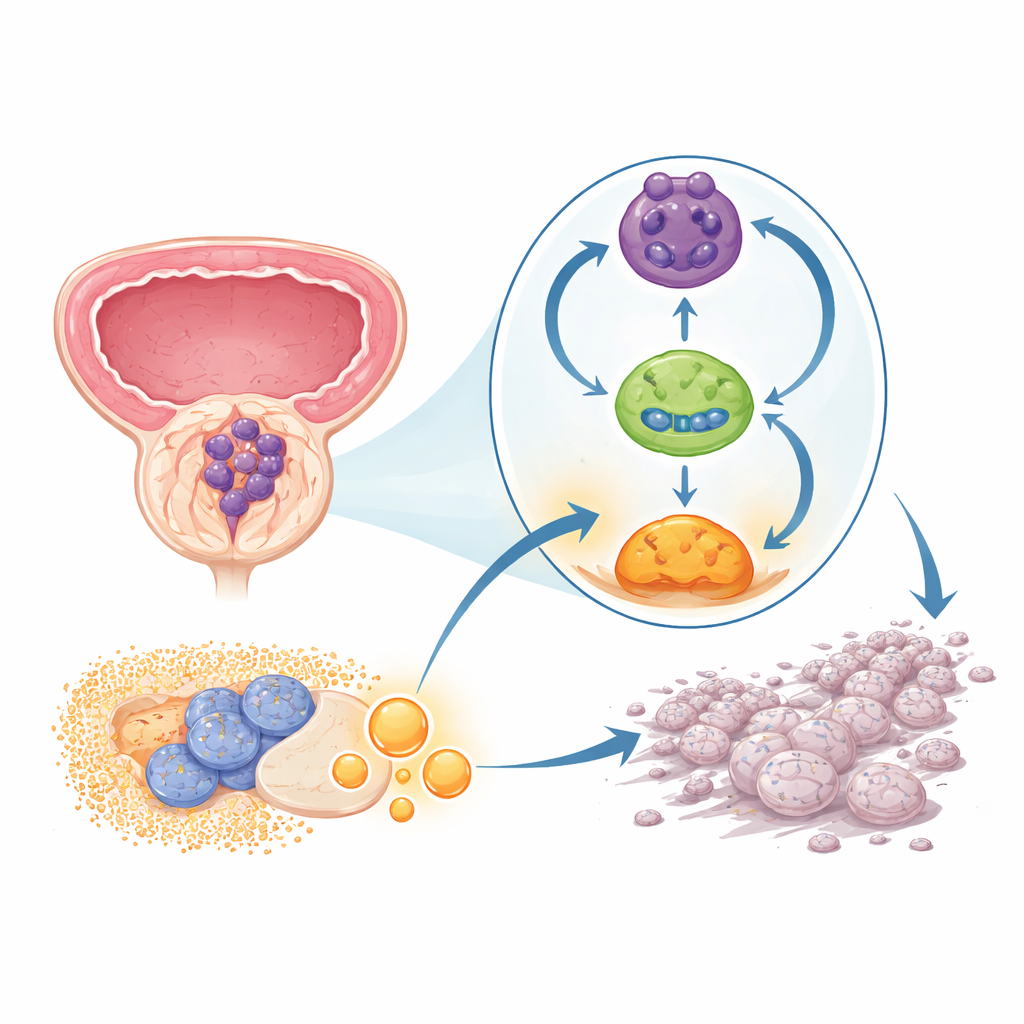
Een verborgen lus die kanker aanhoudt
Het team richtte zich op een recent erkende klasse genetisch materiaal: circulaire RNA’s. In tegenstelling tot de gebruikelijke lineaire strengen vormen deze moleculen gesloten ringen en zijn ze opmerkelijk stabiel. In prostaattumormonsters en kweeklijnen vonden de onderzoekers één specifieke circulaire RNA, genoemd circPHGDH, die consequent hoger aanwezig was dan in nabijgelegen niet-kankerachtig weefsel. Patiënten van wie de tumoren meer van dit RNA hadden, bleken doorgaans grotere tumoren, lokaal gevorderdere groei en uitzaaiingen te hebben, wat erop wijst dat circPHGDH bijdraagt aan een gevaarlijker vorm van de ziekte.
Hoe kankercellen hun gedrag veranderen
Om te achterhalen wat circPHGDH precies doet, veranderden de onderzoekers de niveaus ervan in prostaattumorcellen die in het laboratorium werden gekweekt. Wanneer zij circPHGDH verminderden, vormden de cellen minder kolonies, bewogen en drongen zij minder effectief door membranen en toonden ze tekenen dat ze in een meer "epitheliale" toestand bleven die minder geneigd is te verspreiden. Tegelijkertijd schoof het metabolisme van de cellen weg van de suiker-verlangende stijl die kenmerkend is voor veel tumoren: hun afhankelijkheid van glycolyse daalde en ze gebruikten meer zuurstofgebaseerde energieproductie. Toen circPHGDH juist werd opgevoerd, bewogen al deze kankerversterkende eigenschappen in de tegengestelde richting.
Kleine RNA’s en een groeisignaalrelay
De studie volgde vervolgens hoe circPHGDH deze effecten uitoefent. In het celplasma werkt circPHGDH als een spons voor een klein regulerend RNA, miR-149, door het op te nemen en te verhinderen dat het zijn gebruikelijke doelen remt. Een belangrijk doelwit is RAP1B, een signaaleiwit dat inwerkt op een belangrijke groeien overlevingsroute die bekendstaat als relevant voor prostaatkanker. Wanneer miR-149 wordt geblokkeerd door circPHGDH, stijgen de RAP1B-niveaus en schakelen zij downstreamsignalen in die celdeling, beweging en een glycolyse-intensief metabolisme bevorderen. Het herstellen van miR-149 of het direct verminderen van RAP1B keerde veel van de schadelijke effecten om, zowel in celkweken als in muizen met humane prostaattumoren.
Metabool afval dat het vuur aanwakkert
Een andere laag van het verhaal betreft hoe circPHGDH in de eerste plaats wordt geproduceerd. De vorming ervan hangt af van een splicing-eiwit genaamd ESRP1, dat helpt bepalen hoe ruwe RNA-boodschappen worden geknipt en opnieuw aan elkaar gezet. De onderzoekers toonden aan dat ESRP1 specifieke sites rond het circPHGDH-gebied bindt en de circulaire vorm boven de standaard lineaire versie bevoordeelt. Cruciaal was de ontdekking dat lactaat—het eindproduct van glycolyse—chemisch ESRP1 modificeert op een enkele plaats, waardoor het eiwit stabieler wordt. Omdat circPHGDH zelf cellen naar meer glycolyse en dus meer lactaat duwt, ontstaat hierdoor een zelfversterkende lus: ESRP1 verhoogt circPHGDH, circPHGDH versterkt RAP1B en glycolyse, glycolyse genereert lactaat, en lactaat stabiliseert op zijn beurt ESRP1.
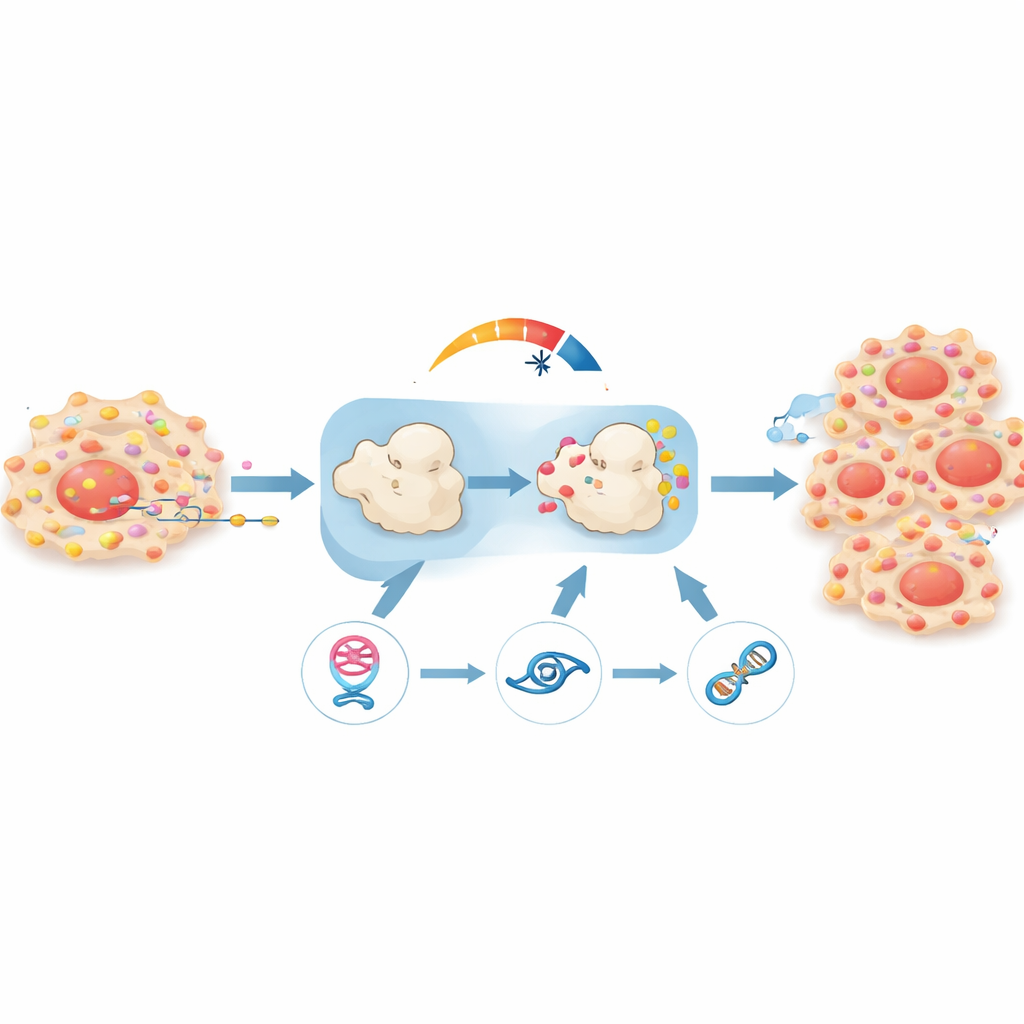
Bewijs uit diermodellen
Om te testen of deze lus echt van belang is in een levend organisme, implanteerde het team humane prostaatkankercellen in muizen. Tumoren waarvan circPHGDH was stilgelegd groeiden langzamer, wogen minder en toonden minder tekenen van uitzaaiing, zoals gemeten met totaallichaamsbeeldvorming en weefselanalyse. Merkers van celproliferatie waren lager en de tumorstructuur zag er minder agressief uit onder de microscoop. Toen de onderzoekers in dezelfde tumoren miR-149 blokkeerden of RAP1B weer omhoog brachten, keerde veel van de groei en verspreiding terug, wat bevestigt dat de circPHGDH–miR-149–RAP1B-keten een centrale motor van ziektegedrag is.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk onthullen de bevindingen een positieve terugkoppelingslus waarin een splicing-eiwit, een circulair RNA, een klein regulerend RNA en een signaaleiwit samenwerken om prostaatkankercellen aan te zetten tot snelle groei, invasie en suikerhongerig metabolisme. Voor niet-specialisten is de kernboodschap dat kankercellen hun genetische en metabole controles in zelfversterkende circuits kunnen organiseren die de ziektetoestand in stand houden. Het doorbreken van deze lus—door circPHGDH te verstoren, miR-149 te herstellen, RAP1B te blokkeren of de lactaatafhankelijke modificatie van ESRP1 te verhinderen—biedt meerdere veelbelovende wegen voor toekomstige geneesmiddelen gericht op het vertragen of stoppen van agressieve prostaatkanker.
Bronvermelding: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
Trefwoorden: prostaatkanker, circulaire RNA, tumormetabolisme, microRNA, signaalroutes