Clear Sky Science · nl
PAK4 bij stofwisselingsziekten: regulatie door voedingssignalen en therapeutische implicaties
Waarom een cellulaire schakel belangrijk is voor alledaagse gezondheid
Obesitas, type 2-diabetes en vette lever worden vaak alleen aan calorieën toegeschreven, maar diep in onze cellen beslissen moleculaire schakelaars of we brandstof verbranden of opslaan. Deze review richt zich op een van die schakelaars, een eiwit genaamd PAK4, en legt uit hoe het reageert op veranderende voedings- en hormoonsignalen en daarmee het metabolisme in vet, lever en spier herschikt. Inzicht in dit verborgen stuursysteem kan de weg openen naar nieuwe behandelingen die meerdere stofwisselingsziekten tegelijk aanpakken in plaats van één symptoom per keer. 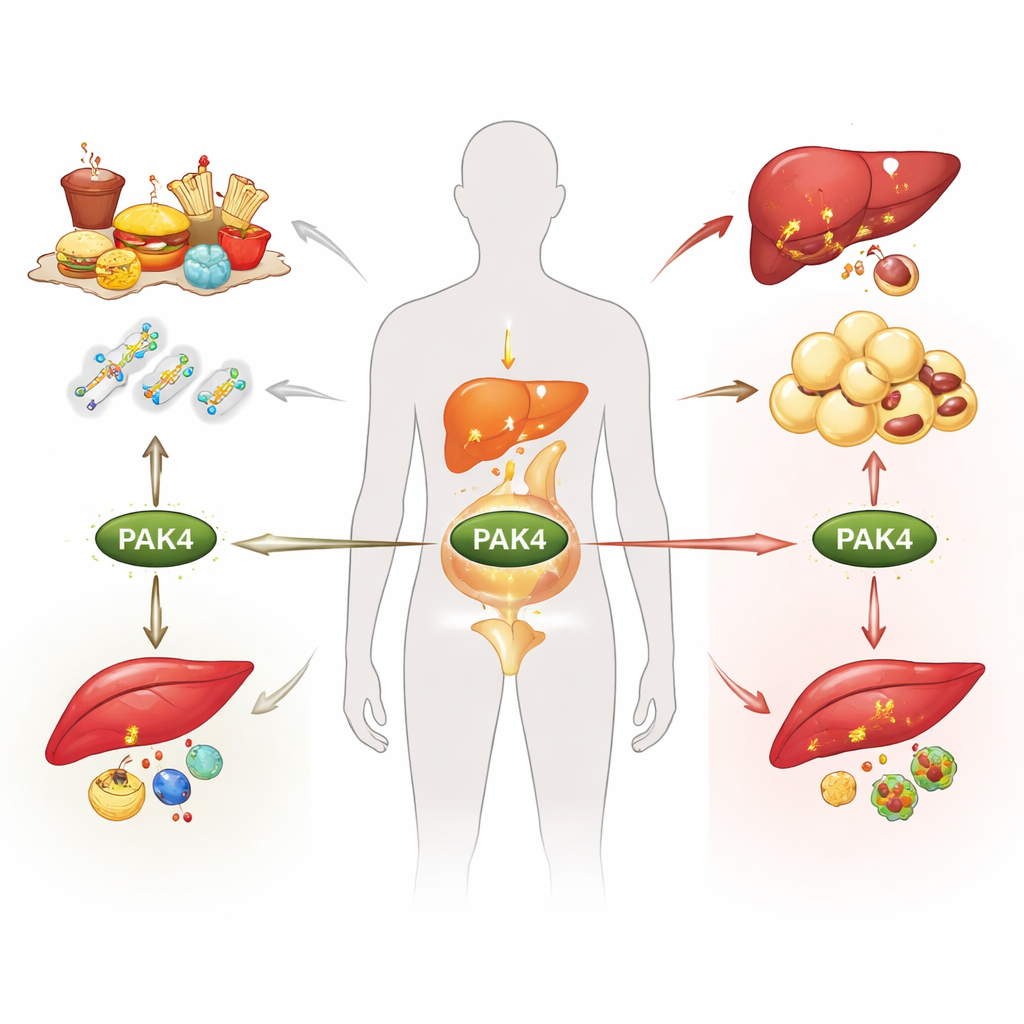
Een hoofdschakel verborgen in onze cellen
PAK4 behoort tot een familie van enzymen die signalen doorgeven van kleine moleculaire “boodschappers” binnen cellen. In gezonde omstandigheden is PAK4 op lage niveaus aanwezig in belangrijke metabole organen. Wanneer de energiebalans verstoord is, zoals bij obesitas of type 2-diabetes, nemen de niveaus toe in vetweefsel, lever en skeletspier. De activiteit van PAK4 wordt op verschillende manieren gereguleerd: door upstream-boodschappers die de vorm veranderen en door chemische labels die na de eiwitsynthese worden toegevoegd of verwijderd. Daartoe behoren fosfaatlabels die PAK4 kunnen activeren of juist markeren voor afbraak, evenals labels die de stabiliteit of activiteit beïnvloeden. Vasten, voeding, hormonen en stress beïnvloeden deze labels, zodat PAK4 effectief de voedingsstatus van het lichaam “voelt” en die informatie doorgeeft aan belangrijke metabole routes.
Hoe PAK4 vetcellen naar opslag kantelt
In vetcellen fungeert PAK4 als een rem op vetverbranding. Normaal gesproken, wanneer we vasten of wanneer stresshormonen stijgen, activeert een ander enzym genaamd PKA de gecontroleerde afbraak van opgeslagen vet in kleine druppeltjes. De review beschrijft hoe PAK4 dit proces tegenwerkt door remmende fosfaatlabels rechtstreeks aan hormoongevoelige lipase en aan een vetzuurbindend eiwit dat vetmoleculen helpt transporteren, toe te voegen. Deze veranderingen verzwakken de machinerie die vet uit opslag vrijmaakt. PAK4 ondersteunt ook de vorming van nieuwe vetcellen vroeg in het leven door celcykleiwitten te helpen precursorcellen te laten uitrijpen tot volwassen vetopslagcellen. Wanneer PAK4 in diermodellen wordt verwijderd of geblokkeerd, verbranden vetcellen meer brandstof, vertonen ze kenmerken van “bruning” die het energieverbruik verhogen, en zijn dieren beschermd tegen door dieet veroorzaakte gewichtstoename. 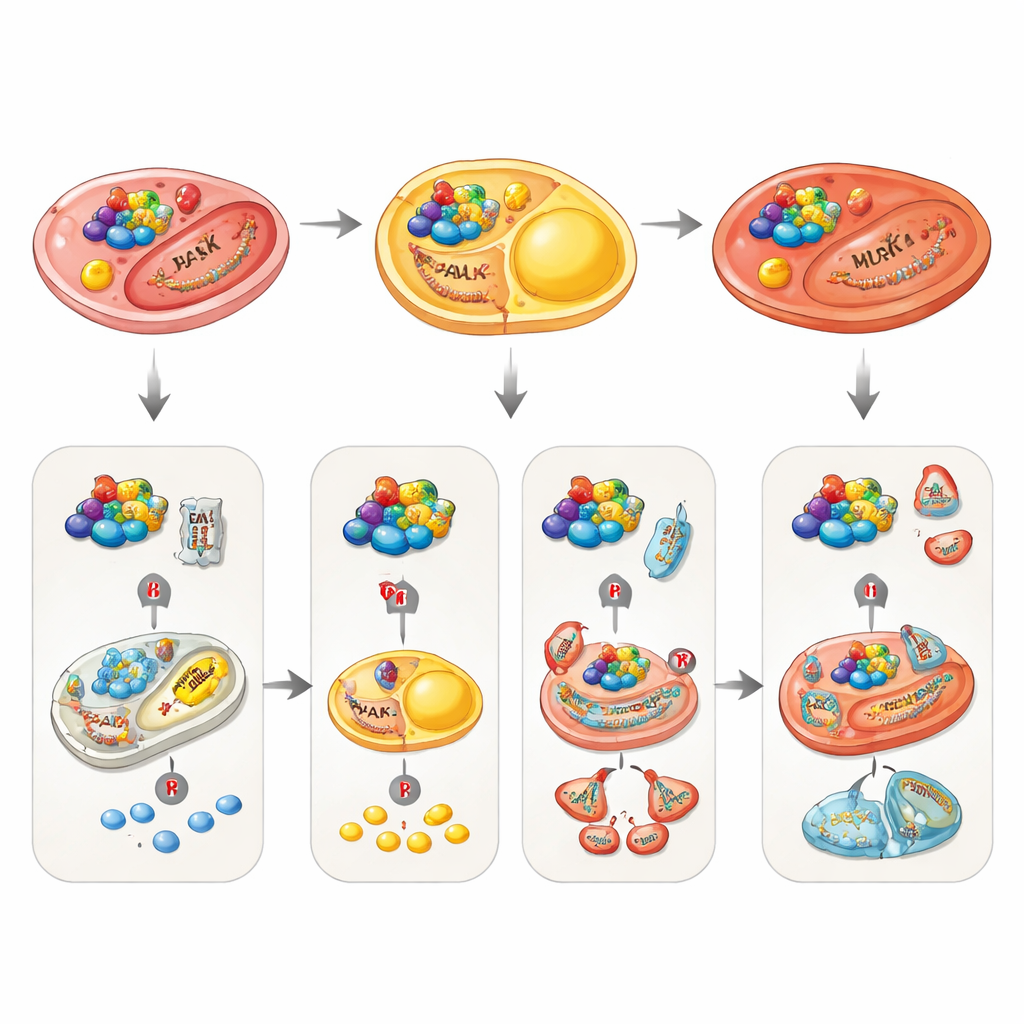
PAK4’s rol bij vette lever en suikerverwerking in spieren
In de lever bevordert PAK4 opnieuw opslag boven verbranding. Tijdens vasten of bij een ketogeen dieet dalen de PAK4-niveaus, waardoor levercellen vetafbraak en ketonproductie kunnen opvoeren, die andere weefsels van energie voorzien en mogelijk zelfs tumorgroei remmen. Wanneer PAK4 overvloedig is, voegt het fosfaatlabels toe aan een nucleair corepressor-eiwit dat vervolgens PPARα, een hoofdregelaar van vetoxidatie en ketenvorming, onderdrukt. Het resultaat is meer vet opgesloten in de lever en minder beschermende ketonen in de bloedbaan. In skeletspier verstoort PAK4 AMPK, een centraal energiezintuig dat zowel de opname van suiker als de mitochondriale activiteit bevordert. Door AMPK zodanig te labelen dat het niet geactiveerd wordt, verlaagt PAK4 de hoeveelheid glucose-transporteur aan het spierceloppervlak en draagt het bij aan insulineresistentie. Spierspecifiek verlies van PAK4 bij muizen keert deze effecten om en verbetert de bloedsuikercontrole, zelfs onder obese omstandigheden.
Stress, bescherming en koppelingen met andere cel-schakelaars
De review belicht ook de impact van PAK4 buiten de alledaagse stofwisseling. Tijdens periodes van verminderde bloedtoevoer en plotselinge reperfusie in organen zoals de lever verzwakt PAK4 de antioxidatieve verdediging door Nrf2 te labelen en te destabiliseren, een belangrijke beschermer tegen oxidatieve stress. Tegelijkertijd vervult een ander familie-lid, PAK1, vaak meer ondersteunende rollen in hartspier, skeletspier en insulinesecreterende cellen van de alvleesklier, en helpt het de normale glucosehuishouding te behouden. Dit contrast tussen schadelijke PAK4-signalen bij stofwisselingsziekte en overwegend voordelige PAK1-werkingen benadrukt de noodzaak van zeer selectieve geneesmiddelen die PAK4 uitschakelen zonder verwante eiwitten te verstoren die essentieel zijn voor hart- en endocriene gezondheid.
Van ontdekking naar behandeling
Aangezien PAK4 overactief is bij kanker en bij stofwisselingsstoornissen, hebben geneesmiddelontwerpers kleine moleculen ontwikkeld die de activiteit blokkeren, evenals nieuwe “degrader”-geneesmiddelen die PAK4 zelf markeren voor verwijdering. Vroege PAK4-remmers toonden antitumorperspectief maar liepen tegen uitdagingen aan wat betreft specificiteit en farmacokinetiek. Recente moleculen die PAK4 preciezer targeten, hebben opvallende resultaten opgeleverd bij obese muizen: lager lichaamsgewicht zonder minder eten, gezondere leverfuncties, actievere spieren en verbeterde bloedsuikercontrole. Degrader-geneesmiddelen gaan een stap verder door PAK4 fysiek uit te schakelen, en vroege dierstudies suggereren dat ze mogelijk beschermen tegen spierverlies en bepaalde vormen van kanker. Gezamenlijk ondersteunen deze bevindingen het beeld dat het terugschakelen van PAK4 gelijktijdig obesitas, diabetes en vette lever zou kunnen verlichten, waardoor een vroeger obscure cellulaire schakel een veelbelovende focus wordt voor toekomstige metabole therapieën.
Bronvermelding: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Trefwoorden: PAK4, stofwisselingsziekte, obesitas, vettige lever, insulineresistentie