Clear Sky Science · nl
Het redox-gevoelige eiwit HMGB1: intracellulaire en extracellulaire rollen
Waarom een vormveranderend eiwit van belang is voor de gezondheid
In bijna elke cel van je lichaam bevindt zich een klein eiwit genaamd HMGB1 dat zich als een multitool gedraagt. In rustige omstandigheden helpt het stilletjes bij het organiseren van DNA. Maar wanneer cellen gestrest of beschadigd zijn, kan HMGB1 uit de kern verplaatsen, in het omliggende weefsel terechtkomen en als alarmsein voor het immuunsysteem fungeren. Dit overzichtsartikel legt uit hoe kleine chemische veranderingen door oxidatie HMGB1 omvormen tot zeer verschillende biologische persoonlijkheden — die weefsels kunnen beschermen, ontsteking kunnen aanwakkeren of zelfs kunnen bijdragen aan chronische ziekte. Inzicht in deze moleculaire "moodring" kan nieuwe manieren openen om overmatige ontsteking te dempen zonder het immuunsysteem volledig uit te schakelen.
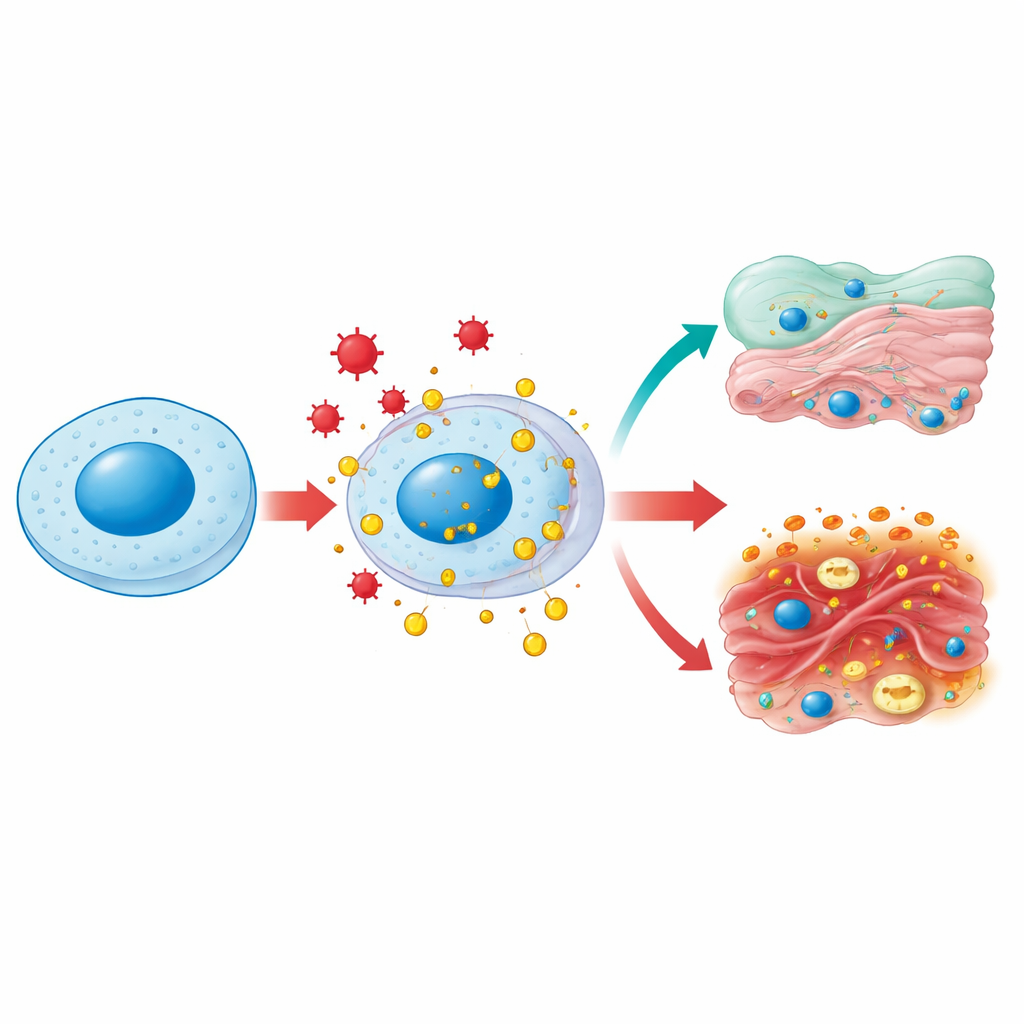
Eén eiwit, vele buurtjes
HMGB1 woont normaal gesproken in de celkern, waar het DNA buigt en losmaakt zodat genen gekopieerd en gerepareerd kunnen worden. Onder stress — zoals bij infectie, hoge bloedsuiker of toxische schade — kan het chemisch gemodificeerd worden en naar het waterige inwendige van de cel en vervolgens naar de buitenwereld begeleid worden. In het cytoplasma helpt HMGB1 de mitochondriën, de energiecentrales van de cel, gezond te houden door een opruimproces genaamd autofagie te bevorderen en door overmatige fragmentatie van deze organellen te voorkomen. Wanneer HMGB1 buiten de cel vrijkomt, wordt het een klassiek "gevaarssignaal": immuuncellen herkennen het als een teken dat weefsels beschadigd zijn en haasten zich naar de plek. Hetzelfde molecuul vervult dus huishoudelijke rollen binnenin de cel en alarmgevende rollen erbuiten, afhankelijk van waar het zich bevindt en hoe het chemisch is afgesteld.
Hoe oxidatie zijn gedrag herschrijft
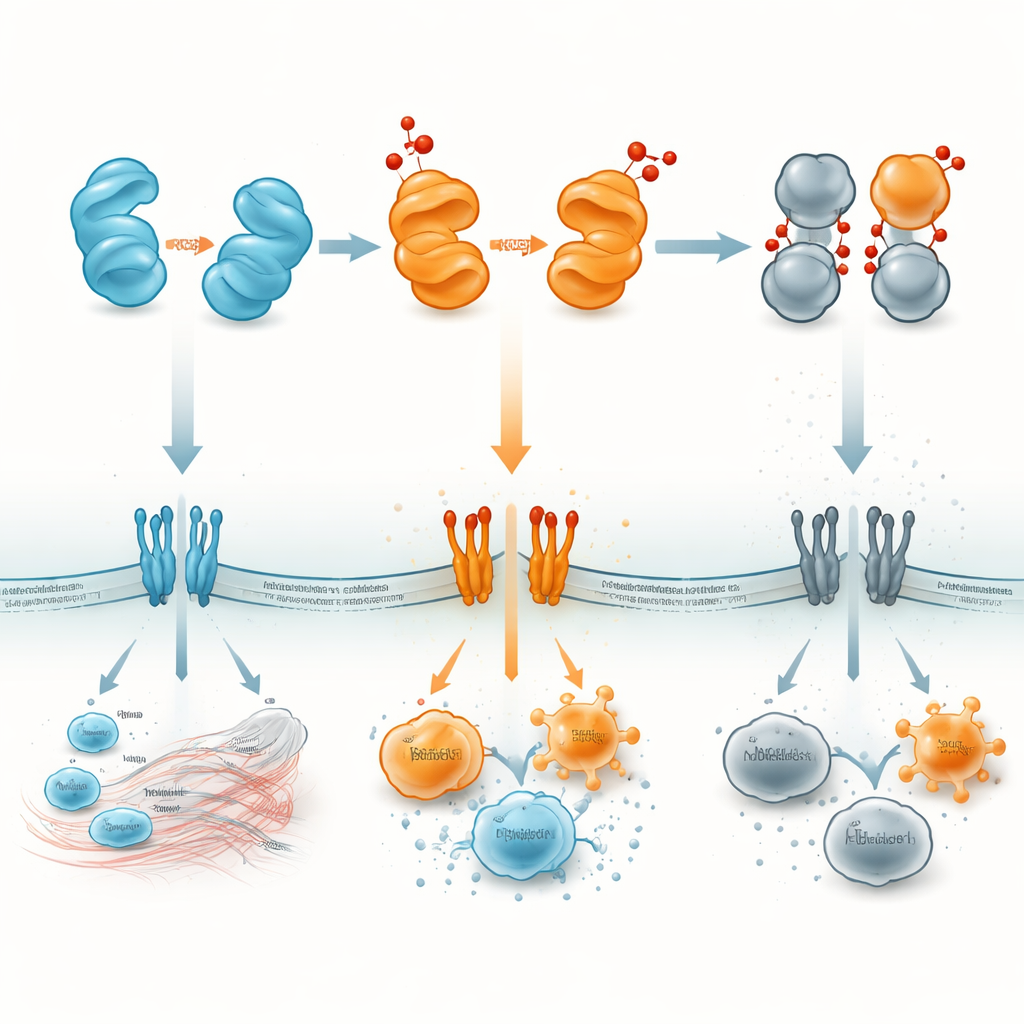
Het middelpunt van dit overzicht is hoe oxidatie — reacties aangedreven door reactieve zuurstofsoorten (ROS) — HMGB1 hervormt. Het eiwit bevat drie zwavelhoudende bouwstenen die als kleine schakelaars werken. In hun volledig gereduceerde staat ondersteunt HMGB1 vaak celoverleving en de aantrekking van herstelcellen. Milde oxidatie kan twee van deze locaties binnen hetzelfde eiwit aan elkaar koppelen, waardoor een "disulfide"-vorm ontstaat die bijzonder goed hecht aan immuunreceptoren zoals Toll-like receptors en RAGE op celoppervlakken. Deze versie stimuleert sterk de productie van ontstekingsboodschappers. Sterkere oxidatieve stress kan het molecuul verder in een overgeoxideerde vorm drukken die niet langer effectief DNA of receptoren kan binden; deze "verbrande" versie wordt immunologisch stil en wordt geassocieerd met de resolutiefase van ontsteking en met celdoodprogramma’s die geen immuunreactie uitlokken.
Van celdoodsignalen naar ziekteveroorzakers
HMGB1 is diep verweven met de vele manieren waarop cellen overlijden. Tijdens gewelddadige vormen van celdood zoals necrose, necroptose, ferroptose en pyroptose lekt HMGB1 of wordt het actief uit cellen getransporteerd, waarbij het een redox‑handtekening draagt die de omringende oxidatieve omstandigheden weerspiegelt. Vroeg in necrose is het vaak in gereduceerde vorm, terwijl langdurige stress het naar meer geoxideerde staten drijft. Eenmaal buiten kan gereduceerd HMGB1 in sommige kankercellen beschermende autofagie bevorderen en zo hun overleving tijdens chemotherapie ondersteunen, terwijl disulfide‑rijke en gedimeriseerde vormen ontstekingscascade en complementactivatie versterken die weefselschade kunnen verergeren. HMGB1 kan ook terugkoppelen om bepaalde doodspaden te bevorderen — bijvoorbeeld door samen te werken met bacteriële lipiden om necroptose te triggeren of door ijzafhankelijke celdood in ondersteunende hersencellen na een beroerte te stimuleren. Op deze manier markeert en moduleert HMGB1 zowel het evenwicht tussen leven en dood in weefsels.
Verbindingen met ontsteking, auto-immuniteit en kanker
Omdat zijn gedrag zo gevoelig is voor oxidatie, komen verschillende HMGB1-varianten in uiteenlopende patronen bij ziektes voor. Disulfide‑rijke HMGB1 wordt sterk geassocieerd met chronische ontsteking: het verschijnt in ontstoken gewrichten bij reumatoïde artritis, in fibrotische lever, bij longschade, bij ischemie–reperfusieschade na een operatie en bij sepsis, waar de bloedspiegels correleren met ernst en sterfterisico. Gereduceerd HMGB1 daarentegen volgt vaak celmigratie en weefselhermodellering, zoals de verplaatsing van hartfibroblasten of monocyten geleid door het chemokine CXCL12. Overgeoxideerd, immunologisch stil HMGB1 is verrijkt in situaties zoals laatstadium apoptose, waar het lichaam dode cellen wil opruimen zonder een aanval uit te lokken. In tumoren ondersteunt de disulfide‑vorm een onderdrukkend, groei‑toegankelijk immuunmilieu, terwijl het blokkeren van HMGB1 tumoren kan laten krimpen en checkpoint‑immuuntherapieën effectiever kan maken.
Een moleculair alarm tot therapeutisch doel maken
Voor een niet‑expert kan HMGB1 gezien worden als een klein eiwitalarm waarvan volume en boodschap veranderen met zijn chemische toestand. Gereduceerd HMGB1 roept vaak herstelploegen; de disulfide‑ en dimeren vormen kunnen een hard alarm laten afgaan dat schadelijke ontsteking voedt; en de volledig geoxideerde vorm valt praktisch stil en helpt ontsteking te laten afnemen. Door in kaart te brengen waar en wanneer elke versie verschijnt — in kernen, in het cytoplasma, in het bloed of in specifieke organen — hopen onderzoekers geneesmiddelen te ontwerpen die ofwel de schadelijke vormen blokkeren ofwel de nuttige stabiliseren. Dergelijke strategieën zouden artsen in staat kunnen stellen sepsis, auto‑immuniteit, beroerte, longschade of kanker te behandelen door niet alleen HMGB1 zelf te richten, maar ook de oxidatieve "dimmer" die bepaalt hoe dit eiwit met het immuunsysteem communiceert.
Bronvermelding: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Trefwoorden: HMGB1, ontsteking, oxidatieve stress, celdood, auto-immuunziekte