Clear Sky Science · nl
UBE2M als een brug tussen neddylatie en celdelingsregulatie bij colorectaal adenocarcinoom
Waarom dit onderzoek van belang is voor darmkanker
Colorectale kanker is een van de meest voorkomende en dodelijke kankers wereldwijd, grotendeels omdat tumorcellen leren om onophoudelijk te delen. Deze studie onthult een voorheen verborgen regelaar die helpt dat colorectale kankercellen een cruciale controlepunt van de celdeling snel passeren. Door te laten zien hoe deze schakel op moleculair niveau werkt — en dat een bestaand schimmelremmend middel die schakel kan verstoren — wijst het werk op een potentiële nieuwe manier om tumorgroei te vertragen of te stoppen.
Een verborgen controlelaag binnen tumorcellen
Cellen delen niet willekeurig; ze doorlopen een ordelijke cyclus met controlepunten die nagaan of het veilig is om DNA te kopiëren en in tweeën te delen. Kankercellen rommelen vaak met deze controlepunten. De auteurs richtten zich op een chemisch labelingsproces genaamd neddylatie, dat eiwitten subtiel verandert na hun aanmaak. Eerdere studies suggereerden dat neddylatie in veel kankers actiever is, maar hoe dit gekoppeld is aan de delingscyclus van colorectale kankercellen was onduidelijk. Met grote single-cell datasets uit menselijke tumoren en bulk genexpressiegegevens van meer dan 1.800 patiënten vond het team dat neddylatie-activiteit vooral hoog is in kwaadaardige darmcellen die zich in de G2/M-fase bevinden — het laatste poortje voordat een cel zich deelt.
In de schijnwerpers: een moleculair “brug”-eiwit
Om uit te zoeken welke moleculen neddylatie aan celdeling koppelen, gebruikten de onderzoekers netwerkachtige computationele analyses om duizenden genen te doorzoeken. Eén eiwit sprong eruit: UBE2M, een enzym dat helpt het kleine NEDD8-label aan andere eiwitten te koppelen. UBE2M was niet alleen sterk verbonden met neddylatie- en celcyclusroutes in de gegevens; het kwam ook veel hoger tot expressie in colorectale tumoren dan in het omringende normale weefsel. Patiënten van wie de tumoren meer UBE2M bevatten, hadden over het algemeen slechtere overleving, wat wijst op een mogelijke drijvende rol in plaats van een bijrol. Wanneer het team UBE2M verminderde in kankercellijnen en in muismodellen met tumoren, vertraagde de tumorgroei, deelden cellen minder en gingen meer cellen geprogrammeerd ten gronde. Omgekeerd versnelde geforceerde overexpressie van UBE2M de groei en voortgang door de celcyclus.
Een relais dat een sleutelgroeipromoter beschermt
Dieper graven leerde de wetenschappers hoe UBE2M cellen helpt delen. Ze ontdekten dat UBE2M niet alleen werkt maar een relais op gang brengt met twee andere eiwitten, USP39 en PABPC1. Normaal wordt PABPC1 bestemd voor afbraak door een keten van ubiquitine-tags, die het naar het cellulaire eiwitafbreeksysteem sturen. Het team toonde aan dat UBE2M USP39 chemisch modificeert met het NEDD8-label. Deze modificatie versterkt USP39’s vermogen om ubiquitine-ketens van PABPC1 af te knippen, waardoor PABPC1 aan afbraak wordt onttrokken en stabieler wordt. Met meer PABPC1 aanwezig is de cel beter in staat specifieke boodschapper-RNA’s te vertalen naar eiwit, waaronder het mRNA voor CCNB1, een cycline die als gaspedaal fungeert voor het G2/M-controlepunt. In wezen helpt UBE2M PABPC1 te stabiliseren, wat op zijn beurt de productie van CCNB1 verhoogt en cellen makkelijker richting deling duwt.
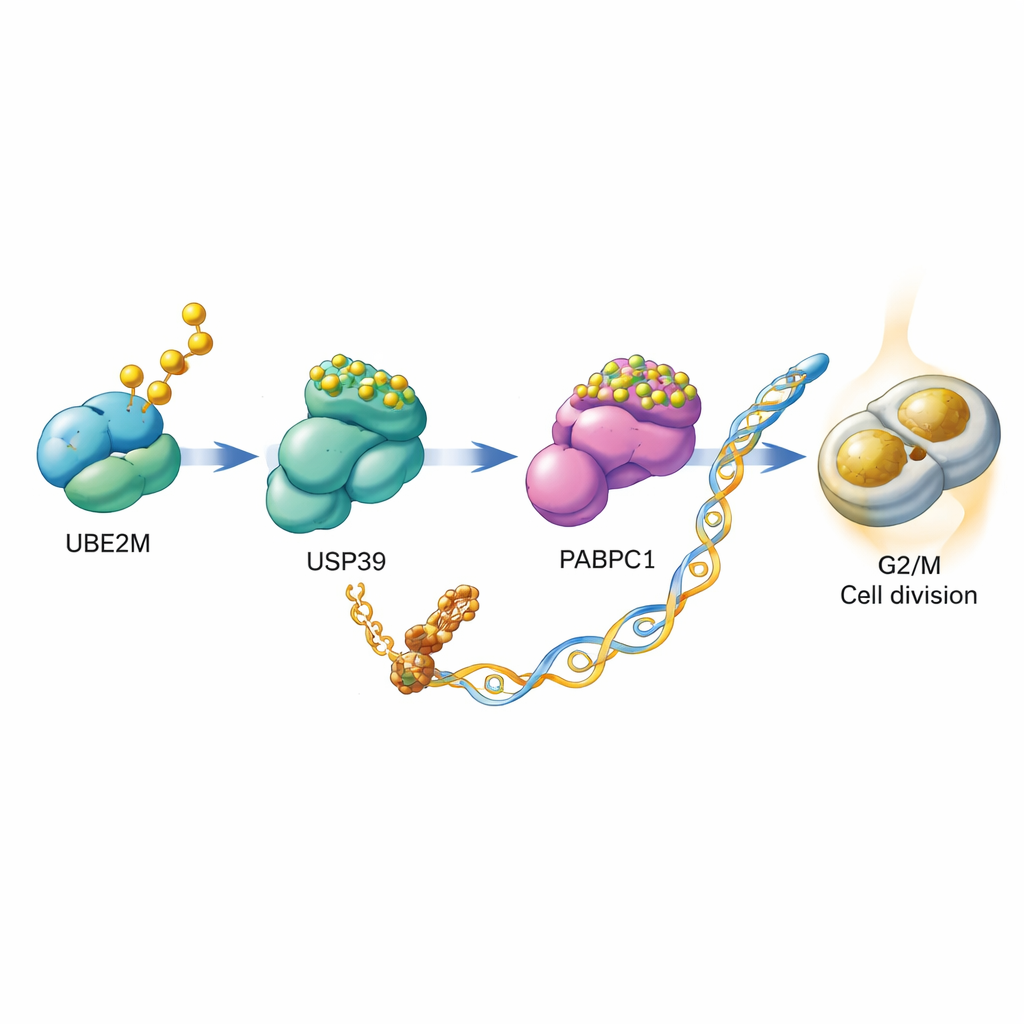
Van moleculair mechanisme naar medicijnkans
De ontdekking van deze UBE2M–USP39–PABPC1–CCNB1-keten wees op een nieuwe kwetsbaarheid in colorectale kankercellen. De auteurs richtten zich op micafungine, een geneesmiddel dat al wordt gebruikt bij schimmelinfecties en recentelijk is geïdentificeerd als remmer van UBE2M’s neddylatie-activiteit. In in vitro gekweekte darmkankercellen verminderde micafungine USP39-neddylatie, verhoogde het de afbraak van PABPC1 en verlaagde het CCNB1-eiwitniveaus. Daardoor vertraagde de celdeling, raakten meer cellen vastgelopen bij het G2/M-controlepunt en nam apoptose toe. In muizen met geïmplanteerde colorectale kankercellen verminderde dagelijkse behandeling met micafungine de tumoromvang significant vergeleken met onbehandelde dieren, zonder dat UBE2M zelf verwijderd hoefde te worden.
Wat dit op de lange termijn voor patiënten betekent
Dit werk schetst een helder beeld van hoe één enzym, UBE2M, een subtiel eiwitlabelingssysteem kan koppelen aan de beslissing van een darmkankercel om te delen. Door een vertaelfactor (PABPC1) via USP39 te stabiliseren, verhoogt UBE2M indirect de niveaus van een krachtige celcyclusstimulator, CCNB1, waardoor tumoren sneller kunnen groeien. Hoewel meer onderzoek en klinische tests noodzakelijk zijn, suggereren de bevindingen dat het blokkeren van dit relais — mogelijk met hergebruikte middelen zoals micafungine — een nieuwe gerichte strategie kan bieden om de progressie van colorectale kanker te vertragen en de uitkomst voor patiënten te verbeteren.
Bronvermelding: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Trefwoorden: dikke darmkanker, celcyclus, neddylatie, UBE2M, gerichte therapie