Clear Sky Science · nl
Geneesmiddel-geïnduceerde gastro-intestinale toxiciteit en barrière-integriteit: cytoskelet-gemedieerde beschadiging in een klinisch relevant humaan intestinaal epitheelmodel
Waarom bijwerkingen in de darm ertoe doen
Veel geneesmiddelen tegen kanker, ontstekingen of andere aandoeningen kunnen onbedoeld het slijmvlies van onze darmen beschadigen. Wanneer deze binnenste “huid” van het darmkanaal aangetast raakt, kunnen mensen last krijgen van diarree, pijn, misselijkheid en slechte voedingsopname, soms zo ernstig dat artsen levensreddende behandelingen moeten stoppen of verlagen. Toch falen de huidige laboratoriumtesten vaak in het opsporen van deze problemen voordat geneesmiddelen bij patiënten komen. Deze studie introduceert een realistischer laboratoriummodel van het menselijk darmepitheel en laat zien hoe het vroegtijdig darmbeschadigende middelen kan opsporen en kan onthullen hoe ze de natuurlijke barrière verzwakken.
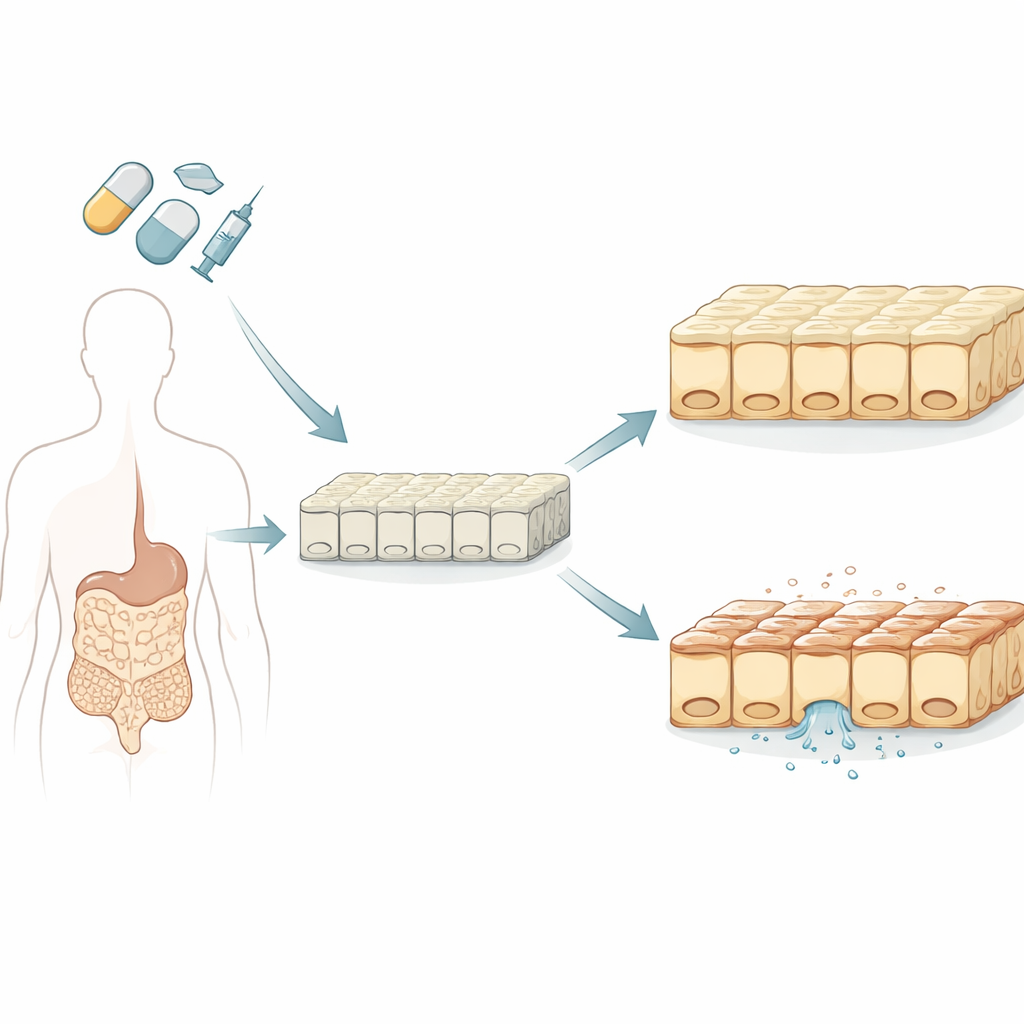
Een beter mini-darm bouwen
De onderzoekers begonnen met het kweken van vellen menselijke darmcellen in het laboratorium uit stamcellen, die zich tot veel weefsels kunnen ontwikkelen. In tegenstelling tot de traditionele, uit kanker afgeleide cellijn die lang voor medicijntests werd gebruikt, vormden deze stamcel-afgeleide cellen een gemengde populatie die nauwer lijkt op de echte dunne darm, inclusief slijmproducerende en hormoonproducerende cellen. Het team bevestigde dat deze in het lab gekweekte bekledingen realistische lekdichtheid hadden, een correcte top- en onderpolariteit en belangrijke transport- en metabole eigenschappen die beïnvloeden hoe geneesmiddelen door de darm bewegen en door de darm worden verwerkt.
De elektrische dichtheid van de barrière meten
Om de veiligheid voor de darm te testen richtte de groep zich op transepithele elektrische weerstand, of TEER, een niet-invasieve maat voor hoe goed aangrenzende cellen afsluiten. Een hoge TEER betekent een strakke, beschermende barrière; een dalende TEER betekent dat de muur tussen darm en bloedbaan lekkend wordt. De wetenschappers vergeleken TEER met een standaardcel-overlevingstest die energiemoleculen zoals ATP meet. Ze stelden zowel hun nieuwe darmmodel als het oudere kankercelmodel bloot aan 17 geneesmiddelen waarvan bekend is dat ze verschillend vaak gastro-intestinale bijwerkingen veroorzaken, waaronder gangbare chemotherapiemiddelen, gerichte kankerpillen en pijnstillers zoals ibuprofen en andere ontstekingsremmers.
Verborgen schade vinden voordat cellen sterven
Over dit panel van geneesmiddelen presteerden TEER-metingen in het stamcel-afgeleide darmslijmvlies beter dan de traditionele ATP-test en de oudere kankercelbarrière. Verschillende chemotherapiemiddelen lieten weinig verandering in ATP zien, wat suggereert dat cellen nog leefden, maar veroorzaakten grote dalingen in TEER en duidelijke schade op live‑dead‑kleuringbeelden. Dit betekent dat de barrière kan falen voordat cellen volledig sterven, een vroegtijdige waarschuwing die klassieke levensvatbaarheidstests missen. Toen het team hun laboratoriumresultaten vergeleek met klinische gegevens over hoe vaak elk geneesmiddel darmklachten veroorzaakt, gaf de nieuwe TEER-assay vrijwel alle hoogrisicomiddelen correct aan en stelde ze gerust voor de laagrisicomiddelen, met een zeer hoge nauwkeurigheid.
Hoe geneesmiddelen het interne skelet ondermijnen
Om te achterhalen wat er binnenin de cellen misging, analyseerden de wetenschappers genexpressie na behandeling met twee chemotherapiemiddelen die microtubuli richten, een belangrijk onderdeel van het interne skelet van de cel. Ze vonden brede verminderingen in genen die betrokken zijn bij het cytoskelet, cel‑tot‑cel‑adhesie en de extracellulaire matrix—het netwerk dat helpt cellen aan hun omgeving te verankeren. Aanvullende experimenten toonden dosisafhankelijke toename van reactieve zuurstofsoorten, onstabiele zuurstofbevattende moleculen die cellulaire structuren kunnen beschadigen. Gezamenlijk wijzen deze veranderingen op een keten van gebeurtenissen waarbij bepaalde geneesmiddelen het interne raamwerk en de verbindingen van darmcellen verstoren, waardoor de barrière losser wordt en stoffen tussen cellen door kunnen lekken.
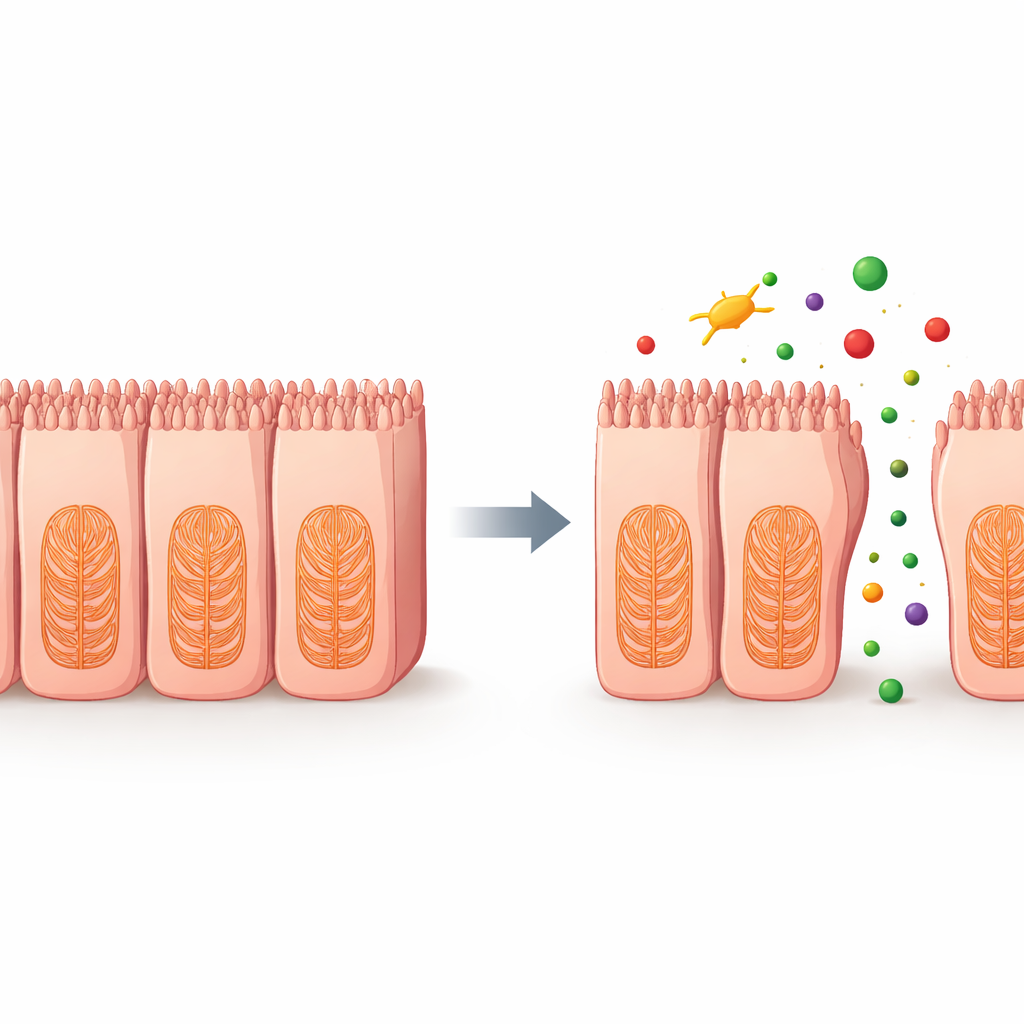
Wat dit voor patiënten betekent
Dit werk toont aan dat een op stamcellen gebaseerd menselijk darmslijmvlies, gekoppeld aan eenvoudige elektrische metingen van barrière‑dichtheid, beter kan voorspellen welke geneesmiddelen waarschijnlijk darmletsel veroorzaken dan langgebruikte labmethoden. Door barrièreverzwakking vroeg te detecteren—en dit te koppelen aan onderliggende schade aan het cellulaire skelet—kan dit platform medicijnontwikkelaars helpen risicovolle verbindingen te verwerpen of te herontwerpen voordat ze de kliniek bereiken. Op de lange termijn kunnen dergelijke realistische “mini‑darm” tests onaangename of gevaarlijke gastro-intestinale bijwerkingen voor patiënten verminderen en artsen in staat stellen krachtige therapieën veiliger toe te passen.
Bronvermelding: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Trefwoorden: gastro-intestinale toxiciteit, intestinale barrière, stamcelmodel, geneesmiddelveiligheid, bijwerkingen van chemotherapie