Clear Sky Science · nl
CDK13 drijft clear-cell nierkanker via METTL16-gemedieerde m6A-modificatie van ACLY-mRNA
Waarom vetgevulde niertumoren ertoe doen
Clear-cell nierkanker ziet er onder de microscoop vaak bleek en vettig uit omdat de cellen vol liggen met vet. Die ongewone verschijningsvorm is niet alleen cosmetisch; ze weerspiegelt een diepere herprogrammering van hoe deze kankercellen hun brandstof verwerken. Deze studie stelt een eenvoudige maar belangrijke vraag: welke moleculaire schakel zet niertumorcellen aan tot het hamsteren van vet, en kan die schakel worden uitgeschakeld om de ziekte te vertragen?
Een verborgen dirigent van tumorgroei
De onderzoekers richtten zich op een eiwit genaamd CDK13, behorend tot een familie enzymen die normaal gesproken cellen helpen delen. Door grote patiëntendatasets en tumormonsters te analyseren, ontdekten ze dat CDK13-niveaus consequent hoger zijn in clear-cell nierkankers dan in normaal nierweefsel. Patiënten wier tumoren meer CDK13 hadden, leken grotere, meer gevorderde tumoren en slechtere uitkomsten te hebben. Wanneer het team CDK13 verlaagde in nierkankercellijnen, groeiden de cellen langzamer en hadden ze moeite door de celcyclus te komen, wat suggereert dat CDK13 fungeert als een verborgen dirigent die zowel groei als overleving coördineert.
Van suiker naar vet: het herbedraden van de brandstoffabriek
Aangezien clear-cell niertumoren vol lipiden zitten, onderzochten de onderzoekers of CDK13 ook regelt hoe deze cellen vet aanmaken. Met een combinatie van genexpressieprofilering en microscopische vetkleuringen toonden ze aan dat het opschroeven van CDK13 de ophoping van lipide druppels in kankercellen verhoogt, terwijl het verminderen van CDK13 het omgekeerde effect heeft. CDK13 beïnvloedde sterk een enzym genaamd ACLY, dat een veelvoorkomend metabolisch tussengproduct omzet in acetyl-CoA, het uitgangsmateriaal voor de opbouw van vetzuren en cholesterol. Hoge CDK13 ging samen met hoge ACLY in patiëntentumoren, en beide eiwitten waren geconcentreerd in dezelfde regio’s van het kankergewebe. Toen ACLY kunstmatig werd opgevoerd, herstelde dat veel van de groeien vetopslagdefecten veroorzaakt door verlies van CDK13, waardoor ACLY als een belangrijke downstream-effector van deze route werd geplaatst. 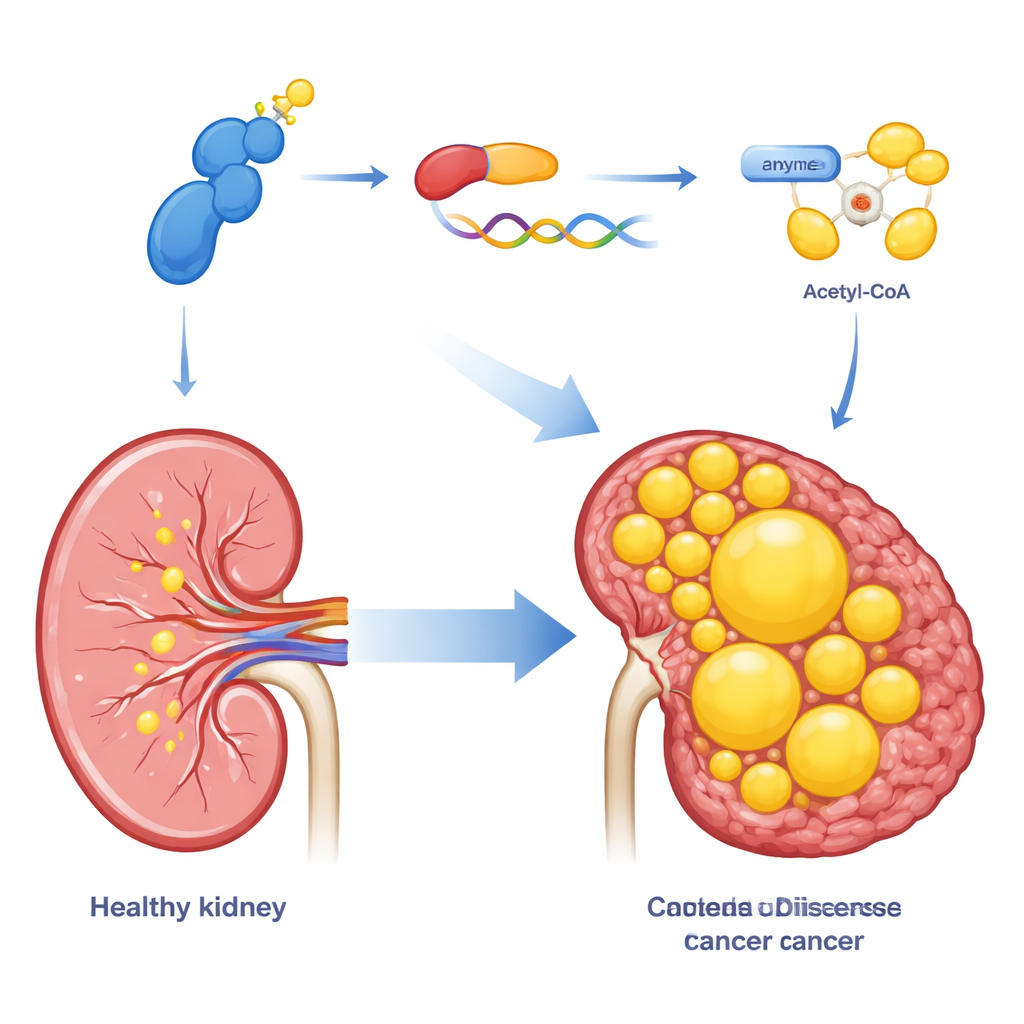
Een gelaagd berichtensysteem binnen kankercellen
In plaats van rechtstreeks op ACLY te werken als een simpele aan/uit-schakelaar, oefent CDK13 zijn invloed uit via een gelaagd berichtensysteem dat is opgebouwd rond RNA, het molecuul dat genetische instructies van DNA naar de eiwitfabrieken draagt. De auteurs ontdekten dat CDK13 fysiek bindt aan en chemisch een ander enzym, METTL16, modificeert, dat specifieke RNA-berichten voorziet van kleine chemische labels, methylgroepen genoemd. CDK13 voegt een fosfaatlabel toe aan METTL16 op een precies punt, waardoor METTL16 actiever wordt. Op zijn beurt plaatst METTL16 extra methyllabels op het RNA-blauwdruk voor ACLY. Deze labels veranderen de genetische code zelf niet, maar ze beïnvloeden hoe de cel dat bericht behandelt. Een derde eiwit, YTHDC2, herkent het gemarkeerde ACLY-RNA en beschermt het tegen afbraak, waardoor er in de loop van de tijd meer ACLY-eiwit geproduceerd kan worden. Deze cascade — CDK13 die METTL16 activeert, METTL16 die ACLY-RNA markeert, en YTHDC2 die dat gemarkeerde bericht bewaakt — creëert een krachtige keten die vetvorming aandrijft. 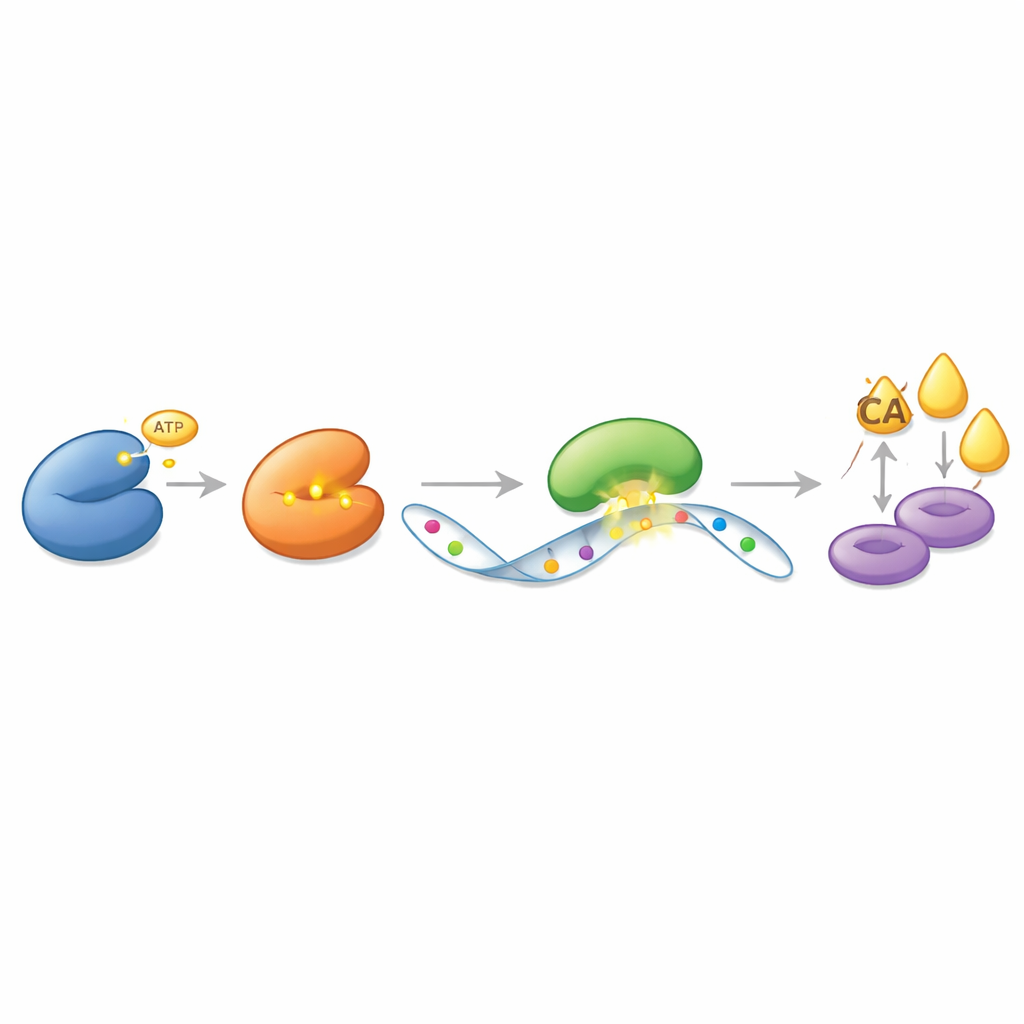
De keten testen in cellen, muizen en patiëntmonsters
De kracht van het werk ligt in hoe grondig de auteurs deze gebeurtenissenketen hebben getest. In gekweekte nierkankercellen verminderde het verstoren van eender welk deel van de CDK13–METTL16–ACLY-route de hoeveelheid lipidedruppels en vertraagde de proliferatie. In muizen waarin menselijke nierkankercellen waren ingeplant, deden het blokkeren van CDK13 of ACLY afzonderlijk de tumoren krimpen en verminderde de vetopslag erin, terwijl het blokkeren van beide samen een nog sterker effect had. Het team gebruikte ook een klein-moleculair compoud, 1NM-PP1, dat CDK13-activiteit remt. Deze geneesmiddelachtige stof verminderde het activerende label op METTL16, verlaagde ACLY-niveaus en onderdrukte tumorgroei, vooral wanneer gecombineerd met METTL16-uitputting. In verschillende patiëntendatasets neigden CDK13, METTL16 en ACLY samen op en neer te gaan, wat het idee versterkt dat deze as actief is in echte kankers, niet alleen in laboratoriummodellen.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat deze studie een nieuwe regelknop blootlegt voor de “vetfabriek” binnen clear-cell niertumoren. In plaats van alleen de enzymen aan te pakken die lipiden maken, laten de onderzoekers een hoger niveau van commando zien dat de instructies voor die enzymen stabiliseert. Door de CDK13–METTL16–ACLY-as te onderbreken, kan het mogelijk zijn tumoren te beroven van de vetten die ze nodig hebben om te groeien en uit te zaaien, terwijl normale cellen minder worden getroffen. Hoewel het werk nog preklinisch is en 1NM-PP1 nog geen nierkankergeneesmiddel is, wijzen de bevindingen op nieuwe strategieën die kinase-remmers koppelen aan middelen die RNA-modificerende enzymen targeten — een preciezere manier om deze metabolisch gedreven vorm van nierkanker te behandelen.
Bronvermelding: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Trefwoorden: clear-cell niercelcarcinoom, lipidenmetabolisme, CDK13, RNA-methylering, ACLY